
代謝性疾患
MASLD/MASHの疾患概念と肝臓から考える代謝疾患
サイトへ公開:2026年03月16日 (月)
ご監修:鎌田 佳宏 先生(大阪大学大学院医学系研究科 保健学専攻・生体物理工学講座 教授)

2023年、欧米の学会を中心に、脂肪性肝疾患の新たな分類・定義が提唱され、NAFLD/NASHはMASLD/MASHへと名称変更されました。
MASLD/MASHとNAFLD/NASHにはどのような違いがあるのでしょうか?これらの分類・定義の変更が代謝疾患の診療にもたらす影響とは。
MASLD/MASHのエキスパートである大阪大学大学院医学系研究科 保健学専攻・生体物理工学講座 教授の鎌田 佳宏 先生に、MASLD/MASHの疾患概念や肝臓からみた代謝疾患診療についてお話を伺いました。
Summary
- MASLDは脂肪性肝疾患に1つ以上の心代謝系危険因子の異常を満たすことで診断される1)
- 日本人はMASLD/MASHになりやすく病態進展しやすい民族であり2)、適切なスクリーニングと肝臓専門医による定期的なフォローが重要である
- 糖尿病合併MASLDや、複数の代謝リスク因子を有するMASLDはハイリスク症例である
- 近年の疫学研究から、脂肪肝があることが代謝疾患の新規発症リスクである可能性が示唆されており3)、肝臓機能の正常化が糖代謝や脂質代謝の正常化に重要な可能性がある
- 年齢、AST、ALT、血小板数から算出されるFIB-4 indexはMASLDの一次スクリーニングに有用であり4,5)、日常臨床に取り入れることが提案される
- EASL-EASD-EASO Clinical Practice Guidelines on the management of metabolic dysfunction-associated steatotic liver disease (MASLD).
J Hepatol. 2024; 81(3): 492-542. - Nishioji K, et al.: PLoS One. 2015; 10(10): e0140427.
- Demir M, et al.: Obes Rev. 2023; 24(10): e13612.
- Sumida Y, et al.: BMC Gastroenterol. 2012; 12: 2.
- Kamada Y, et al.: Nutrients. 2022; 15(1): 66.
脂肪性肝疾患の新分類“MASLD”とは
MASLD(metabolic dysfunction-associated steatotic liver disease)は従来のNAFLD(nonalcoholic fatty liver disease)に相当し、BMI高値、糖代謝異常、血圧高値、高中性脂肪血症、低HDL-C血症の5つの心代謝系危険因子のうち少なくとも1つ異常値を満たすことが条件とされます(図1)。
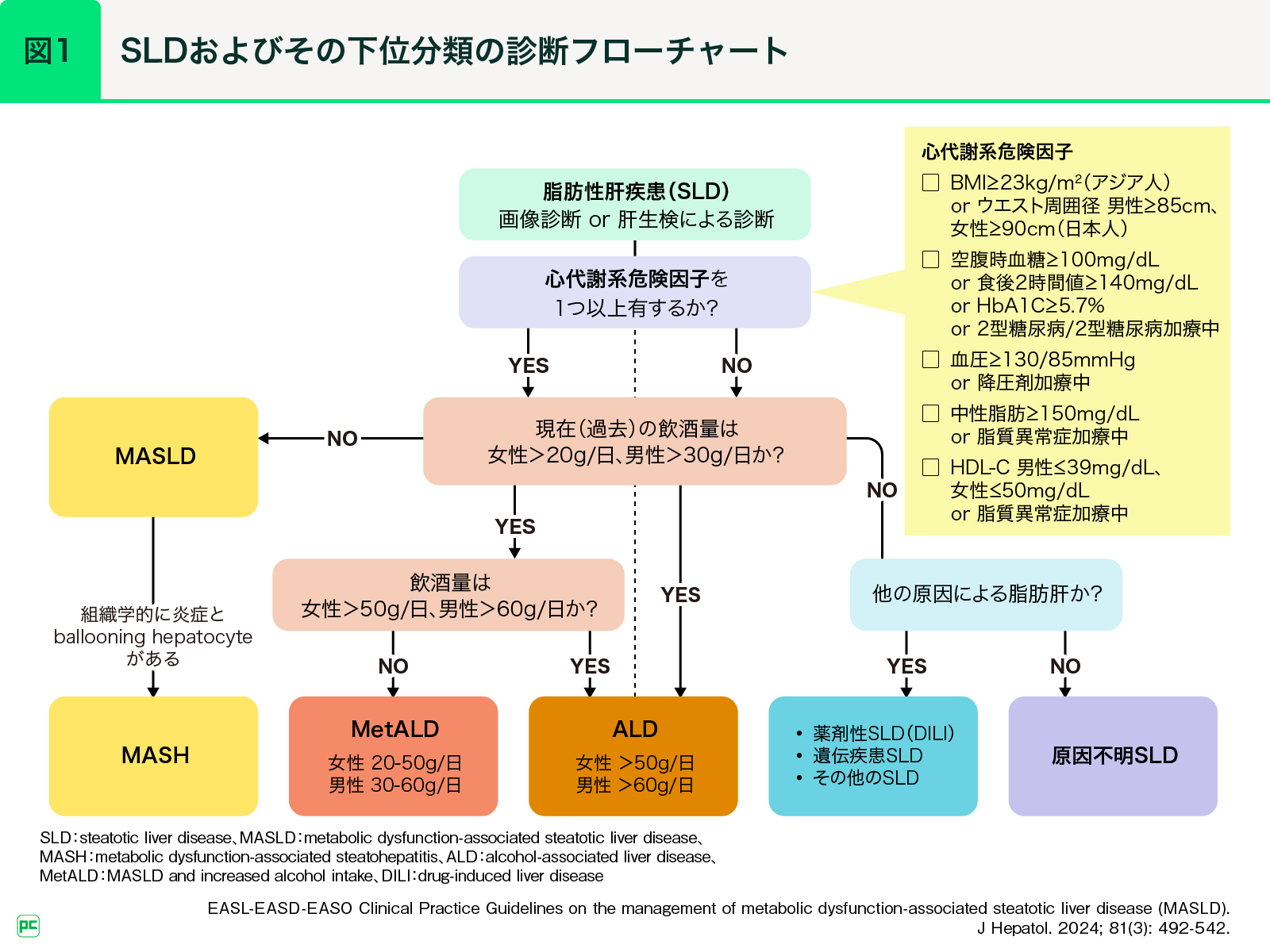
従来用いられてきたNAFLDに含まれる“fatty”や“alcoholic”がスティグマに該当するというのが名称変更の大きな理由で、“fatty”は“steatotic”に置き換わり、これにより日本での脂肪性肝疾患はfatty liver disease(FLD)からsteatotic liver disease(SLD)へと変更されました。また、従来のNASH(nonalcoholic steatohepatitis)はMASH(metabolic dysfunction-associated steatohepatitis)に変更されました。
MASLDとNAFLDでは診断基準が異なりますが、これらはほぼ同一疾患とみなすことができます。われわれが健診コホートを用いて調べたところ、MASLDとNAFLDの一致率は99%で1)、その他にも95~99%一致するとの報告が相次いでいます2-4)。したがって、今後は、過去の知見や現在進行している各種臨床試験についてもNAFLD/NASHをMASLD/MASHと読み替えていくことになると考えられます。
また、今回提唱された脂肪性肝疾患(以下、SLD)の新たな分類では、飲酒量が中間の群にMetALD(MASLD and increased alcohol intake)という病名がつき、飲酒量にかかわらずどこかに分類されるようになりました。これまでNAFLDとアルコール関連肝疾患(ALD;alcohol-associated liver disease)は病名がありましたが、MetALDに該当する方々は病名がつかなかったため、医療機関を受診していないケースも多いと考えられます。しかし、中には適切なフォローアップが必要な症例も含まれるため、こうした患者さんを疾患単位で対応できるようになったことは非常に重要です。
日本の成人4人に1人が罹患―MASLDを診断・フォローする必要性
MASLDは日本の成人の4人に1人が罹患するともいわれるCommon diseasesで5)、その患者数は国内に2,000万人以上と推計されます。このような多くのMASLD患者さんの中には、肝臓専門医が定期的にフォローすべき、線維化が進んだ症例や炎症の強い症例が含まれます。こうした症例をスクリーニングするためにも、代謝系のリスク因子をもつ患者さんでは、年1回は腹部エコー検査により脂肪肝の有無をチェックし、脂肪肝がみられ、FIB-4 index(FIB-4)や血液バイオマーカーなどによってハイリスクと判断された場合、一度肝臓内科を受診いただくことが推奨されます。
また、日本人はSLDになりやすく、病態進展しやすい民族であることが知られています。ゲノムワイド関連研究(GWAS)の結果、脂質代謝関連遺伝子であるPNPLA3がMASLDの発症および進展に重要な遺伝子であることが明らかとなっていますが6)、日本人は欧米人に比べてPNPLA3のマイナーアレル(G)保有率が高いことが報告されています7)。具体的には、マイナーアレルのホモ変異割合が、イギリス人では5%なのに対し、日本人では一般人口の約20%以上も存在します7,8)。これは、たとえば健診コホートでみた場合に20%以上ということであり、MASLD診断例や線維化進展例のコホートでは濃縮されてさらに割合が高まります。したがって、日本人ではMASLD/MASHの発症および進展に注意を要する方の割合が非常に多いと考えられます。こうした点からも、ハイリスク症例では肝臓専門医が定期的にフォローすることが大事であるといえます。
MASLDにおけるハイリスク症例とは
ではどのような症例がハイリスクなのかというと、まず注意が必要なのは糖尿病合併脂肪肝症例です。通常、MASLDの約10%がMASHといわれますが9)、糖尿病合併MASLDでは、58%がMASHであり、ステージ3,4の高度肝線維化症例が38%もいたとする報告があるくらい、炎症を起こしている頻度が高いことが知られています10)。2型糖尿病患者の5人に1人がステージ3,4であるとするレビューも報告されています11)。
また、最近はMASLDと高血圧の関連を裏付けるエビデンスも増加しており1,12)、その他にも、いわゆるメタボ関連疾患の合併が多く、複数の代謝リスク因子が存在するほど、疾患進行や肝細胞がんのリスクが高まることも知られています13)。そのため、糖尿病がまず重要であるものの、その他のメタボ関連疾患を合併しているかどうかもハイリスクを見極めるひとつの線引きになると考えられます。
さらに、MASLD症例は心血管疾患(CVD)のハイリスク症例でもあります。海外の研究ではMASLD患者の死因のトップはCVDで約40%を占めていました(図2)。このように、MASLDの予後決定因子としてCVDは重要な要素です。糖尿病や肥満症、脂質異常症といった代謝疾患のCVDリスクはすでに広く認知されているところですが、MASLDではSLDによるリスクも加わることになるため、心臓や脳梗塞のリスク層別化も大事になってくるでしょう。
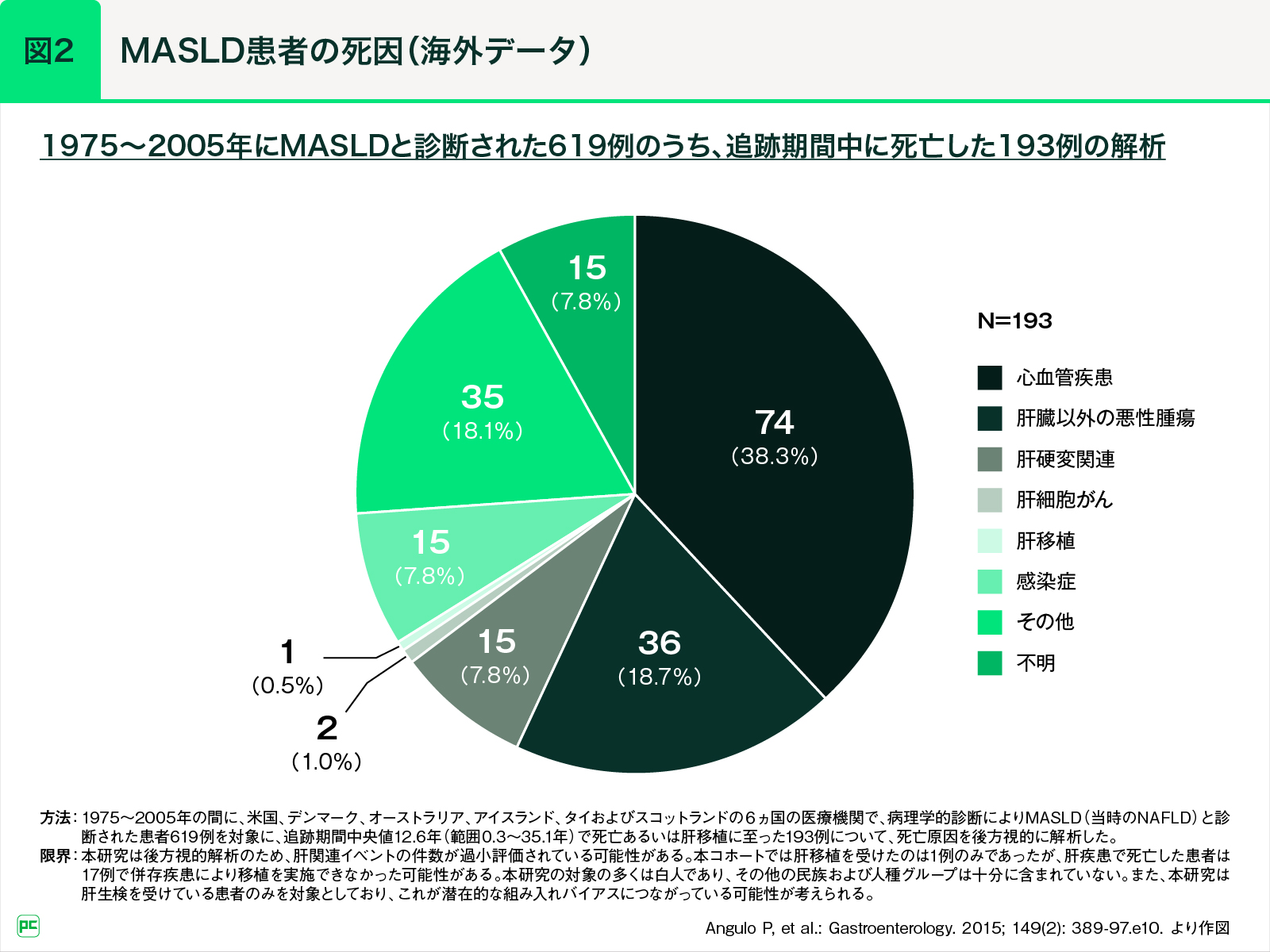
SLDを起点とした代謝疾患への影響
今、個人的に興味をもっているのは、SLDが各種代謝疾患に与える影響についてです。
近年の研究から、脂肪肝があることが代謝疾患の発症リスクである可能性が示唆されています14)。つまり、肥満を背景にSLDを発症し、そこから種々のメタボリックシンドロームが引き起こされる、という仮説が考えられます。この仮説を検証するため、現在われわれは、健診コホートを用いて脂肪肝の有無別に各種代謝疾患の新規発症リスクを解析しています。現状では、脂肪肝がない肥満の方は代謝疾患を発症しにくく、脂肪肝があると代謝疾患を発症しやすい傾向がみられています。
これは病態生理学的な観点で考えるとイメージしやすく、SLDは肝臓に脂肪が蓄積した状態であるため、当然、肝細胞の代謝機能が障害されることとなります14)。すると、血糖や脂質の代謝機能が低下し、さらに動脈硬化が惹起されることで高血圧にもなりやすいと考えられます。
肝臓は人体における代謝の中枢であり、糖代謝や脂質代謝を正常化するには、肝臓の機能を正常化することが非常に重要です。そういう意味では、各種代謝疾患を考えるうえで、肝臓は格好のターゲットであるといえるでしょう。
MASLDハイリスク群の拾い上げと専門医への紹介アルゴリズムの提案
最後に、どのような症例を肝臓専門医へ紹介すべきかという点について、FIB-4を用いた紹介アルゴリズムを提案します(図3)。アルゴリズムはいたってシンプルで、まず第1段階として、FIB-4により肝線維化マーカー測定や画像診断の必要性を判断します。FIB-4が1.3以上、65歳以上の場合は2.0以上であれば、第2段階として肝線維化マーカーまたはエラストグラフィで絞り込みを行います。そして、カットオフ値以上の場合に肝臓専門医へ紹介するというものです。
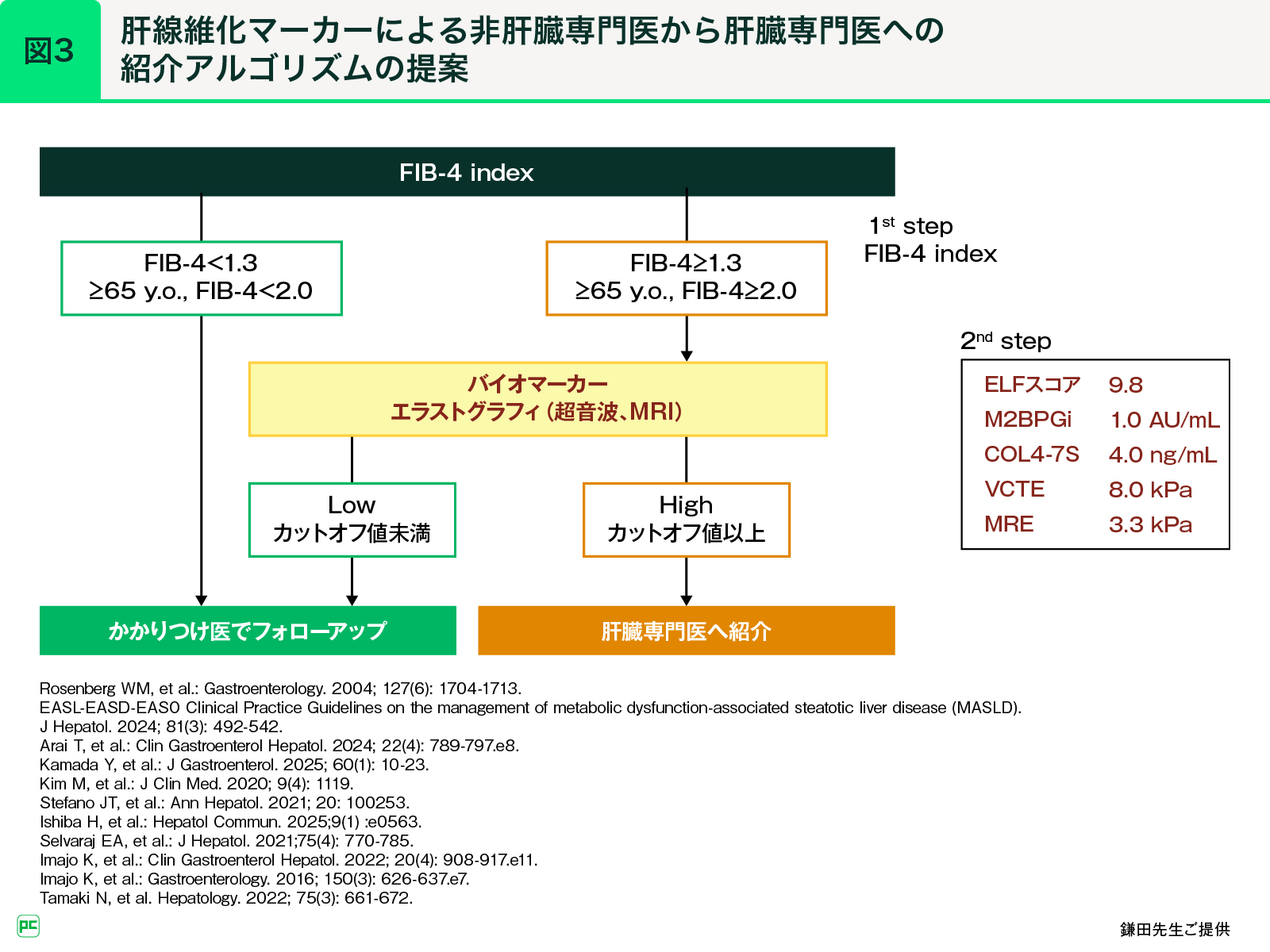
FIB-4は、年齢、AST、ALT、血小板数という4つのパラメータの組み合わせのみに基づいたシンプルなスコアリングシステムです。特に線維化進展例の除外診断に有効で15)、われわれの検討では、肝関連疾患のみならず、他臓器がんやMACEの予測因子としても機能することがわかっています16)。アメリカ糖尿病学会(ADA)の糖尿病診療ガイドラインでも、FIB-4が1.3以上の場合はエラストグラフィによる肝硬度測定、あるいはELF testを使ってリスク層別化すべきとされています17)。代謝疾患をメインに診療される先生方は、血小板数を測定していないケースも多いと考えられるため、まずは血小板数の測定という1ポイントを取り入れていただけたらと思っています。
次のステップのバイオマーカーやエラストグラフィについても、非肝臓専門医の先生には、保険収載されているさまざまな手法のうちどれか1つ得意になっていただいて、その1つがわれわれの提唱する数値を超えている場合に紹介していただくという単純なフローとしています。
ただし、本アルゴリズムは、自分のところで詳しく調べたうえで紹介したいという先生方に向けて、特に危険な患者さんをスクリーニングすることを目的として提案するものです。糖尿病をはじめとする代謝疾患をもつ患者さんでは、脂肪肝があるとわかった段階で一度紹介していただいてもよいという点は強調しておきたいです。
Take home message
国内のMASLD患者数は2,000万人以上と推計され、こうした多数の患者さんから、日常診療の中でハイリスク症例を囲い込んでいくことが重要です。
最近では、保険適用可能な非侵襲的検査が複数登場し、日常臨床で気軽にスクリーニングできるようになりました。MASLDはCVDや代謝疾患のリスクでもあることをぜひ心にとめていただき、何か1つ得意な検査を設定することで、リスクの疑われる患者さんを肝臓専門医に連携していただけたらと思います。
- Kamada Y, et al.: Gastro Hep Adv. 2024; 3(8): 1148-1156.
- Loomba R, et al.: Aliment Pharmacol Ther. 2024; 59(2): 150-156.
- Suzuki K, et al.: Hepatol Res. 2024; 54(6): 600-605.
- Younossi ZM, et al.: J Hepatol. 2024; 80(5): 694-701.
- Fujii H, Kamada Y, et al.: Hepatol Res. 2023; 53(11): 1059-1072.
- Romeo S, et al.: Nat Genet. 2008; 40(12): 1461-1465.
- Nishioji K, et al.: PLoS One. 2015; 10(10): e0140427.
- Liu YL, et al.: J Hepatol. 2014; 61(1): 75-81.
- 日本肝臓学会 編:NASH・NAFLDの診療ガイド2021, 文光堂, 2021. p52
- Castera L, et al.: Diabetes Care. 2023; 46(7): 1354-1362.
- Wongtrakul W, et al.: J Gastroenterol Hepatol. 2024; 39(11): 2299-2307.
- Li G, et al.: Int J Endocrinol. 2022; 2022: 8463640.
- Kanwal F, et al.: Hepatology. 2020; 71(3): 808-819.
- Demir M, et al.: Obes Rev. 2023; 24(10): e13612.
- Sumida Y, et al.: BMC Gastroenterol. 2012; 12: 2.
- Kamada Y, et al.: Nutrients. 2022; 15(1): 66.
- American Diabetes Association Professional Practice Committee. Diabetes Care . 2025; 48(Supplement_1): S59-S85.
この記事はお役に立ちましたか?
その他の関連情報




