
PF-ILD診療の歴史とINBUILD試験を振り返る(静止画)
サイトへ公開:2025年08月28日 (木)
クイックリンク
ご監修・ご出演:井上 義一 先生(大阪府結核予防会 大阪複十字病院 顧問、独立行政法人 国立病院機構 近畿中央呼吸器センター 臨床研究センター 客員研究員)

抗線維化剤オフェブは2015年に発売され、2020年に進行性線維化を伴う間質性肺疾患(PF-ILD)に対する適応を取得しました。
本コンテンツでは、大阪府結核予防会 大阪複十字病院 顧問、独立行政法人 国立病院機構 近畿中央呼吸器センター 臨床研究センター 客員研究員 井上 義一先生にオフェブ登場による間質性肺疾患(ILD)治療の変化や診療への影響の振り返りとともに、今後のPF-ILD治療の課題についてお伺いしました。
インタビュー実施日:2025年4月22日
インタビュー実施場所:ホテル阪急インターナショナル
PF-ILDという概念の登場背景
PF-ILDという概念は、どのような医学的背景から登場したのでしょうか?
特発性間質性肺炎(IIPs)は多様性に富んでいて、症例ごとに所見や経過が異なることの多い疾患です。典型例であれば分類できても、実際には非典型的なものが多く、その非典型例をどのように管理していくかは以前から議論されていました。
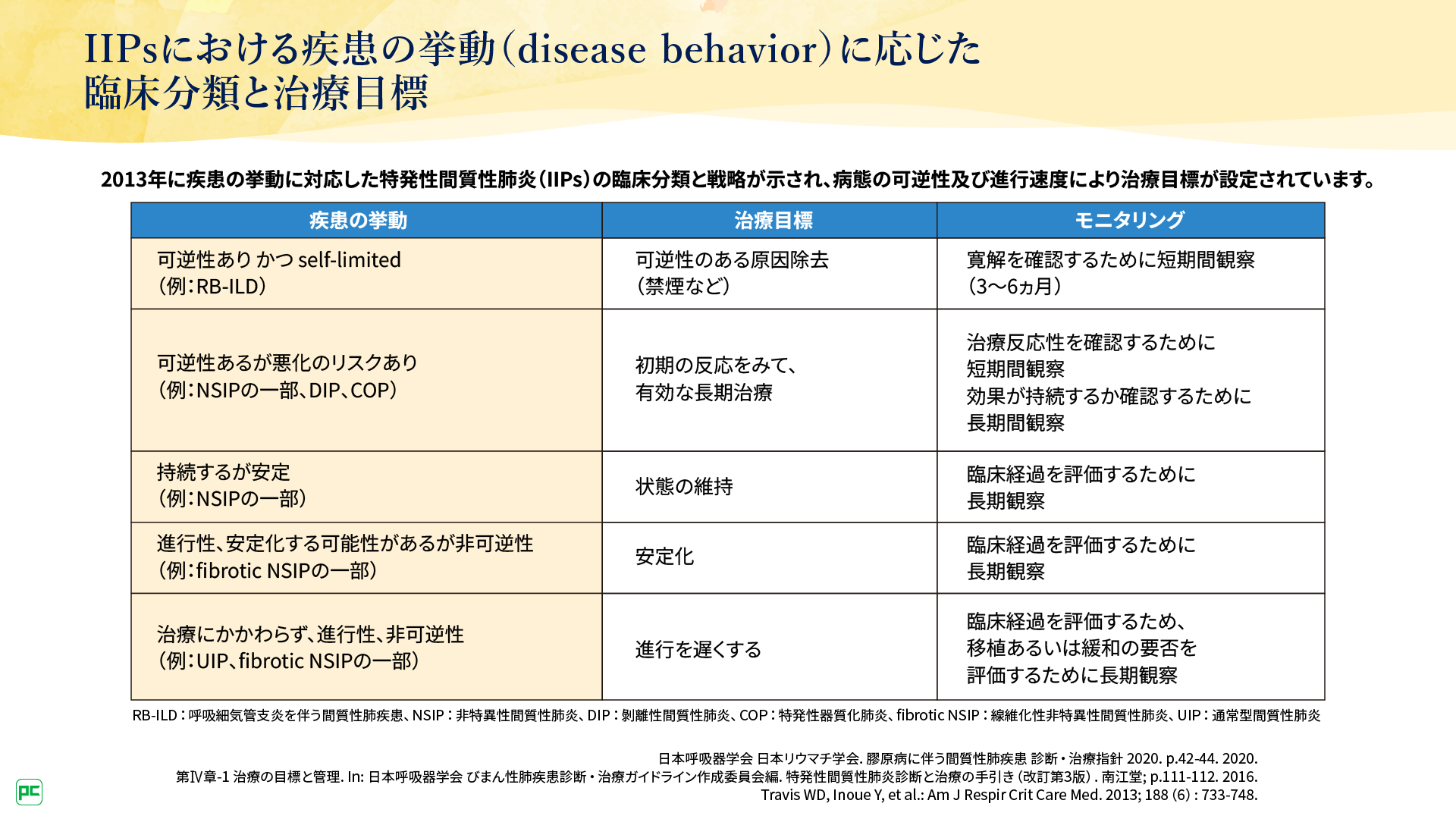
2013年に発表されたアメリカ胸部学会/欧州呼吸器学会(ATS/ERS)による特発性間質性肺炎の分類に関するステートメント1)では、形態学に基づいてIIPsを特発性肺線維症(IPF)や特発性非特異性間質性肺炎(iNSIP)などに分類していますが、さらに診断がはっきりしない場合の管理方法として、病態の可逆性や進行速度など疾患挙動(disease behavior)に応じた臨床分類が提案されました(図1)。この臨床分類では、診断名にかかわらず、疾患がどのように挙動するかによって治療目標や管理方法が設定されました。
たとえばIPFと類似した、病態が進行性かつ非可逆性のIIPsの場合、IPFに準じて進行を遅くすることが治療目標となります。
2008年にピルフェニドン、2015年にオフェブと2つの抗線維化剤が世界に先駆けて日本でIPFに対する治療薬として登場しました。すでに述べたような背景から、オフェブはさらにIPF以外のILDにおける有効性・安全性についても試験を行う運びとなり、全身性強皮症(全身性硬化症、SSc)で治験が開始されました。さらにIPF以外の疾患の治験が検討された結果、IPF類似の疾患挙動をまとめてオフェブの有効性と安全性を検討することになりました。こうしてPF-ILDが定義され、INBUILD試験が開始されました。

図1
INBUILD試験を振り返って
本試験では具体的にどのような組み入れ基準が設定されましたか?
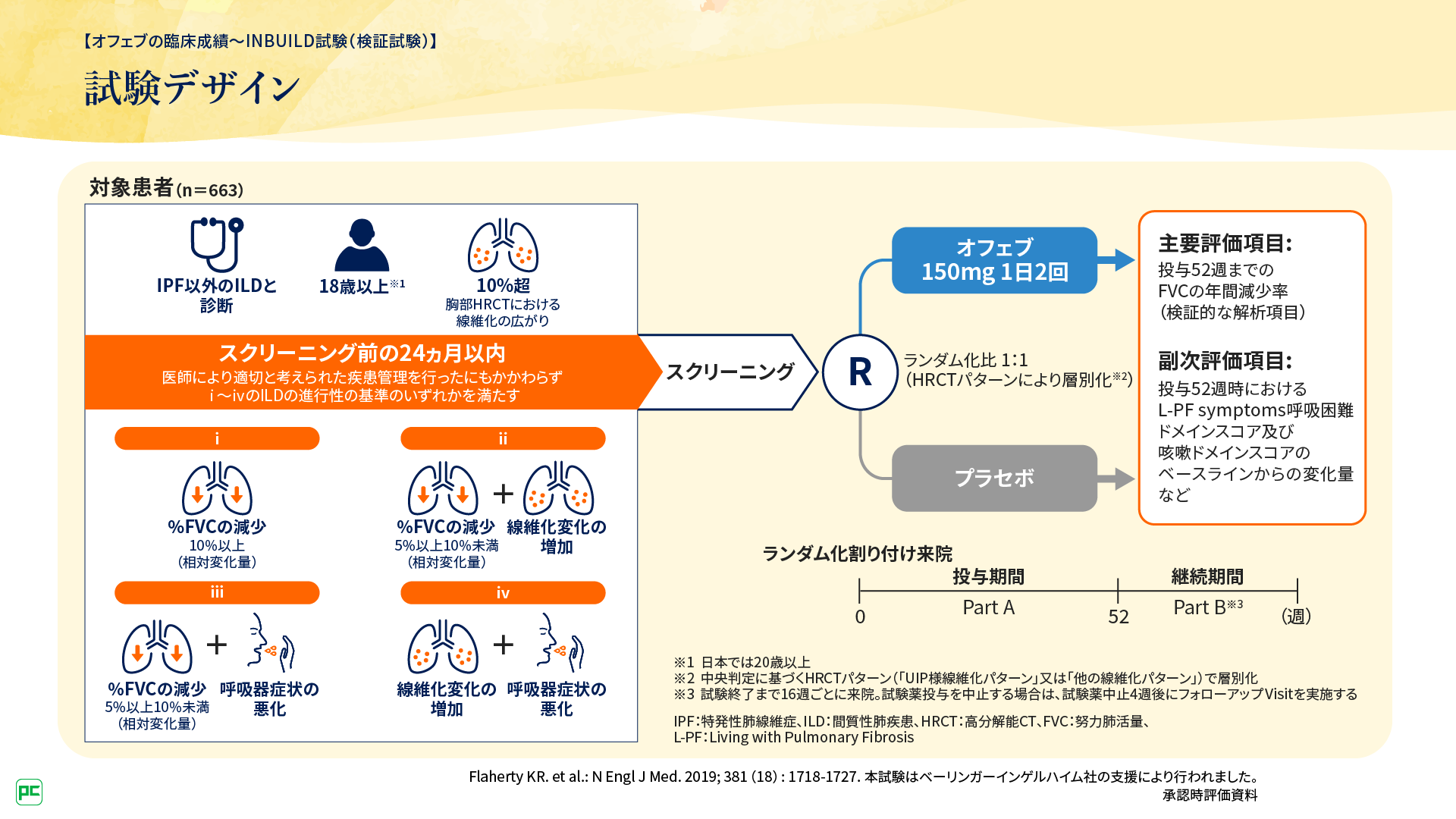
INBUILD試験では、「IPF以外のILDと診断」「18歳以上※」「胸部高分解能CT(HRCT)における線維化10%超」といった組み入れ基準のほかに、「対標準努力肺活量(%FVC)の減少」「胸部HRCTにおける線維化変化の増加」「呼吸器症状の悪化」を組み合わせた基準が設定されました(図2、3)。
※日本においては20歳以上
このようにINBUILD試験の組み入れ対象は、個々の疾患とする従来の考え方とは異なり、ILDのうち線維化がだんだんと進行している一群という捉え方をしました。PF-ILDというこれまでにない新しい概念の基準を仮定して新薬の開発を行う、当時としてチャレンジングな試験でありました。
図2

図3
INBUILD試験の結果について教えてください。
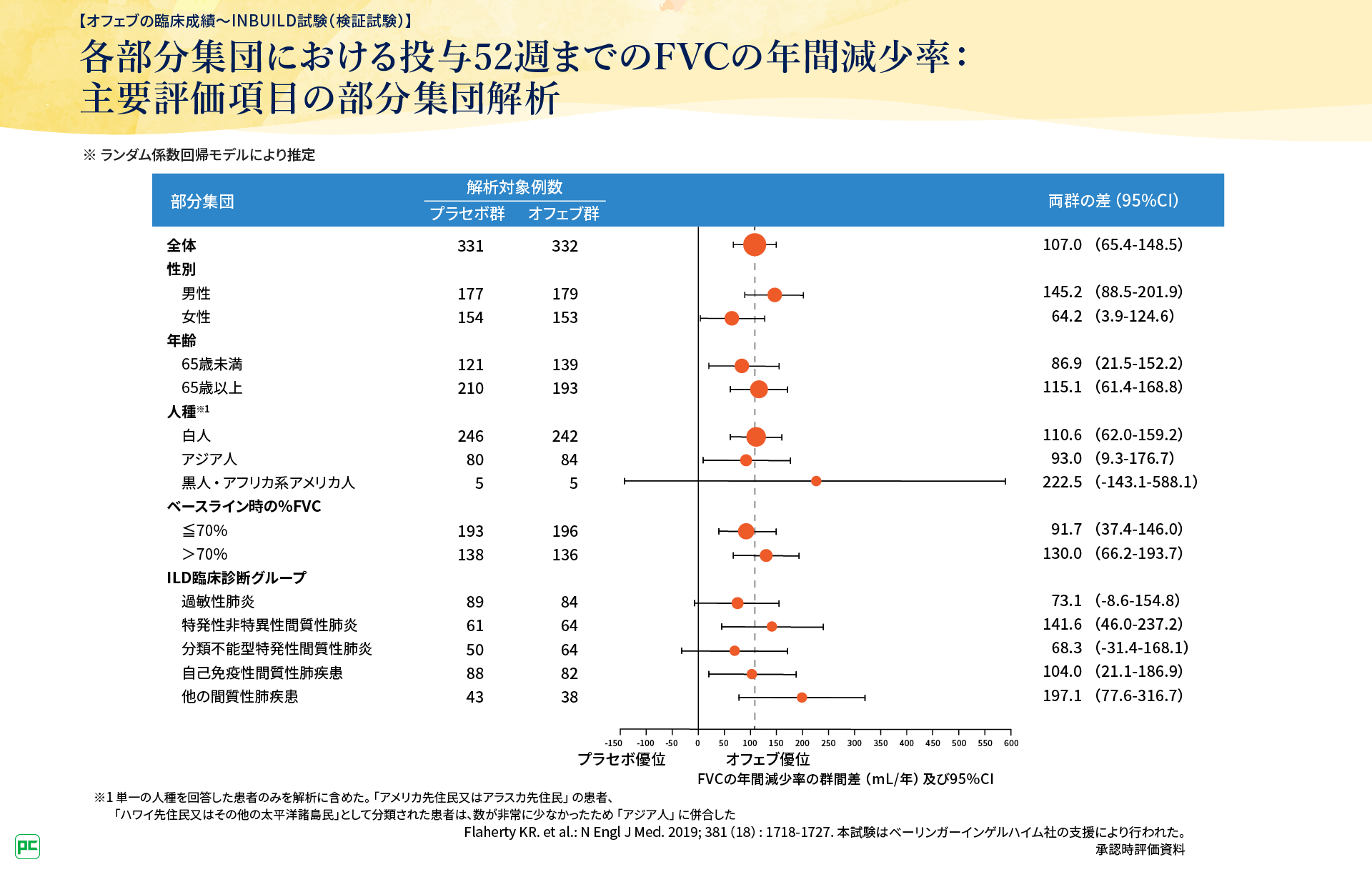
INBUILD試験の主要評価項目は、投与52週までのFVCの年間減少率でした。この結果、オフェブはプラセボに対し呼吸機能の低下を有意に抑制することが検証されました(p<0.0001, ランダム係数回帰モデル)(図4)。また%FVCを含む、さまざまなベースラインで部分集団解析を実施した結果、交互作用のp値0.05を基準として主要評価項目に影響を与えるベースラインの部分集団はみられませんでした(図5)。
図4
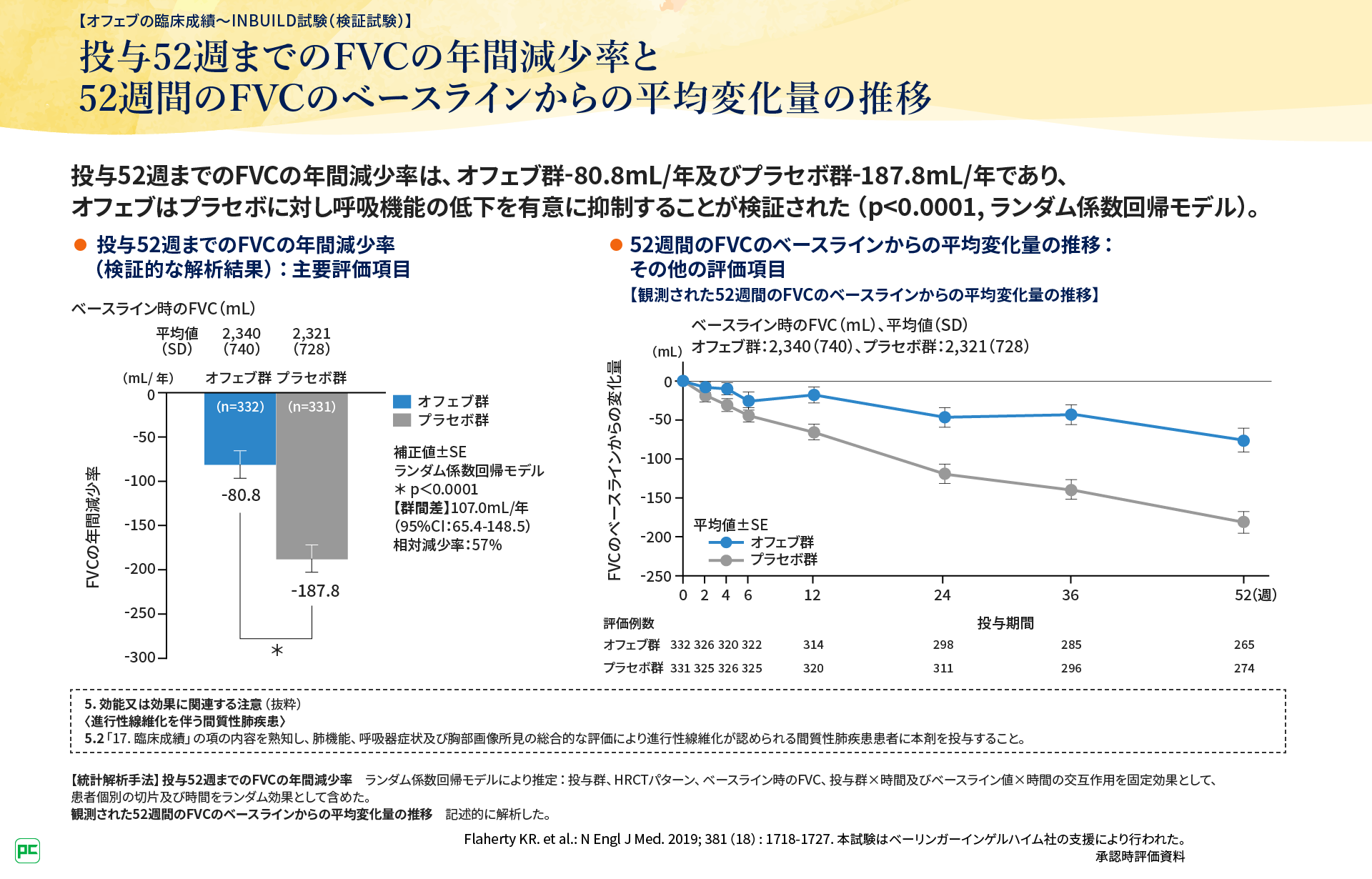
図5
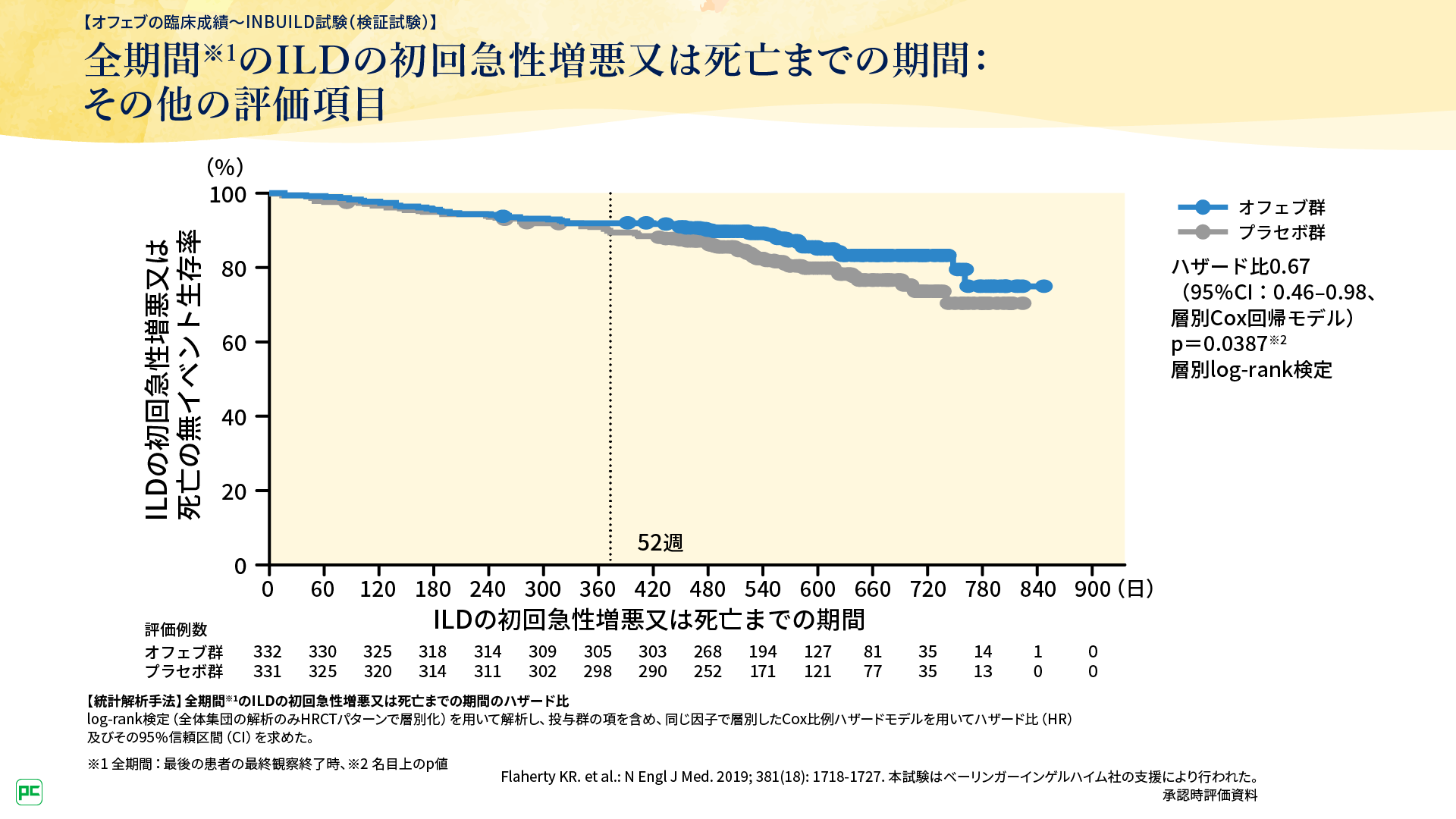
全期間※のILDの初回急性増悪又は死亡までの期間の解析で、オフェブ群のプラセボ群に対するハザード比は0.67であり(p=0.0387、層別log-rank検定、名目上のp値)、オフェブ群では急性増悪や死亡のリスクの低下がみられました(図6)。
※最後の患者の最終観察終了時
図6
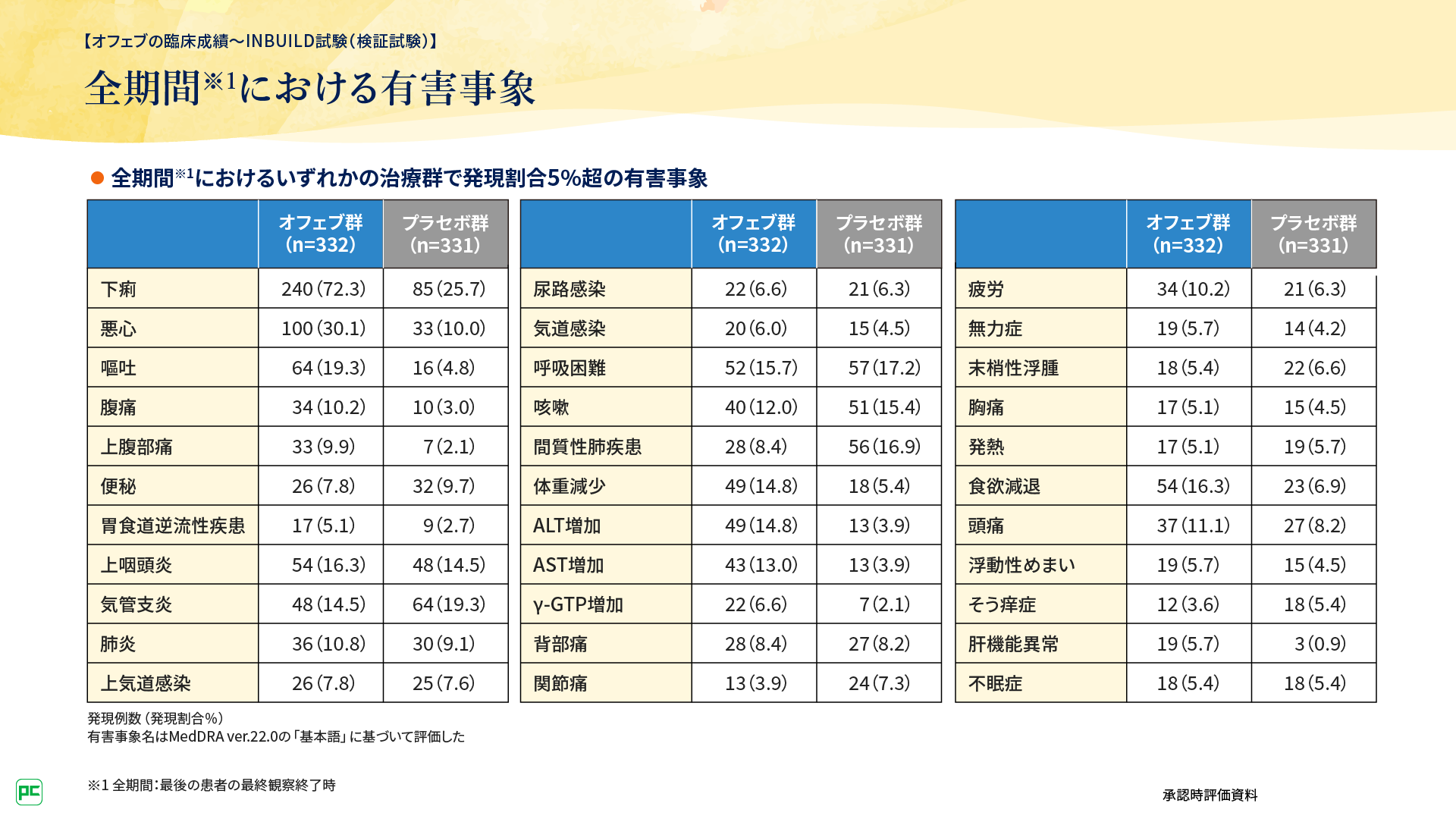
また、有害事象はオフェブ群では332例中326例(98.2%)、プラセボ群331例中308例(93.1%)に認められました。オフェブ群における主な有害事象として下痢(72.3%)や悪心(30.1%)、嘔吐(19.3%)などが認められました。重篤な有害事象は147例に認められ、主なものは肺炎24例、間質性肺疾患19例、急性呼吸不全16例でした。(図7、8)。
図7

図8
INBUILD試験の結果をご覧になった当時の印象はいかがでしたか?
一般的に、PF-ILDのように複数の疾患にまたがったグループでは背景のバラつきが大きく、それだけ統計学的有意差が出にくいと考えられます。ILDの領域での試みは初めてで、うまくいくだろうかと心配していたところ、有意な結果が示されました。
INBUILD試験の結果によって、オフェブがIPF、SSc-ILDに加えてPF-ILDに対しても適応となったことで、それまで治療が限られていた線維化性ILDsの患者さんの治療選択肢が増えたことは意義深い成果だったと思います。
PF-ILDからPPFへ
近年は進行性肺線維症(PPF)という分類も登場していますが、PPFはPF-ILDとどのように関連していますか?
進行性線維化を伴う間質性肺疾患(PF-ILD)はINBUILD試験で定義され、日本ではPF-ILDとしてPMDAに承認されました。しかし海外では“進行性フェノタイプを伴う慢性線維化性間質性肺疾患(Chronic fibrosing ILDs with a progressive phenotype)”として承認されました。
2022年のATS/ERS/日本呼吸器学会(JRS)/ラテンアメリカ胸部協会(ALAT)による臨床診療ガイドライン2)では、これを進行性肺線維症(PPF)として新しく定義しました。ガイドライン委員会ではPF-ILDとして定義したINBUILD試験とは異なる基準が提示されました。委員会でINBUILDを用いなかった理由は、治験で製薬メーカーが定義した名称であること、ほかいろいろな議論の後にPPFが採用されました。国際ガイドラインで定義されたことから、今後はPPFの名称に統一されていくものと思われます。
ガイドラインにおけるPPFの定義には肺拡散能(DLco)が含まれ、また前治療の有無など、INBUILD試験の組み入れ基準と異なっており、2025年段階でエビデンスはありません。現在PPFの名称を用いながらPF-ILDの基準が用いられることが多く、混乱が続いていますが、今後の研究で明らかにされ固まってくると考えられます。

今後の課題
今後のPF-ILD治療における課題は何でしょうか?
ILDの診療においては進行性の線維化を早期に見極めることが重要ですが、抗線維化剤による治療をいつ開始するのが最適なのかはまだ明らかになっていません。
抗線維化剤のほかに免疫抑制薬や生物学的製剤が治療選択肢になる疾患であれば、患者さんの個々に適した組み合わせや順番について今後検討されていくべき課題だと考えます。
最後に、ILD診療に携わる先生方へのメッセージをお願いします。
近年、個々の患者さんに応じた精密医療の実践において、Treatable Traits(治療可能な特性)に応じた治療管理が提案されています。Treatable Traitsとは、疾患の表現型やエンドタイプのうち、予後不良と関連するなど臨床的に重要であり、バイオマーカーによって特定することができ、治療が可能であるものと定義されています3)。
PF-ILD(PPF)はILDにおけるTreatable Traitsのひとつと見なされており3)、バイオマーカーなどで進行性の線維化を見極めて個々の患者さんに適した治療を選択することが重要と考えられています。
オフェブによる治療は線維化性ILDの治療管理における基本のひとつであり、下痢や肝障害の副作用を適切に管理しながら長期に治療を行っていくことが重要だと考えます。
まとめ
- INBUILD試験の対象は、個別の疾患ではなく間質性肺疾患のうち線維化が進行していく一群として捉えられ、この対象が「進行性線維化を伴う間質性肺疾患(PF-ILD)」と名付けられた。
- 複数の疾患にまたがるINBUILD試験の有効性・安全性の結果から、それまで治療が限られていた患者さんにも治療選択肢がもたらされた。
- 近年、日本での呼称であるPF-ILDは、欧米で進行性肺線維症(PPF)として新たに定義されている。
- 今後の課題として、最適な治療開始時期や個々の患者さんに適した治療戦略の検討が挙げられる。
その他の関連情報


特発性肺線維症および進行性肺線維症 国際診療ガイドライン2022(静止画)
日本ベーリンガーインゲルハイム
メディカルチャット 利用規約
当社の「日本ベーリンガーインゲルハイム メディカルチャット」(以下「本サービス」といいます)のご利用に際しては、本利用規約が適用されますので、必ず以下の記載事項をご確認下さい。
利用規約
- 本サービスは、当社所定のウェブページから文字によりお問い合わせいただくことにより、当社医薬品等に関する一般的な情報を、人工知能あるいは当社担当者により、文字及び図表により回答するサービスです(以下、人工知能による回答サービスを「AIチャット」、当社担当者による回答サービスを「有人チャット」といいます。)。ただし、AIチャットによる回答を原則とし、有人チャットは、AIチャットでの回答に対し、有人チャットでの回答も希望された場合に、提供させていただきます。
- 本サービスをご利用いただくことができるのは、当社医薬品等を扱いかつ国内に在住する医療関係者の方に限られます。当該医療関係者以外の方は、ご利用いただくことができません。
- 本利用規約に同意いただけない場合、本サービスを利用いただくことができません。本利用規約を最後までお読みいただき、「同意して利用する」ボタンを押した上で、本サービスをご利用下さい。
- 本サービスは、当社医薬品等に関する一般的なお問い合わせに対して回答するものとし、次の各号に掲げるお問い合わせについては、回答しないものとします。
- 当社医薬品等と関係のないお問い合わせ、または本サービスの回答範囲を逸脱したお問い合わせ
- 具体的な症状や治療方法に関するお問合せ
- 当社に適用される法令、ガイドラインまたは行政上の指導、当社自主規制その他当社が遵守すべきルールにより回答できないお問い合わせ
- 文字化け等により入力内容が判断できないお問い合わせ
- 前各号に掲げるほか、本サービスにより、適切な回答をすることができないと当社が判断した事項に関するお問い合わせ
- 本サービスは、日本語のみに対応しています。
- 本サービスは、当社医薬品の副作用、不具合及び有害事象の報告を受け付けていません。
- お問い合わせの内容によっては、本サービスでは十分に回答できない場合もございます。予めご了承下さい。
- 本サービスの利用可能時間は、以下のとおりです。
- AIチャット
24時間365日 - 有人チャット
平日9:00~17:00
- AIチャット
- 前項に関わらず、メンテナンス及び障害等のため一時的に本サービスを中断する場合がございます。
本サービスのご利用の際には、原則として、個人情報(お名前、ご住所、電話番号、メールアドレス等)を入力しないようお願いします。ただし、AIチャット及び有人チャットを問わず、当社医薬品の適用外使用に関するお問い合わせについては、コンプライアンス上の理由により、当社より、氏名及び施設名の入力を求める場合がございます。この場合には、当社プライバシーポリシーの内容を確認いただき、同意いただける場合に限り、入力して下さい(プライバシーポリシーについては「VIII 利用規約、プライバシーポリシー」に記載のURLからアクセス下さい)。その他の場合に、当社より個人情報の入力を求めることは一切ございません。
- 当社医薬品のご使用にあたっては、最新の添付文書等をご確認下さい。
- 当社は、本サービスまたは本サービスにより提供される情報の利用に際し生じた結果については、一切責任を負いません。
本サービスの利用にあたり、以下の各号の行為を禁止します。
- 本サービスにより提供される情報を複製、複写、転載、改変等する行為
- 第三者または当社の知的財産権その他の権利を侵害する行為
- 第三者または当社を誹謗中傷し、または名誉・信用を毀損する行為
- 本サービスの利用による営利目的の行為
- 本サービスの運営又は他の利用者による本サービスの利用の妨げとなる行為
- 前各号のほか、当社が不適当であると判断する行為
当社は、いつでも本サービスの提供を終了、またはその内容を変更することができるものとします。
本サービスの利用に関しては、以下の利用規約及びプライバシーポリシーが併せて適用されますので、ご確認下さい。



