
特発性肺線維症(IPF)診療の今とアンメットニーズ(静止画)
サイトへ公開:2026年03月30日 (月)
クイックリンク

間質性肺疾患(ILD)は、肺の間質に線維化や炎症などの病的変化が生じる疾患群で、原因不明の特発性間質性肺炎(IIPs)、関節リウマチなどの膠原病による自己免疫性ILD、過敏性肺炎などの職業環境性ILD、薬剤性などの医原性ILD等、200以上の疾患が含まれます1)。IIPsの中で最も多いのは特発性肺線維症(IPF)で、生存期間中央値は3~5年と予後不良であり、早期診断・治療が重要となります1)。
ここでは、IPFの病態、生命予後、診断と治療の現状を踏まえ、IPF診療の今をレビューし、今なお残るアンメットニーズについて解説します。
間質性肺疾患の病態と疾患負荷
肺の線維化は、繰り返される肺の損傷に続く、異常な創傷治癒反応によって生じます(図1)。肺胞上皮細胞や血管内皮細胞が損傷すると、組織修復のために様々な炎症・線維化反応が誘導されます。炎症と線維化の相互作用は疾患プロセスの早期からはじまり、慢性化して制御不能になることで、肺の線維化が生じます。ILDには、線維化が中心のものと炎症が主体のものがありますが、炎症が主体であっても、病態の進行により線維化が進行する可能性があります。
図1
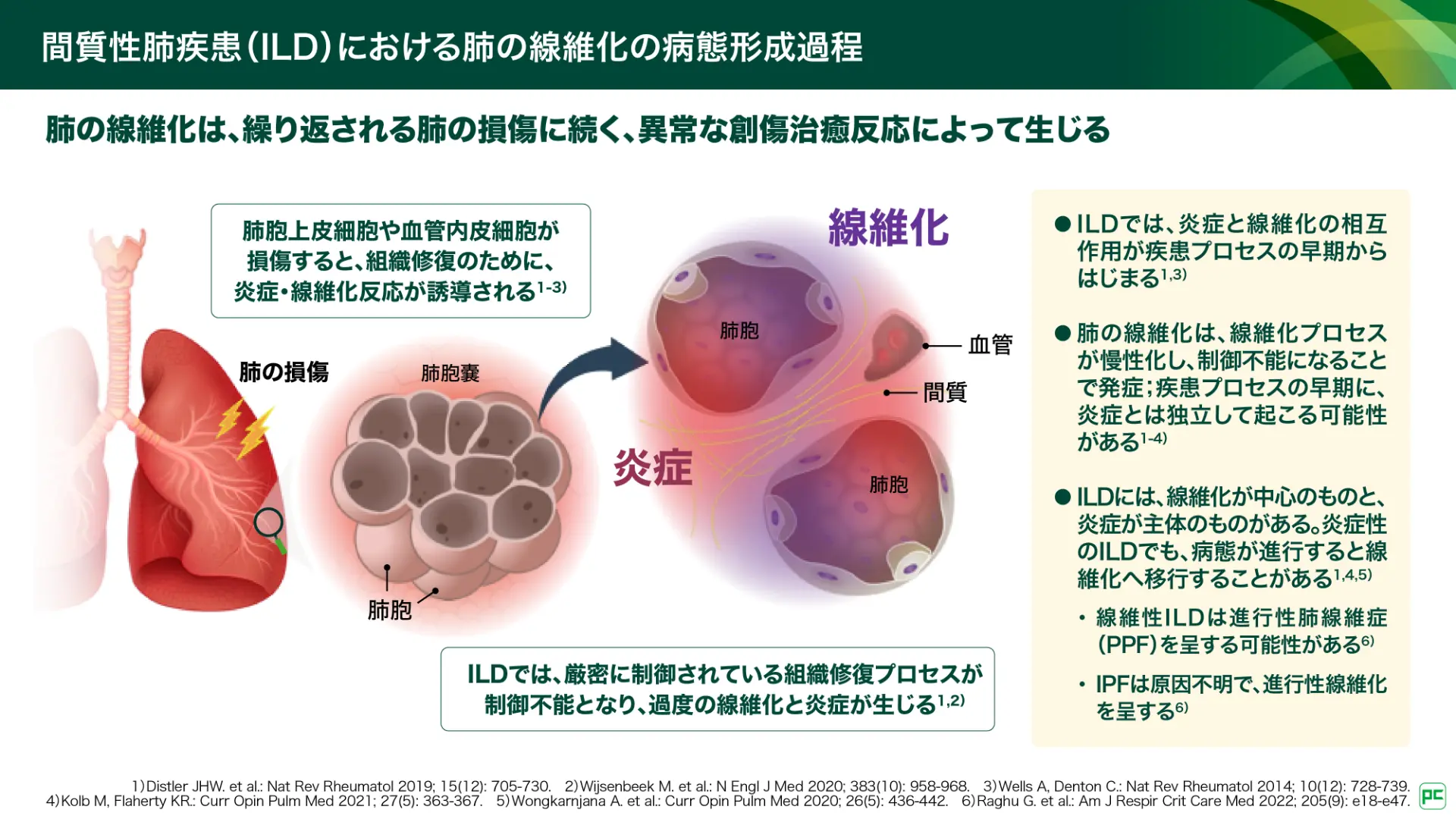
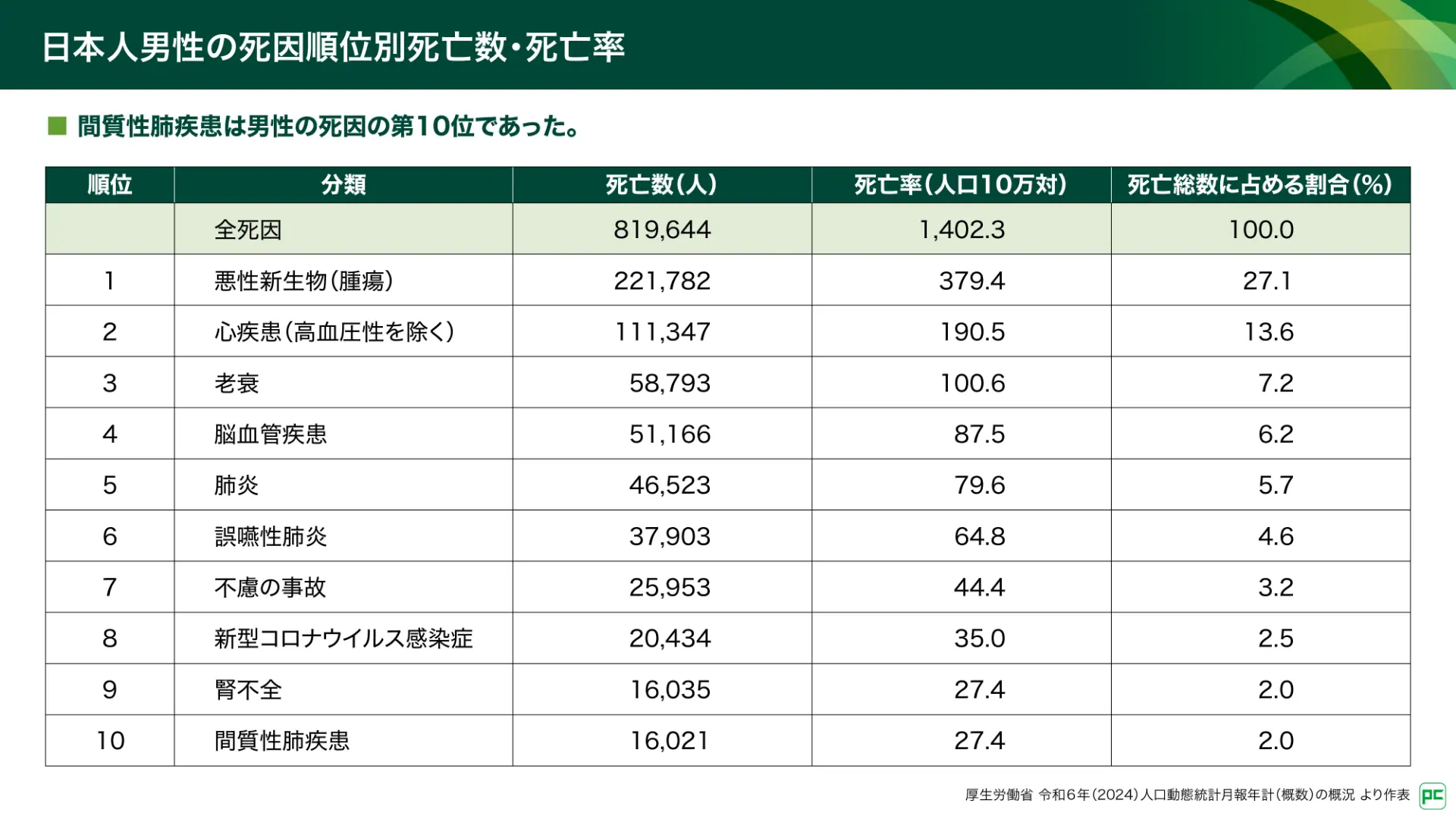
ILDの主症状は咳嗽、呼吸困難、及びそれに伴う疲労感です(図2)。これらの症状は、入院や死亡などの健康への影響に加え、身体・社会的活動の低下や失職などの身体機能的影響、うつ病や自立性の喪失、恐怖感などの感情的な影響を引き起こし、患者さんの生活を多岐にわたって変化させます。また、2024年の人口動態統計によると、日本人男性において、ILDによる死亡者数は16,021人、死因の第10位を占めており、社会的にもその対応が重要となっています(図3)2)。
図2
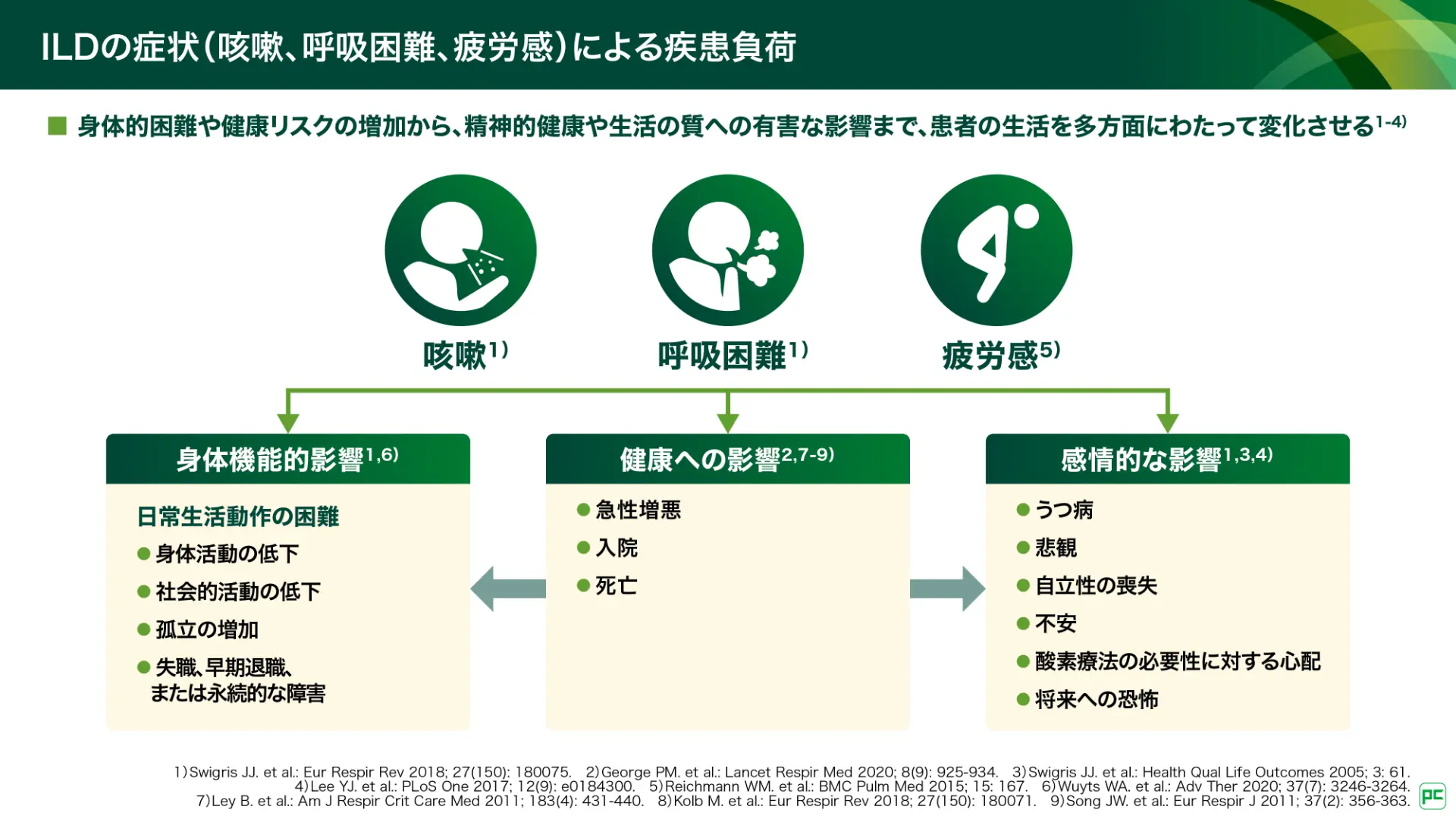
図3
日本におけるIPFの有病率
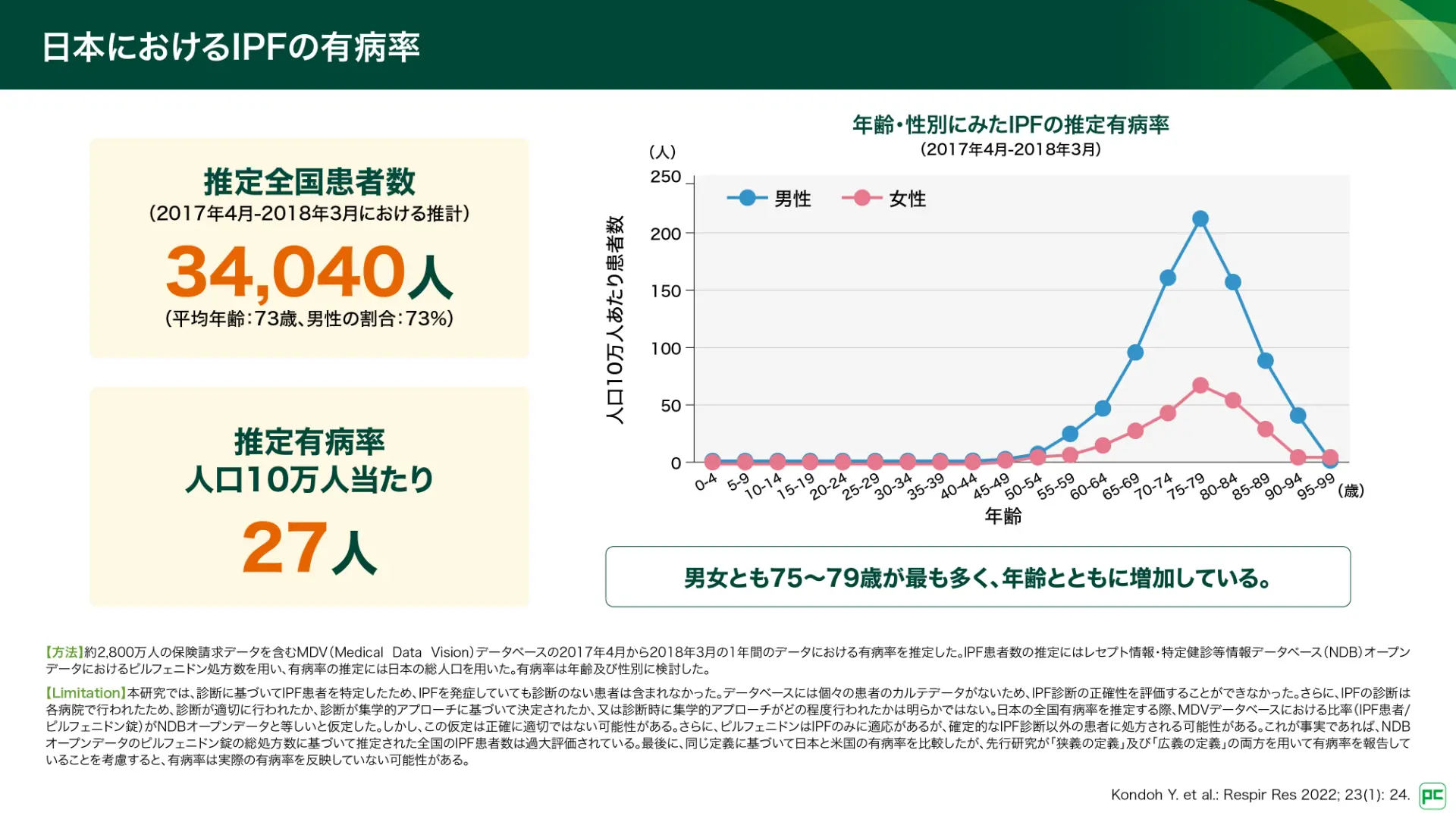
日本におけるIPFの患者数は34,040人、有病率は人口10万人当たり27人と推定されています(図4)3)。平均年齢は73歳で、男性が73%と多くを占めています。年齢・性別にみた推定有病率では、男女とも75~79歳が最も多く、年齢とともに増加しています。
図4
抗線維化薬登場後のIPFの生命予後
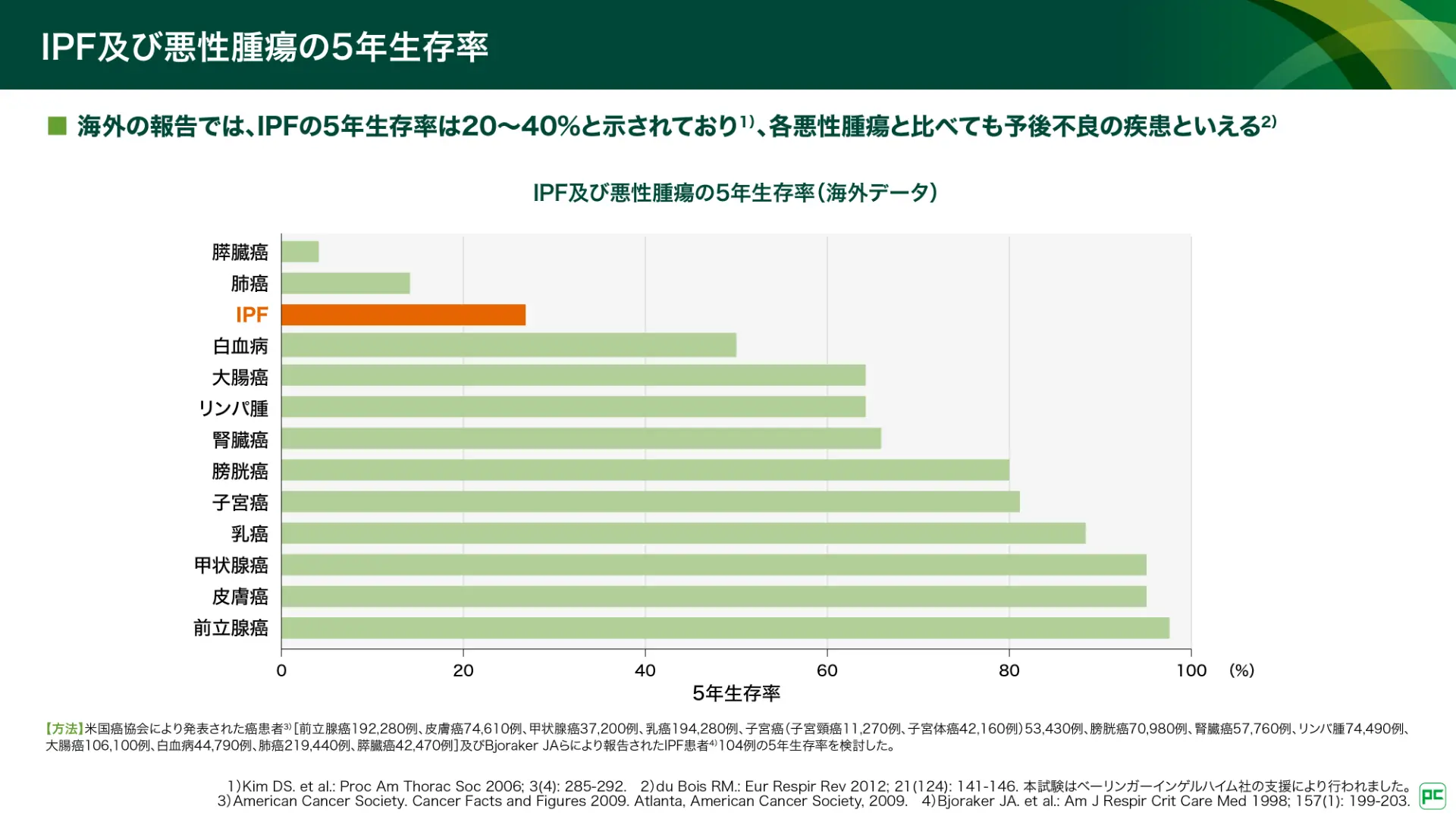
IPFの5年生存率は20~40%と報告されており4)、各悪性腫瘍と比較しても膵臓癌や肺癌に次いで低く、予後不良の疾患です(図5)5)。
図5
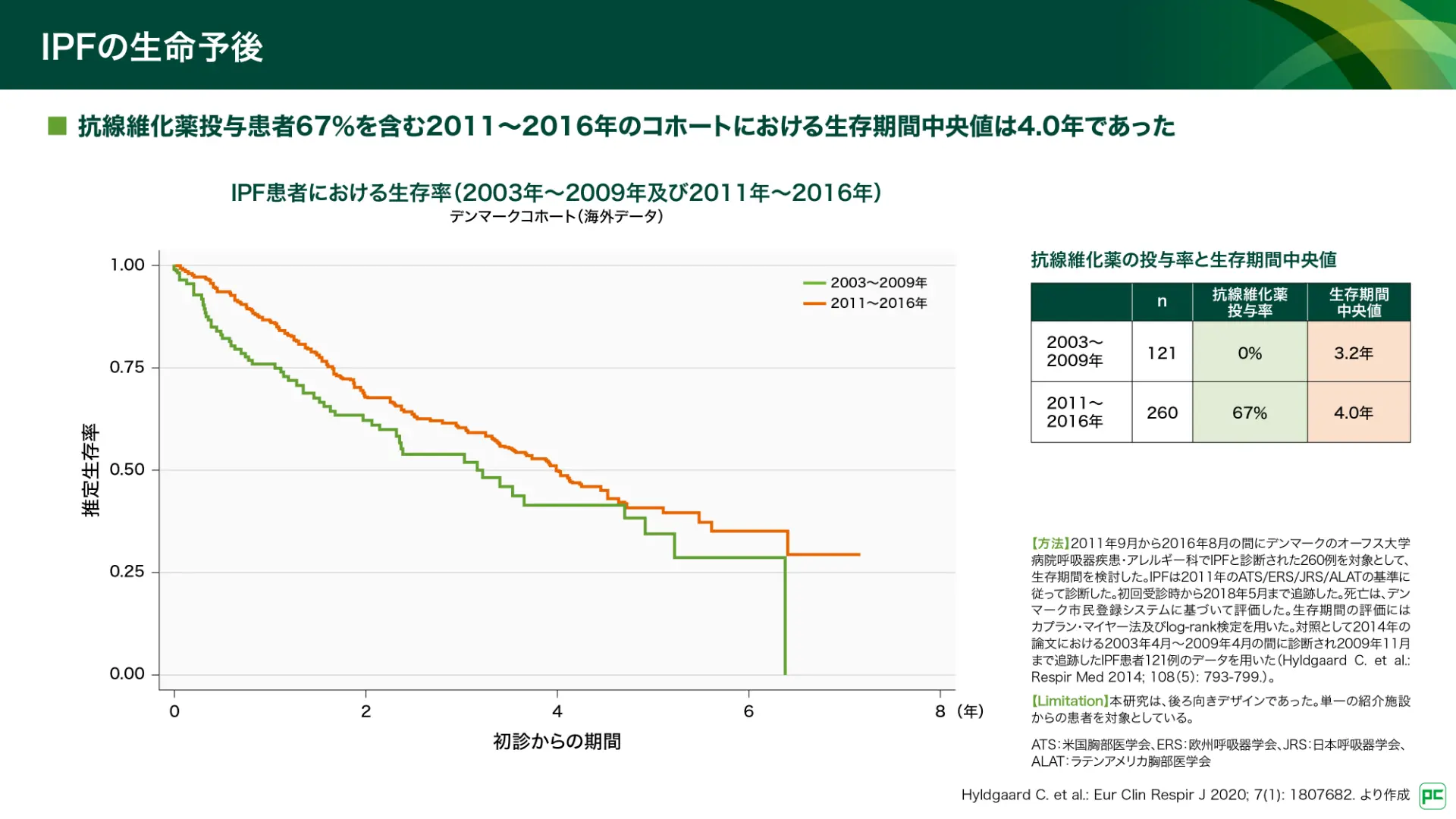
2011~2016年に診断されたIPF患者の追跡調査が報告されています(図6)6)。抗線維化薬による治療を行っていた患者67%を含む2011~2016年コホートにおける生存期間中央値は4.0年、一方、抗線維化薬の登場前の2003~2009年コホートでは3.2年でした。日本においても、2003~2007年に新規受理の特定疾病医療費受給者を対象とした北海道studyで、生存期間中央値は35.0ヵ月と報告されており7)、抗線維化薬登場前の予後は同様の結果でした。
図6
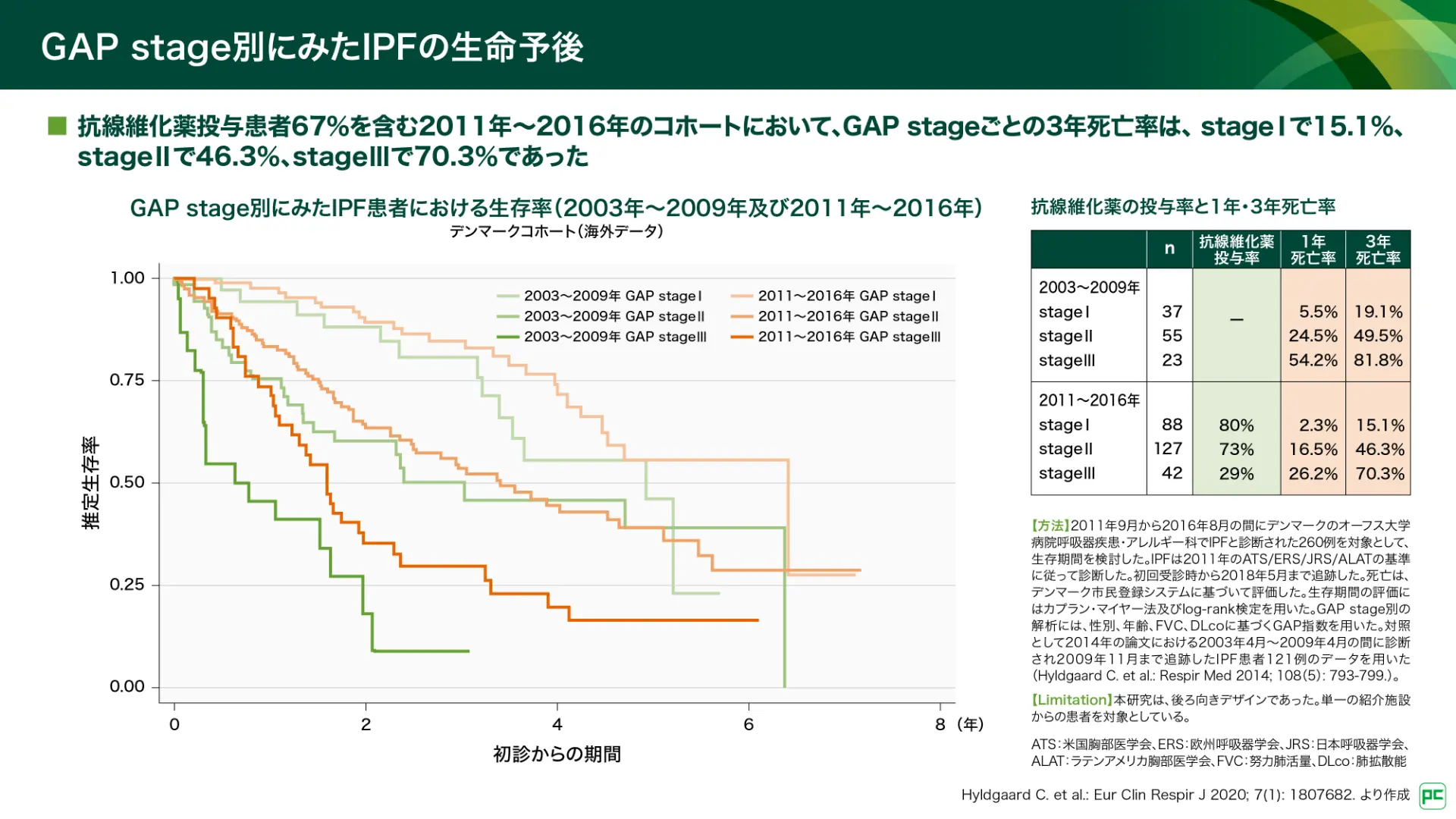
また、GAP stage別にみた生存率の解析では(図7)6)、抗線維化薬の投与率はstageIで80%、stageIIで73%、stageIIIで29%、3年死亡率はstageIで15.1%、stageIIで46.3%、stageIIIで70.3%でした。一方、抗線維化薬登場前の2003年~2009年コホートにおける3年死亡率はstageIで19.1%、stageIIで49.5%、stageIIIで81.8%でした。
図7
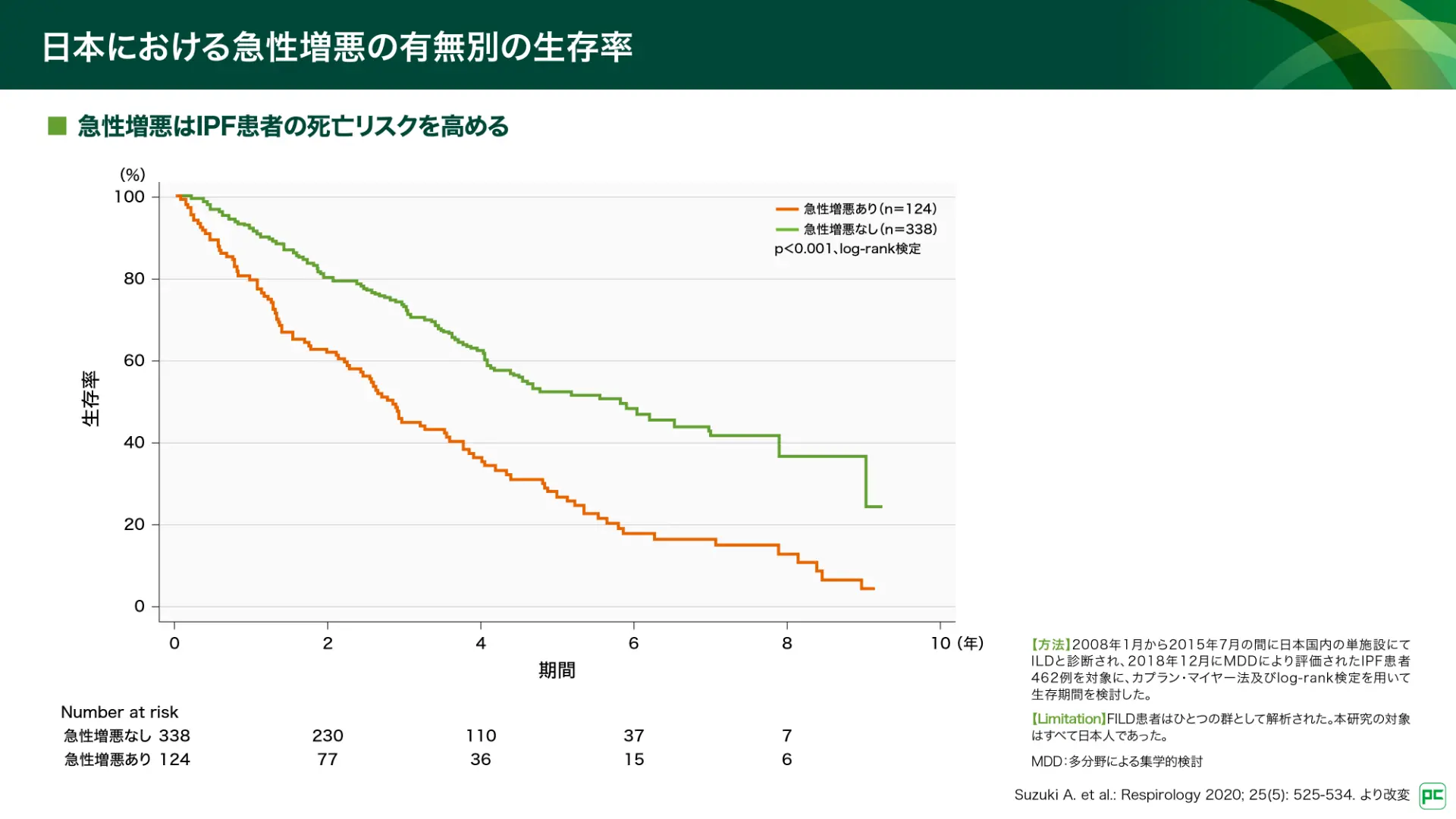
IPF患者さんの死亡原因の40%は急性増悪です7)。日本の患者さんにおける急性増悪の有無別にみた生存率では、急性増悪を発現すると、その後の生命予後が悪いことが示されています(図8)8)。
図8
このように、抗線維化薬による治療を行っているIPF患者さんにおいても予後不良であるのが現状です。また、IPFは、入院や医師の診察、年間の医療費コストなどの相当な医療資源の利用に関連していることも報告されており9)、早期に診断を行い、早期に治療を開始することが重要です。
IPFの診断の現状
IPF診断のフローチャートが特発性間質性肺炎 診断と治療の手引き 2022(改訂 第4版)に示されています(図9)1)。胸部X線写真の間質性陰影や聴診所見の捻髪音でILDが疑われたら、膠原病や過敏性肺炎、薬剤性肺障害などの鑑別を行います。HRCT所見がUIPパターンであり、明らかな原因がない場合は、外科的肺生検(SLB)や気管支鏡検査を行わなくとも、MDDを行ってIPFと診断可能です。probable UIPの場合は、IPFの臨床像に矛盾しない、又はIPF以外を想定する所見や経過がなければ多くの場合はIPFと診断可能です。indeterminate for UIP及びalternative diagnosisの場合は、初期のIPFや他疾患の可能性が十分考えられるので、気管支鏡検査(気管支肺胞洗浄、経気管支肺生検、経気管支クライオ肺生検)や外科的肺生検(SLB)を積極的に行いIPFの可能性を検討します。
図9
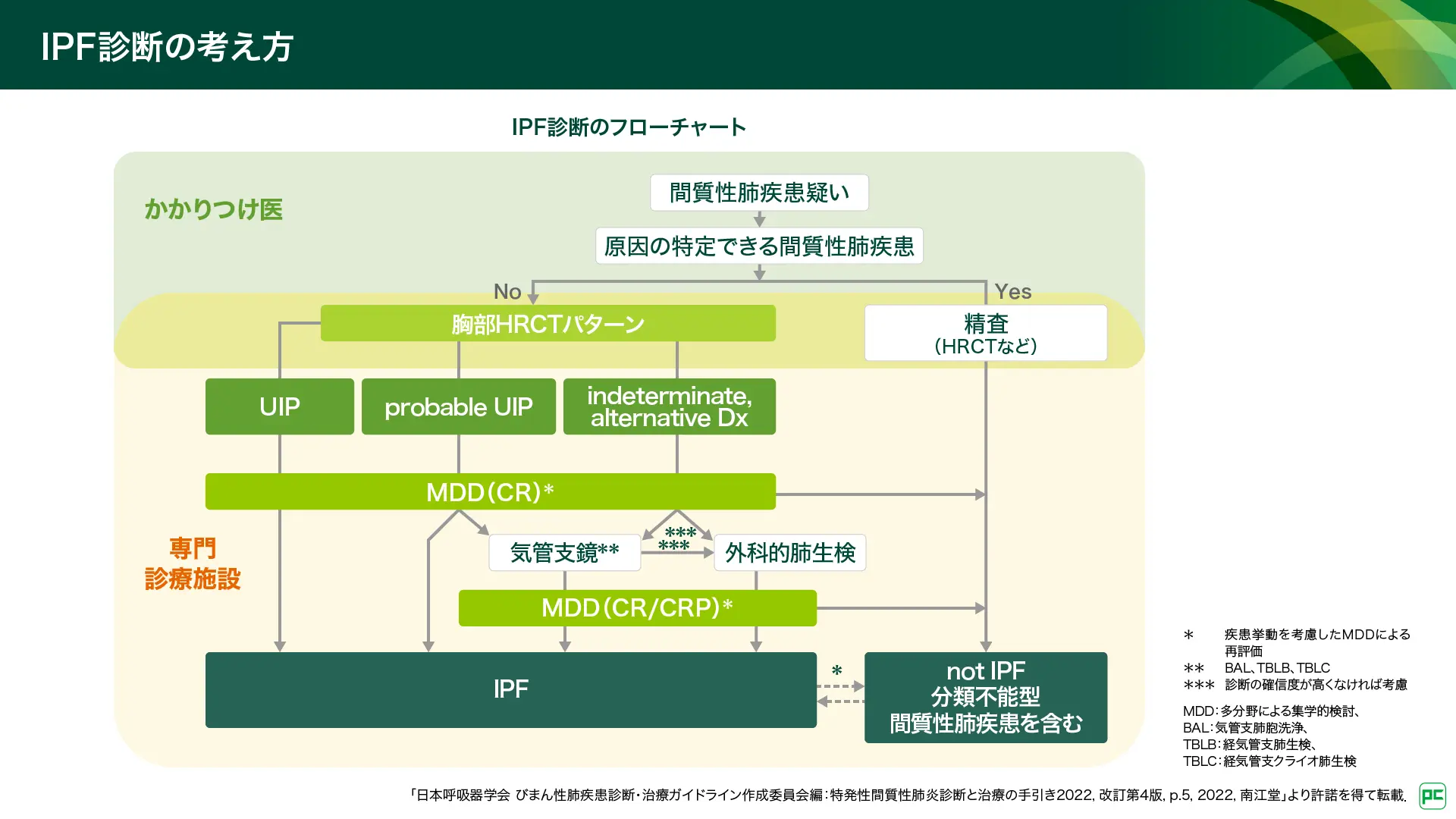
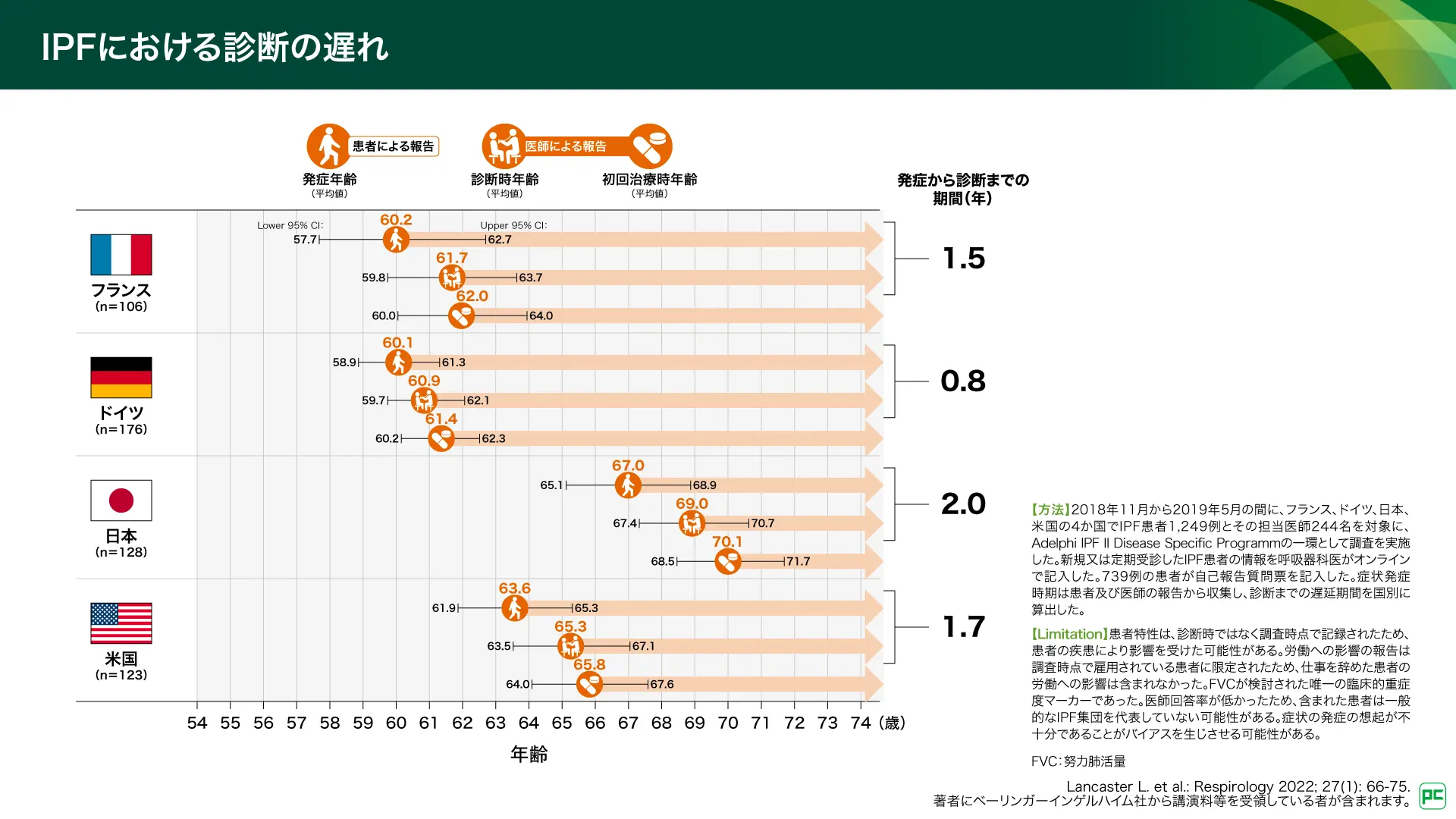
IPFの症状は多様で不均一であり、感染症やCOPD、喘息など同じ症状をもつ様々な疾患があることから、初期段階で誤診が起こりやすく、正確かつ迅速に診断することが課題となっています10,11)。日本を含む4ヵ国における診断及び治療までの期間に関する研究では、日本での発症から診断までの期間は2.0年と、フランス(1.5年)、ドイツ(0.8年)、米国(1.7年)と比べて長く、診断までに時間がかかっていることが示されています(図10)12)。また、本研究では早期IPF患者の最大45%が、COPDと誤診された可能性があることも示されています。2025年に報告された、国内の呼吸器内科医及び膠原病内科医を対象とした調査結果においても、発症から診断までの期間は21.2ヵ月とされており、同様の結果でした13)。
図10
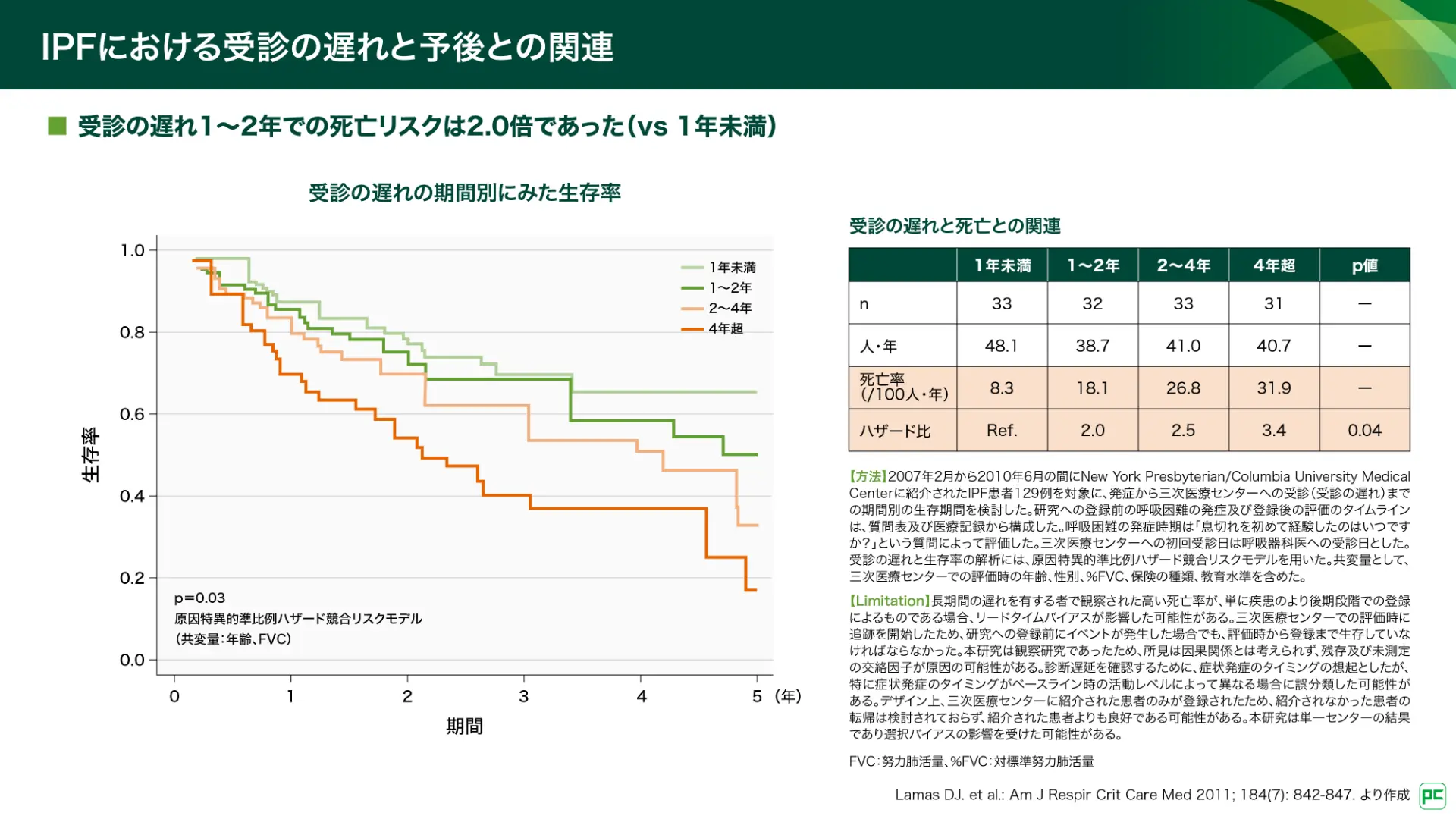
また、IPFの生命予後に対する受診の遅れの影響が報告されています(図11)14)。発症から三次医療センターへの受診までの期間が1~2年の患者では、1年未満の患者に対するハザード比が2.0であり、死亡リスクが上昇することが示されています。
図11
このように、IPFにおいては受診及び診断の遅れが生命予後に影響を与えるにもかかわらず、症状が多様で気づきにくいことから、診断までに時間がかかっていることが課題となっています。
ILDの治療の現状
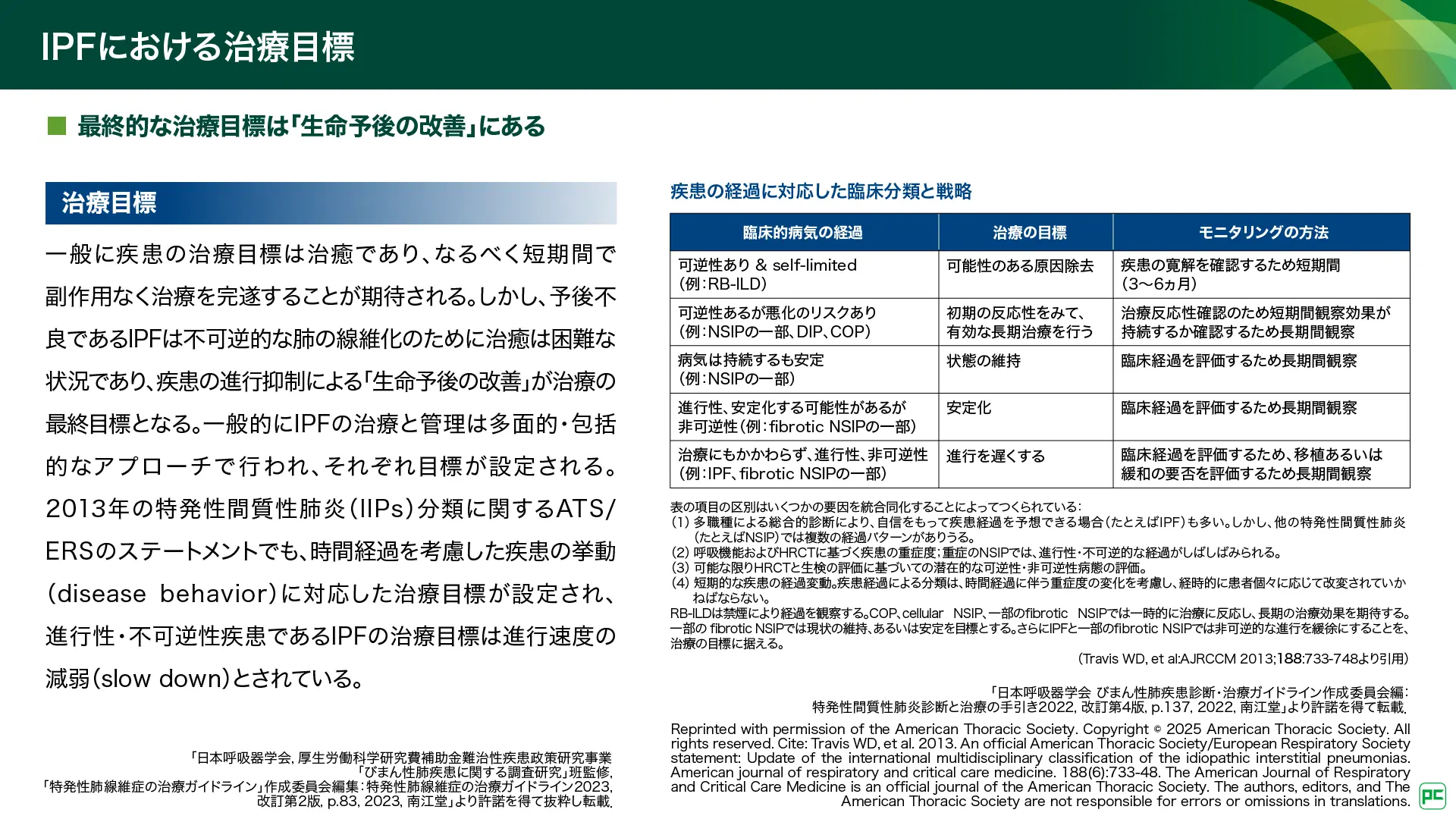
IPF治療の目標について、特発性肺線維症の治療ガイドライン2023(改訂第2版)15)では『予後不良であるIPFは不可逆的な肺の線維化のために治癒は困難な状況であり、疾患の進行抑制による「生命予後の改善」が治療の最終目標となる』とされています(図12)。これは、特発性間質性肺炎 診断と治療の手引き2022(改訂 第4版)1)においても同様です。また、疾患の経過に対応した臨床分類と戦略が示されており、IPFの治療目標は進行を遅くすることとされています。
図12
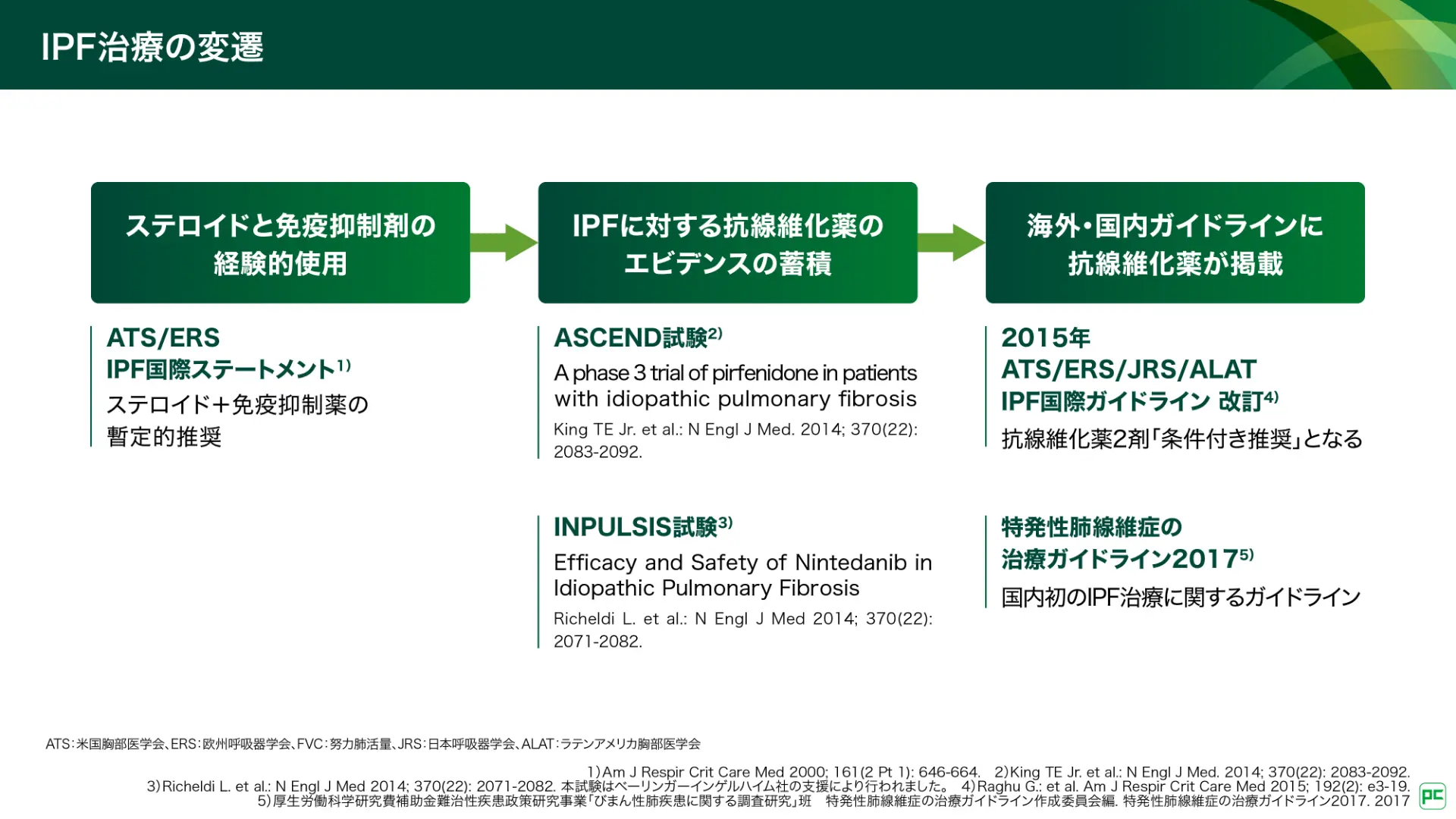
国内ガイドラインにおいて、慢性期のIPFに対して投与することを提案するとされている薬物療法は、抗線維化薬です15)。抗線維化薬登場前のIPF治療では、2000年の「ATS/ERS IPF国際ステートメント」において、ステロイドと免疫抑制薬の使用が暫定的に推奨されていました(図13)16)。しかし、経験に基づく推奨であり、エビデンスに基づく治療法が乏しい状況でした。その後ASCEND試験17)やINPULSIS試験18)などで、IPFに対する抗線維化薬のエビデンスが蓄積し、2015年の「ATS/ERS/JRS/ALAT IPF国際ガイドライン」19)では、抗線維化薬が「条件付き推奨」と記載されました。一方、ステロイドと免疫抑制薬については、PANTHER20) 試験などの臨床研究の結果が考慮され、これらの併用療法は「使用しないことを強く推奨」するとされました19)。
日本で実施されたリアルワールドデータの検討では、2019年時点で抗線維化薬による治療を受けていた患者は約50%でした21,22)。
図13
抗線維化薬治療における課題の1つとして、治療継続率が低いことが指摘されています。2014年10月~2019年7月の間の米国保険請求データを用いたIPF患者10,996例の研究では、抗線維化薬を投与されたIPF患者さんの42.8%が服薬を中止し、平均投与期間は約10ヵ月(302日)でした23)。その理由として副作用や高額な医療費、煩雑な手続きなどが挙げられています。抗線維化薬による治療時には、治療継続率を可能な限り高められるよう、適切な副作用マネジメントや医療費に関する情報提供等の患者さんサポートなどが重要です。
まとめ:IPFにおけるアンメットニーズ
IPFは、抗線維化薬登場後の現在でも未だ予後不良の疾患であり、早期診断・治療が求められています。診断の課題として、診断の遅れやMDD実施率の低さなどが、また、治療の課題として抗線維化薬の導入率の低さや治療中の服薬中止率の高さなどが指摘されています22)。
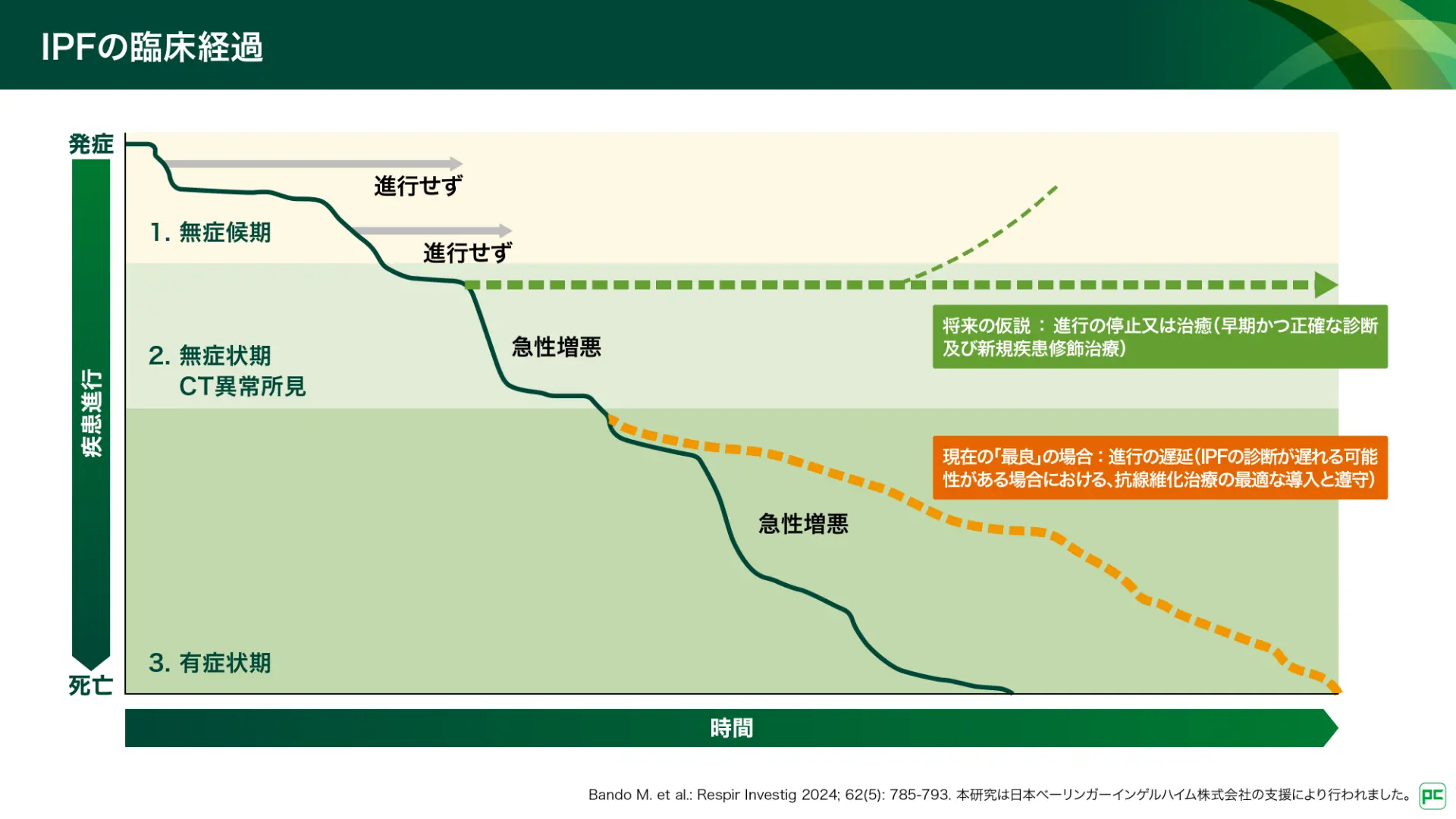
IPFは患者さんごとに多様な臨床経過をたどります(図14)22)。IPF治療においては、診断の遅れが生じる可能性のある中で、抗線維化治療の適切なタイミングでの導入と副作用マネジメントを通じて服薬遵守を促すことが重要です。国内のガイドライン及び手引きにおける治療の最終目標である「生命予後の改善」の実現に向け、今後は、早期かつ正確な診断や新規の疾患修飾治療の開発に基づき、進行の停止又は治癒が望める治療の確立が期待されます。
図14
2024年にはIPF治療においても「Feel(自覚症状)、Function(呼吸機能)、Survival(生存)」に重点をおいた検討が必要であることが提唱されています24)。今後のIPF診療においては、患者さん中心の評価に焦点をあて、最終的にQOLや生命予後を向上させるエビデンスの蓄積が期待されています。
図15

【参考文献】
- 日本呼吸器学会びまん性肺疾患診断・治療ガイドライン作成委員会編. 特発性間質性肺炎 診断と治療の手引き2022(改訂第4版). 2022
- 厚生労働省 令和6年(2024)人口動態統計月報年計(概数)の概況
- Kondoh Y. et al.: Respir Res 2022; 23(1): 24.
- Kim DS. et al.: Proc Am Thorac Soc 2006; 3(4): 285-292.
- du Bois RM.: Eur Respir Rev 2012; 21(124): 141-146. 本試験はベーリンガーインゲルハイム社の支援により行われました。
- Hyldgaard C. et al.: Eur Clin Respir J 2020; 7(1): 1807682.
- Natsuizaka M. et al.: Am J Respir Crit Care Med 2014; 190(7): 773-779.
- Suzuki A. et al.: Respirology 2020; 25: 525-534.
- Corral M. et al.: BMC Pulm Med 2020; 20(1): 188.
- Koudstaal T. et al.: Presse Med 2023; 52(3): 104166.
- Luppi F. et al.: Respir Res 2021; 22(1): 109.
- Lancaster L. et al.: Respirology 2022; 27(1): 66-75.
- Kaneko Y. et al.: Front Med (Lausanne) 2025; 12: 1526530.
- Lamas DJ. et al.: Am J Respir Crit Care Med 2011; 184(7): 842-847.
- 「特発性肺線維症の治療ガイドライン」作成委員会編. 特発性肺線維症の治療ガイドライン2023(改訂第2版). 2023
- Am J Respir Crit Care Med 2000; 161(2 Pt 1): 646-664.
- King TE Jr. et al.: N Engl J Med 2014; 370(22): 2083-2092.
- Richeldi L. et al.: N Engl J Med 2014; 370(22): 2071-2082. 本試験はべーリンガーインゲルハイム社の支援により行われました。
- Raghu G. et al.: Am J Respir Crit Care Med 2015; 192(2): e3-19.
- Idiopathic Pulmonary Fibrosis Clinical Research Network.: N Engl J Med 2012; 366(21): 1968-1977.
- Suda T. et al.: Respir Investig 2022; 60(6): 806-814.
- Bando M. et al.: Respir Investig 2024; 62(5): 785-793. 本研究は日本べーリンガーインゲルハイム株式会社の支援により行われました。
- Dempsey TM. et al.: Ann Am Thorac Soc 2021; 18(7): 1121-1128.
- Raghu G. et al.: Am J Respir Crit Care Med 2024; 209(6): 647-669.
その他の関連情報


特発性肺線維症および進行性肺線維症 国際診療ガイドライン2022(静止画)
日本ベーリンガーインゲルハイム
メディカルチャット 利用規約
当社の「日本ベーリンガーインゲルハイム メディカルチャット」(以下「本サービス」といいます)のご利用に際しては、本利用規約が適用されますので、必ず以下の記載事項をご確認下さい。
利用規約
- 本サービスは、当社所定のウェブページから文字によりお問い合わせいただくことにより、当社医薬品等に関する一般的な情報を、人工知能あるいは当社担当者により、文字及び図表により回答するサービスです(以下、人工知能による回答サービスを「AIチャット」、当社担当者による回答サービスを「有人チャット」といいます。)。ただし、AIチャットによる回答を原則とし、有人チャットは、AIチャットでの回答に対し、有人チャットでの回答も希望された場合に、提供させていただきます。
- 本サービスをご利用いただくことができるのは、当社医薬品等を扱いかつ国内に在住する医療関係者の方に限られます。当該医療関係者以外の方は、ご利用いただくことができません。
- 本利用規約に同意いただけない場合、本サービスを利用いただくことができません。本利用規約を最後までお読みいただき、「同意して利用する」ボタンを押した上で、本サービスをご利用下さい。
- 本サービスは、当社医薬品等に関する一般的なお問い合わせに対して回答するものとし、次の各号に掲げるお問い合わせについては、回答しないものとします。
- 当社医薬品等と関係のないお問い合わせ、または本サービスの回答範囲を逸脱したお問い合わせ
- 具体的な症状や治療方法に関するお問合せ
- 当社に適用される法令、ガイドラインまたは行政上の指導、当社自主規制その他当社が遵守すべきルールにより回答できないお問い合わせ
- 文字化け等により入力内容が判断できないお問い合わせ
- 前各号に掲げるほか、本サービスにより、適切な回答をすることができないと当社が判断した事項に関するお問い合わせ
- 本サービスは、日本語のみに対応しています。
- 本サービスは、当社医薬品の副作用、不具合及び有害事象の報告を受け付けていません。
- お問い合わせの内容によっては、本サービスでは十分に回答できない場合もございます。予めご了承下さい。
- 本サービスの利用可能時間は、以下のとおりです。
- AIチャット
24時間365日 - 有人チャット
平日9:00~17:00
- AIチャット
- 前項に関わらず、メンテナンス及び障害等のため一時的に本サービスを中断する場合がございます。
本サービスのご利用の際には、原則として、個人情報(お名前、ご住所、電話番号、メールアドレス等)を入力しないようお願いします。ただし、AIチャット及び有人チャットを問わず、当社医薬品の適用外使用に関するお問い合わせについては、コンプライアンス上の理由により、当社より、氏名及び施設名の入力を求める場合がございます。この場合には、当社プライバシーポリシーの内容を確認いただき、同意いただける場合に限り、入力して下さい(プライバシーポリシーについては「VIII 利用規約、プライバシーポリシー」に記載のURLからアクセス下さい)。その他の場合に、当社より個人情報の入力を求めることは一切ございません。
- 当社医薬品のご使用にあたっては、最新の添付文書等をご確認下さい。
- 当社は、本サービスまたは本サービスにより提供される情報の利用に際し生じた結果については、一切責任を負いません。
本サービスの利用にあたり、以下の各号の行為を禁止します。
- 本サービスにより提供される情報を複製、複写、転載、改変等する行為
- 第三者または当社の知的財産権その他の権利を侵害する行為
- 第三者または当社を誹謗中傷し、または名誉・信用を毀損する行為
- 本サービスの利用による営利目的の行為
- 本サービスの運営又は他の利用者による本サービスの利用の妨げとなる行為
- 前各号のほか、当社が不適当であると判断する行為
当社は、いつでも本サービスの提供を終了、またはその内容を変更することができるものとします。
本サービスの利用に関しては、以下の利用規約及びプライバシーポリシーが併せて適用されますので、ご確認下さい。



