
膠原病に伴う間質性肺疾患(CTD-ILD)診療の今とアンメットニーズ(静止画)
サイトへ公開:2026年03月30日 (月)
クイックリンク

膠原病に伴う間質性肺疾患(CTD-ILD)は、膠原病患者さんにおける死亡原因の上位を占める重要な疾患です。全てのCTD-ILD患者さんで治療を必要とするわけではありませんが、進行性肺線維症(PPF)を呈する場合は特に生命予後が悪く、進行を見極めて適切なタイミングでの治療が必要となります1)。
ここでは、CTD-ILDの疫学と疾患負荷、PPFを呈する患者さんにおける生命予後、PPFの診断と治療の今をレビューし、今なお残るアンメットニーズについて解説します。
膠原病患者さんにおける間質性肺疾患(ILD)の疫学と疾患負荷
膠原病患者においてILDを伴う患者さんの割合は疾患ごとに多様です。2023年のシステマティック・レビューでは、関節リウマチ(RA)で11%、特発性炎症性筋疾患(IIM)で41%、全身性硬化症(SSc)で47%などと推定されています2)(図1)。
図1
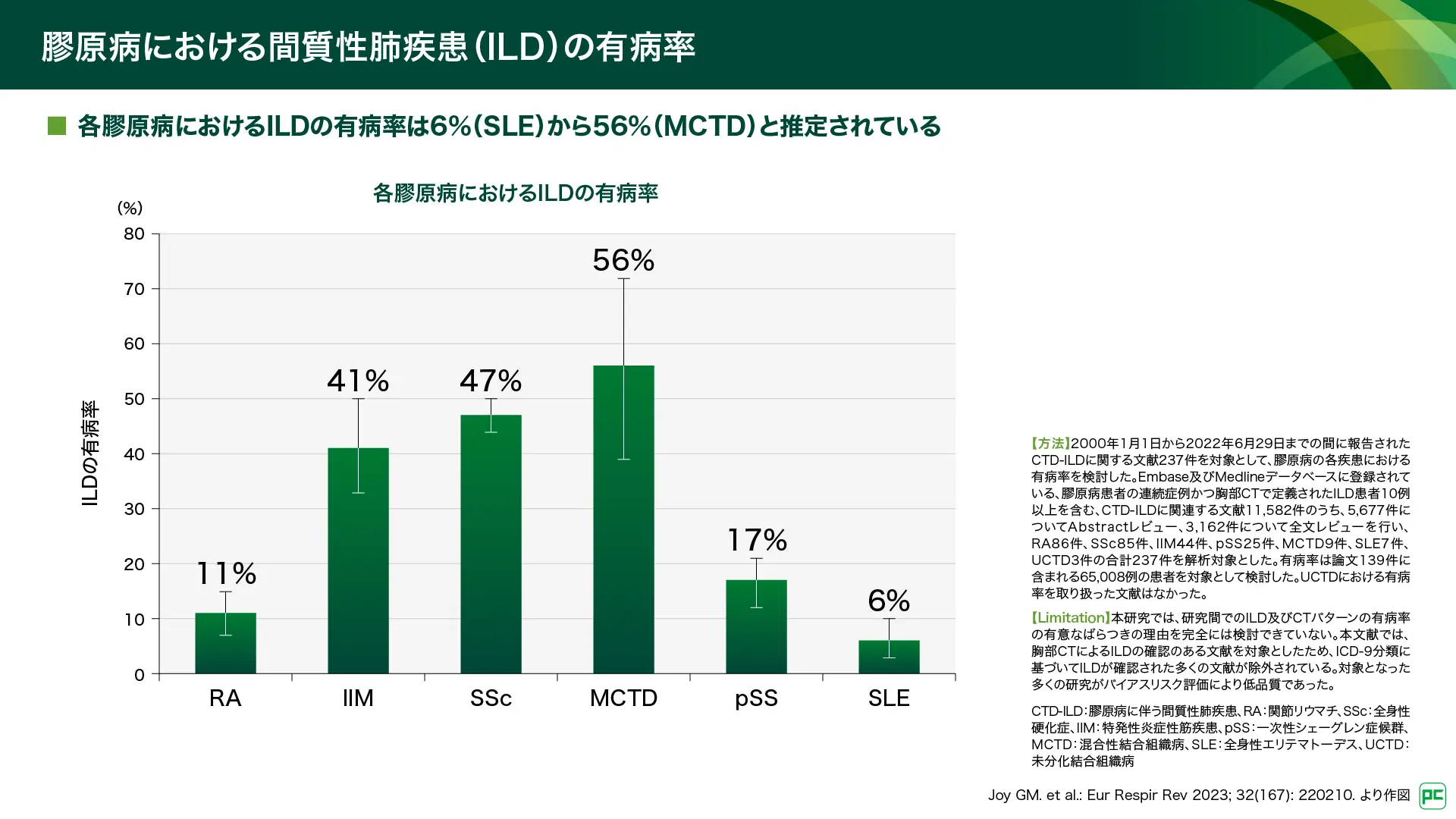
主な症状は咳嗽、呼吸困難、及びそれに伴う疲労感です(図2)。これらの症状は、入院や死亡などの健康への直接的な影響に加え、身体・社会的活動の制限や失職などの身体機能的影響、うつ病や自立性の喪失、恐怖感などの感情的な影響を引き起こし、患者さんの生活に多岐にわたる変化をもたらします。また、2024年の人口動態統計によると、日本人男性において、特発性間質性肺炎(IIPs)を含むILD全体による死亡者数は16,021人であり、死因の第10位を占めています3)。新規に診断されたILD患者さんの約30%はCTD-ILDであったとの報告もあり4)、社会的にもその対応が重要な課題となっています。
図2
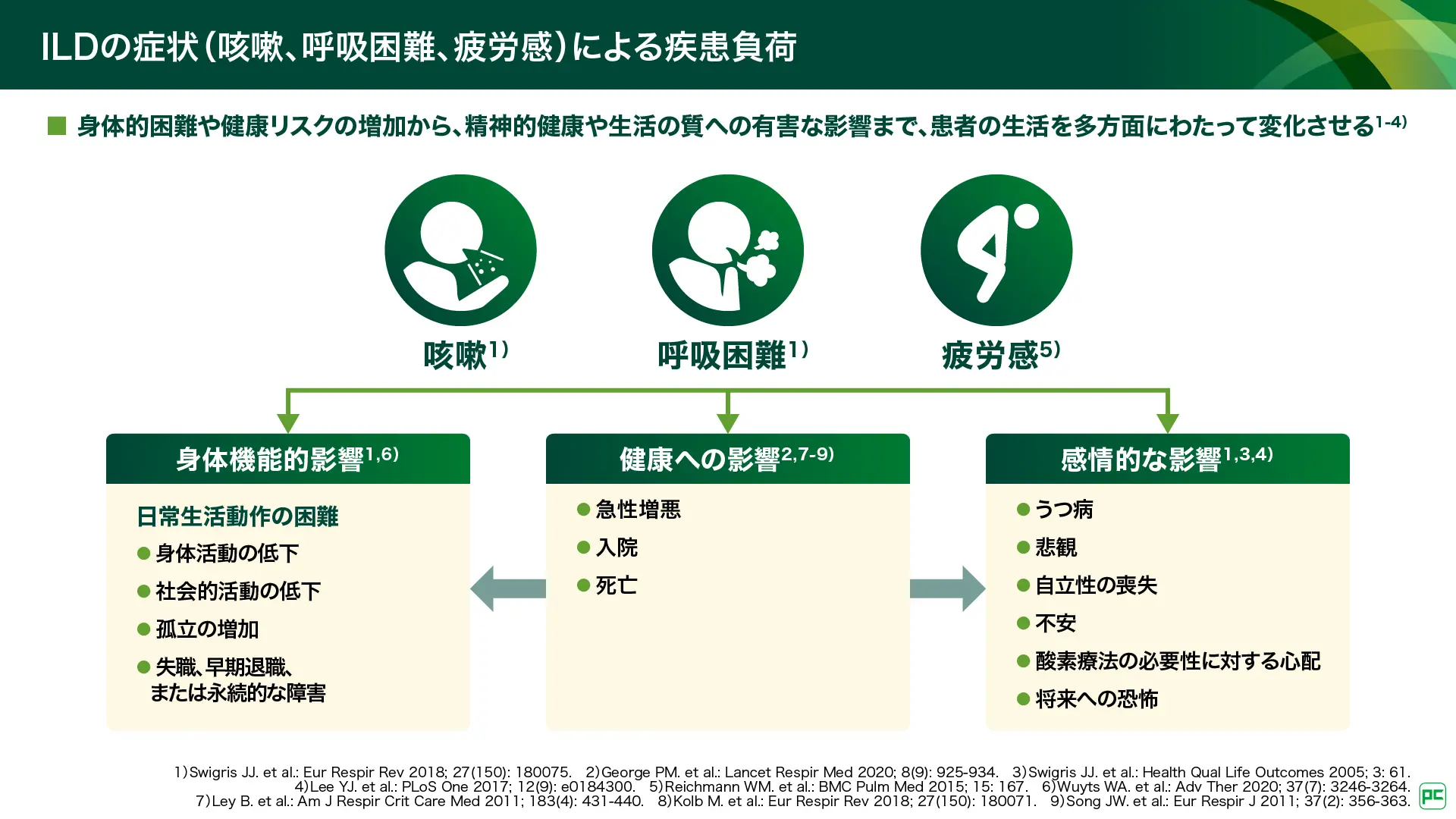
ILDは膠原病患者さんの生命予後に影響することが報告されています。デンマークの全国レジストリにおける死亡率の検討では、RA-ILDの生存期間中央値は6.6年、ILDを伴わないRAでは10年以上でした(図3)5)。1年死亡率はRA-ILDで13.9%及びRAで3.8%、5年死亡率はRA-ILDで39.0%及びRAで18.2%でした。ノルウェーのNor-SScコホートにおける検討では、HRCTで線維化所見のあるSScの生命予後は線維化所見のないSScと比べて不良でした(p<0.001、log-rank検定)(図3)6)。
図3
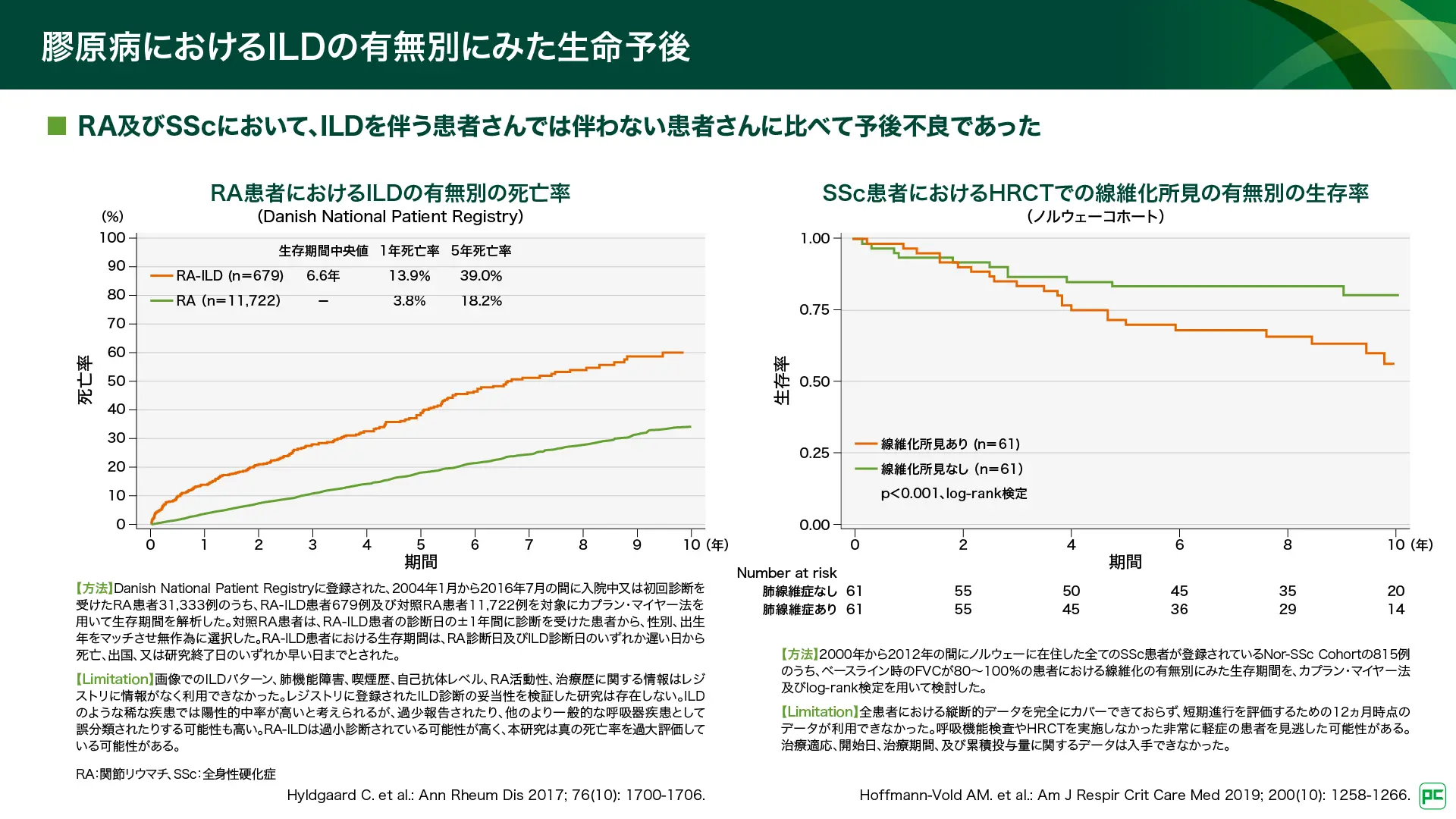
このようにILDは、膠原病に伴う様々な呼吸器疾患の中でも、頻度が高く、生命予後への影響が最も大きい疾患です1)。
CTD-ILDの病態形成及び線維化の進展プロセス
CTD-ILDの病態形成メカニズムはまだ十分に明らかにされていないものの、炎症と線維化が早期から相互に作用して進行すると考えられています(図4)。
図4
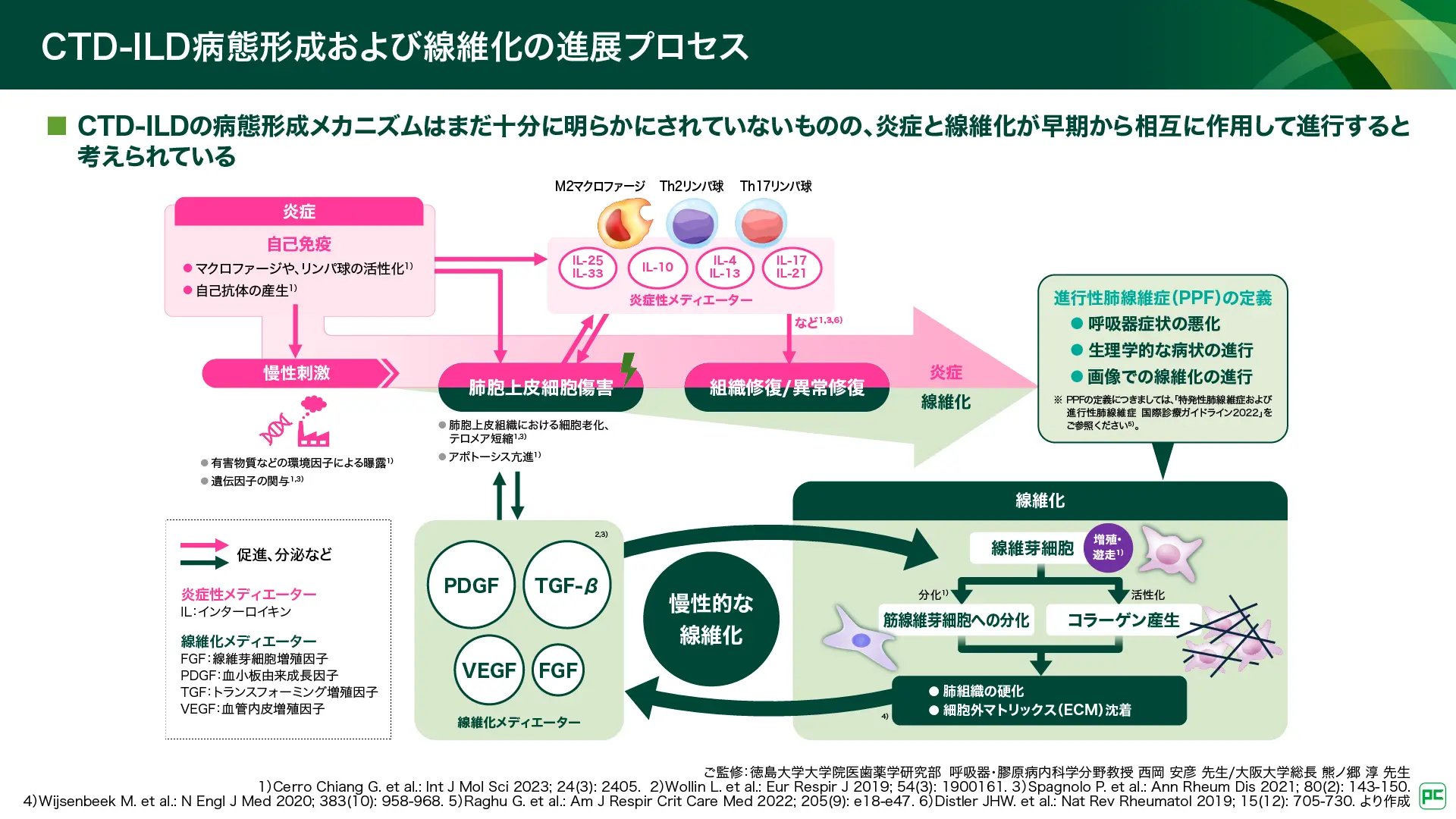
膠原病の病態形成には、マクロファージやリンパ球の活性化、自己抗体の産生など、自己免疫反応による炎症が関わっており、肺組織においても免疫が亢進しています7)。肺胞上皮細胞は、膠原病と関連する免疫反応や環境因子の曝露などによって、慢性的に刺激を受けています7,8)。
肺胞上皮細胞が傷害されると、組織修復プロセスが開始され、「炎症性メディエーター」と「線維化メディエーター」が働きます。肺胞上皮細胞やM2マクロファージ、Th2リンパ球、Th17リンパ球からは、IL-25やIL-33、IL-10などの「炎症性メディエーター」が分泌され9)、肺胞上皮細胞の炎症応答を惹起します10)。また、マクロファージや上皮細胞などからは、PDGFやTGF-β、VEGF、FGFなどの「線維化メディエーター」が分泌され11)、線維芽細胞の増殖や遊走を促進し12,13)、筋線維芽細胞への形質転換を引き起こします7)。従来、コラーゲンは筋線維芽細胞から産生されると考えられていましたが、近年では活性化された線維芽細胞からの産生を示唆する報告もあります14)。筋線維芽細胞や活性化線維芽細胞からのコラーゲン産生により14)、細胞外マトリックス(ECM)の沈着、肺組織の硬化が引き起こされます15)。
肺組織の硬化は、さらに線維化メディエーターの放出を引き起こし、その結果、線維芽細胞の活性化や筋線維芽細胞への形質転換が増強され、肺組織のさらなる硬化が生じます。このような一連のプロセスにより、線維化が継続的に進行していくループが形成され12)、慢性的な線維化の進行につながります。
これらの知見は、肺胞上皮細胞が傷害される時点から線維化のメカニズムがすでに始まっていることを示唆しています。そのため、原疾患に対して、免疫抑制剤などの抗炎症薬による治療中であっても、ILDの発症早期から定期的にモニタリングを行い、線維化の進行を見逃さないことが重要です。
進行性肺線維症(PPF)を呈する患者割合
慢性経過で線維化が進行する症例は様々なILDでみられ、PPFという概念が提唱されています。PPFにおける背景疾患の病因は異なるものの、共通する病態の存在が推測されています1)。従来は、「PF-ILD」や「progressive, non-IPF lung fibrosis」などの用語があり、臨床試験でも様々な基準が用いられてきましたが、現在では慢性経過で線維化が進行する疾患挙動を呈するILDを包括する用語としてPPFが受け入れられています(図5)16)。
図5

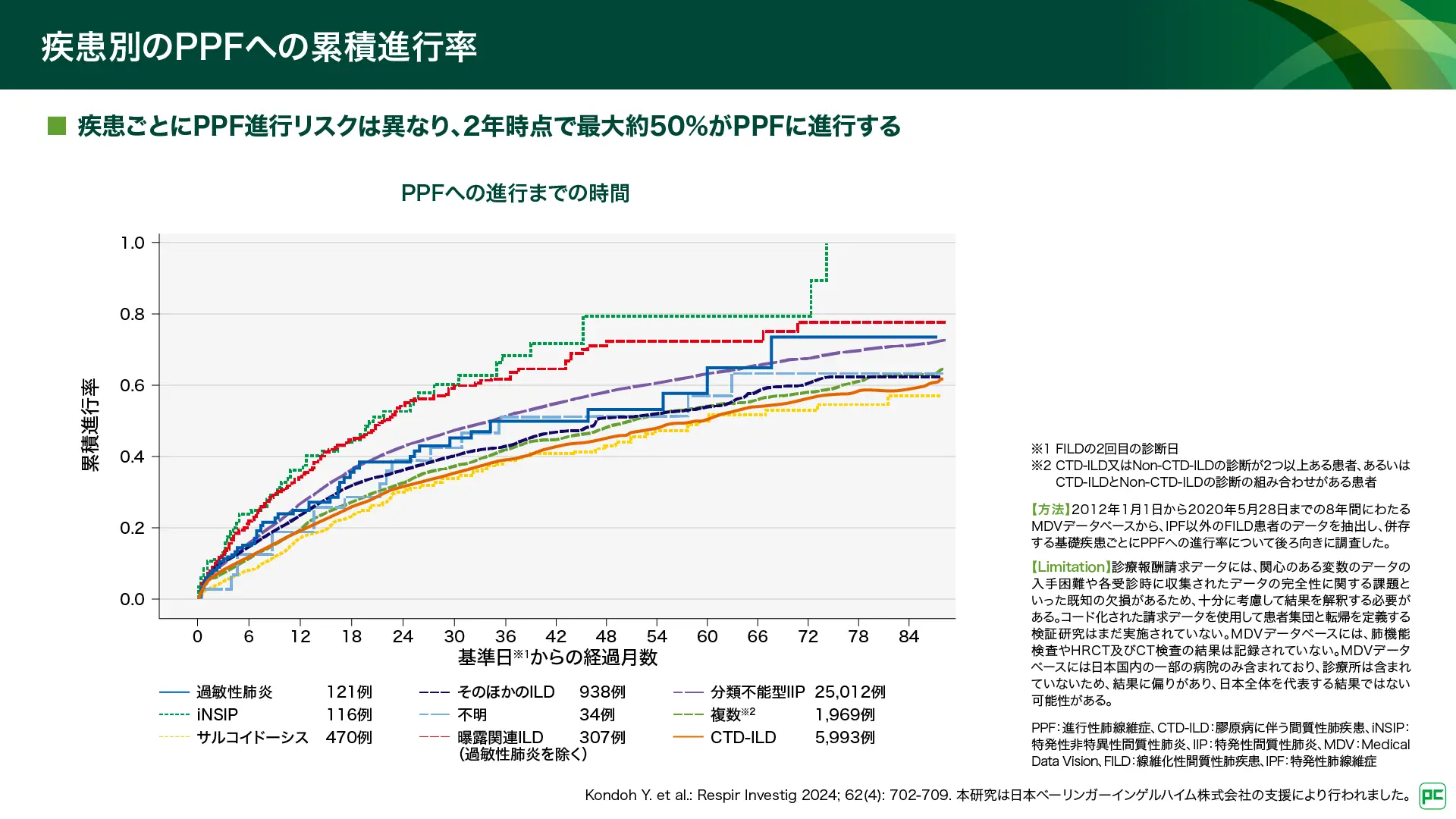
各疾患の中でPPFを呈する割合は、疾患ごとに多様であると考えられており(図6)17)、CTD-ILDの最大40~50%がPPFを呈すると推定されています18)。また、CTD-ILD患者5,993例を含む、日本の2012~2020年の診療報酬請求データを用いたPPFへの進行リスクに関する検討が報告されています(図7)19)。24ヵ月時点のPPFへの進行の推定発生率は、RA-ILDで26.2%、SSc-ILDで28.4%、多発性筋炎/皮膚筋炎に伴う間質性肺疾患(PM/DM-ILD)で34.9%とされ、CTD-ILD全体では31.3%でした。疾患ごとにPPFへの進行リスクは異なり、2年時点で最大約50%がPPFに進行することが示されています。
図6

図7
PPFの生命予後と急性増悪
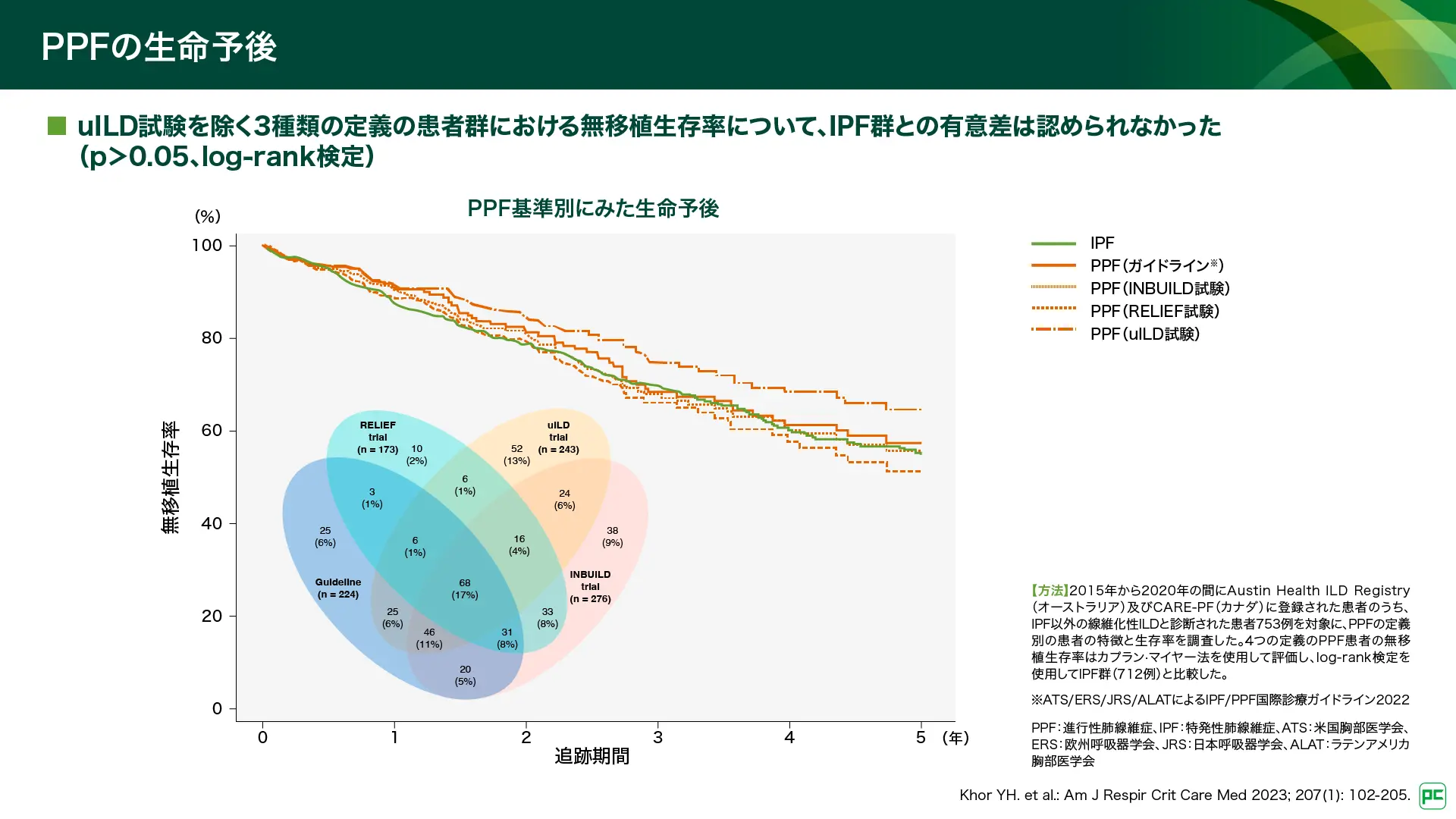
PPFの生命予後について、オーストラリア及びカナダのレジストリを用いた検討が報告されています(図8)20)。2022年IPF/PPF国際診療ガイドライン、INBUILD試験、RELIEF試験の基準で定義したPPFの生存率は、5年生存率20~40%21)とされている特発性肺線維症(IPF)と有意差はなく、予後不良であることが示されています。
図8
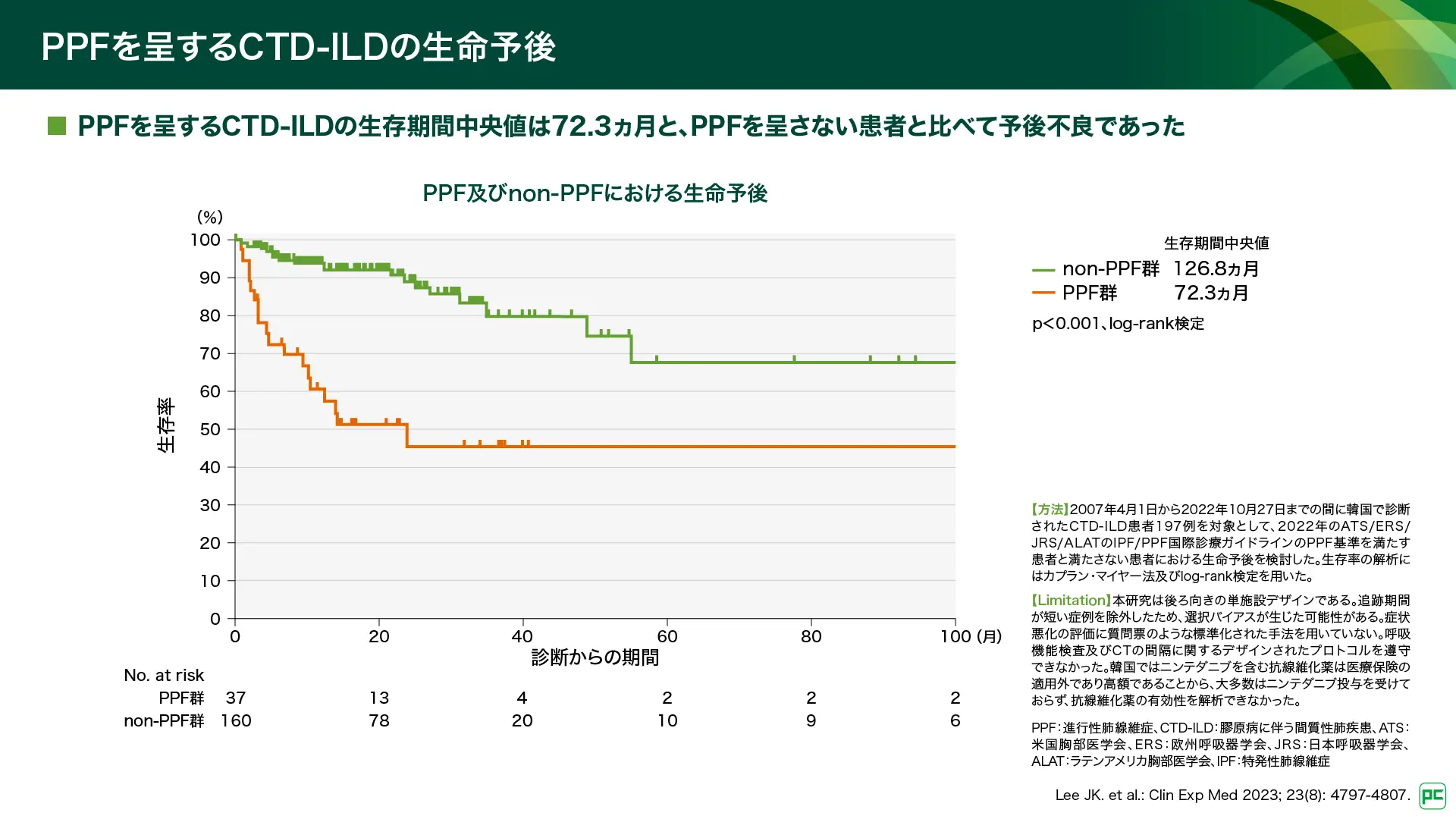
アジア人のCTD-ILDにおける生存率の検討では、PPFを呈するCTD-ILDの生存期間中央値は72.3ヵ月であり、PPFを呈さないCTD-ILD(126.8ヵ月)と比べて予後不良であることが示されています(p<0.001、log-rank検定)(図9)22)。この結果は、RA-ILD及び炎症性筋疾患においても同様でした(p=0.001及びp=0.003、log-rank検定)。また、CTD-ILDのうち、経過中に%FVCが10%以上低下する群では、5年生存率が50%未満であったと報告されています1,23)。
図9
急性増悪は、慢性経過をたどるILDが通常1ヵ月以内の間に急激に悪化する病態で、生命予後に大きく関わります1)。ILDの急性増悪は、2013年に本邦からIPFでの発現が報告されましたが1,24)、その後、CTD-ILDをはじめその他のILDでも発現することが報告されています1,25)。
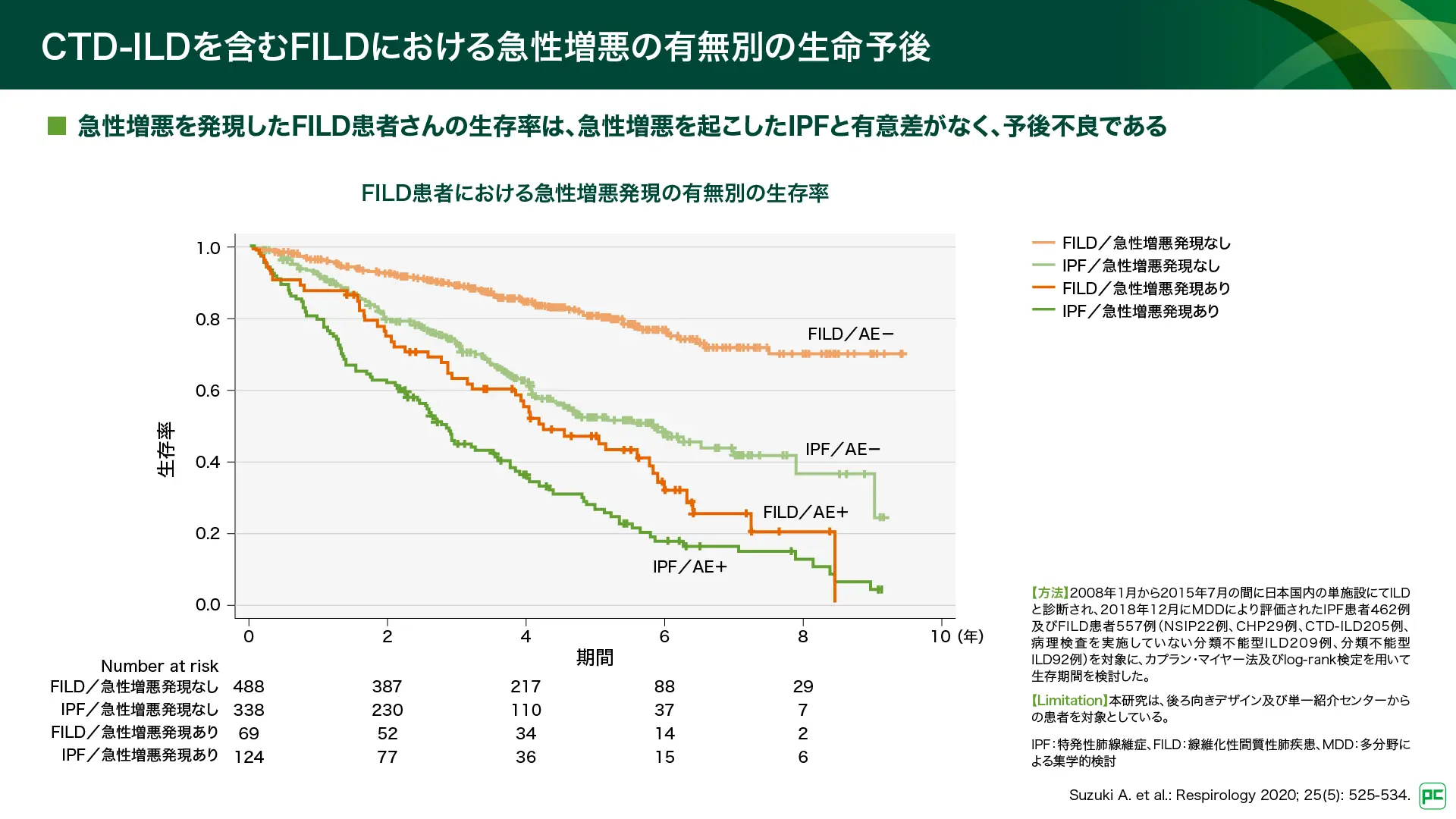
急性増悪の発現頻度に関する大規模データの研究はありませんが、日本における205例のCTD-ILDの報告では年間3.19%であったと報告されています1,26)。また、RA-ILDでは年間2.6~11.1%1,27)、炎症性筋炎では12年間の後向き研究で13.3%1,28)、SSc-ILDでは24年間の観察期間で19.6%1,29)との報告があります。日本における急性増悪の有無別にみた生存率の検討では、急性増悪を発現したCTD-ILDを含むFILDの生命予後は、IPFと有意差がなく、予後不良であることが示されています(図10)26)。
図10
このように、PPFを呈するCTD-ILD患者さんの生命予後はIPFと同様であるという報告もあります。そのため、進行する患者さんを見極めて適切に対応することが重要となります。
PPFを伴うCTD-ILDの診断の現状
CTD-ILDは症状の現れ方や進行パターンが多様であり、感染症やCOPD、喘息などの同じ症状をもつ様々な疾患があることから、正確かつ迅速に診断することが課題となっています(図11)30)。
図11

PPF患者さんを対象とした、発症から診断・死亡までのペイシェント・ジャーニーの調査が報告されています(図12)31)。発症からILD診断までの期間はRA-ILDで11.5ヵ月、SSc-ILDで9.3ヵ月、他のCTD-ILDで11.0ヵ月でした。日本における検討でも、CTD-ILD全体における発症から診断までの期間は14.3ヵ月とされており、同様の結果でした32)。また、ILDと診断された後、PPFの発現から医師によるPPFの認識までの期間は、RA-ILDで11.0ヵ月、SSc-ILDで9.6ヵ月、他のCTD-ILDで11.2ヵ月でした(図12)31)。
図12
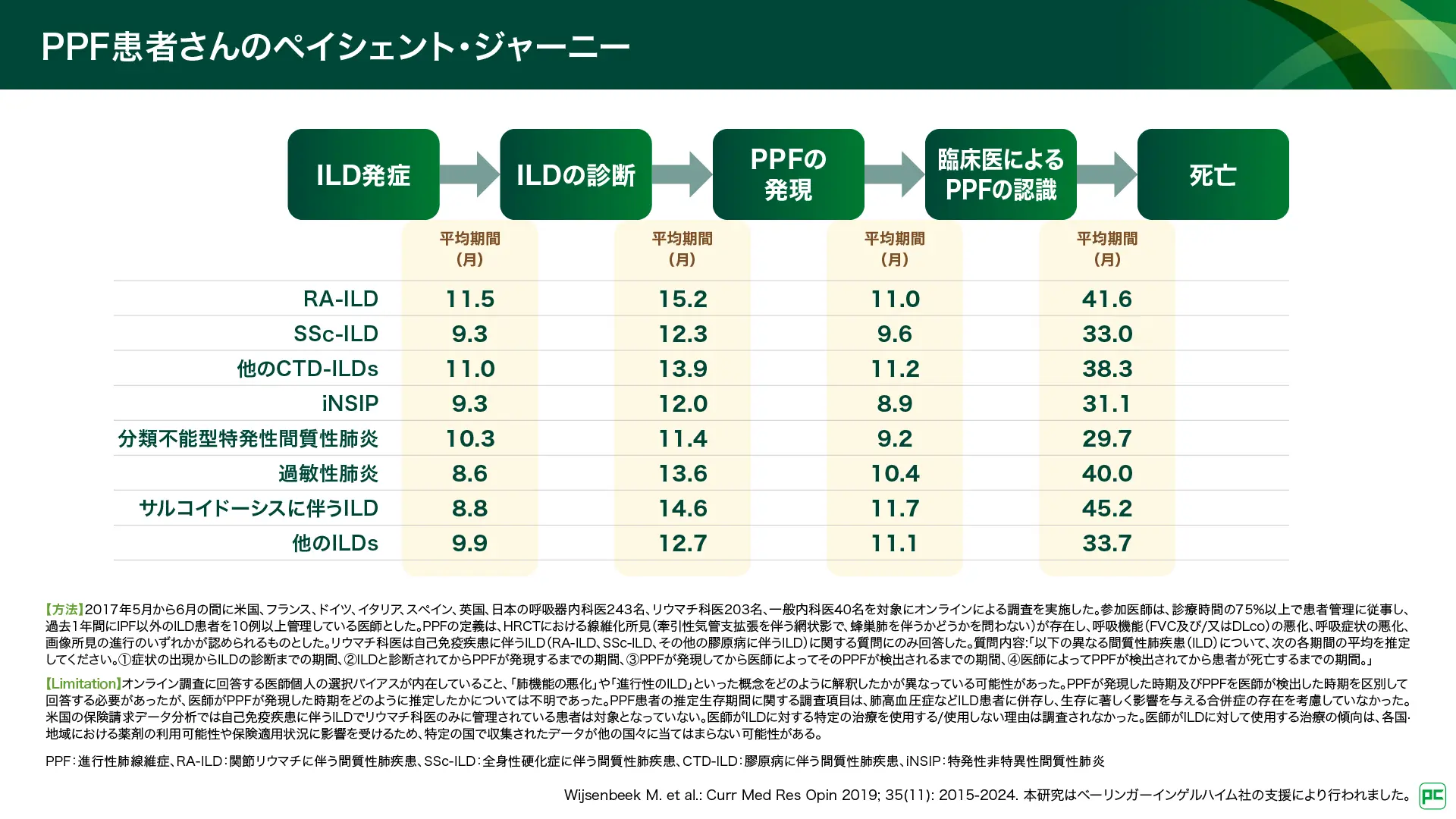
PPFはCTD-ILD患者さんの生命予後に影響を与えるにもかかわらず、ILDの発症から診断、及びILD診断からPPFの認識までに時間を要していることが指摘されています31,32)。2025年9月にアップデートされた間質性肺疾患の国際多分野合意分類33)では、CTD-ILDを含む二次性間質性肺炎も対象に含まれ、ILDに対する包括的な分類に変更されました。CTD-ILDにおいても、画像・病理パターンを「UIP」、「NSIP」などと正確に把握し、放射線科医・病理医・呼吸器内科医とより緊密に連携し、品質の高いMDDを実施することで、より正確かつ早期からの診断につなげることが期待されています。
PPFを伴うCTD-ILDの治療の現状
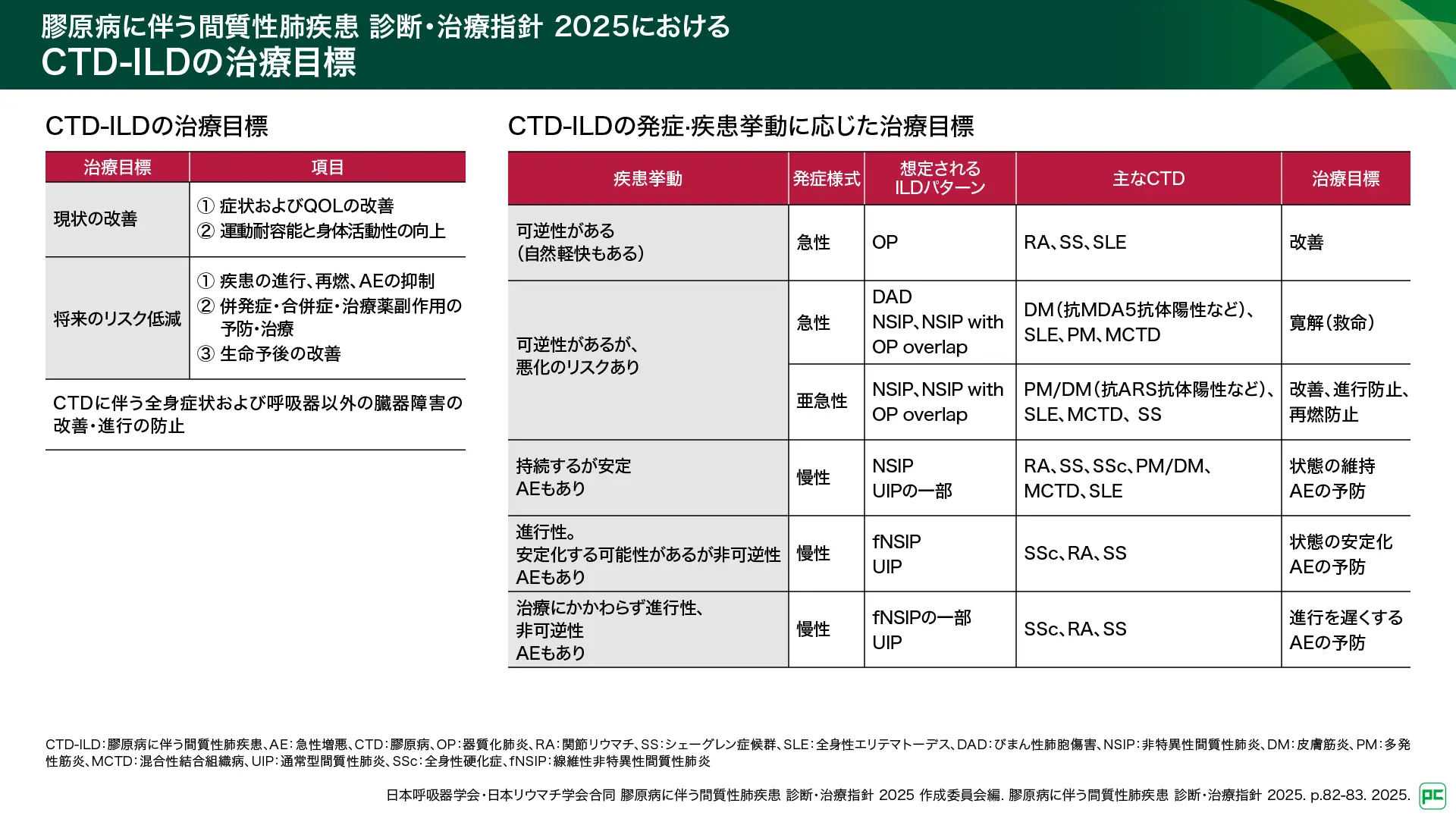
CTD-ILDの治療目標について、膠原病に伴う間質性肺疾患 診断・治療指針 20251)では、「症状を改善させるのみではなく、生命予後を改善させ、かつ社会生活を含めた生活の質を改善させること」と示されています(図13)。また、進行が急速なもの(炎症が主体)と慢性のもの(線維化が関与)とで治療目標が異なることから、疾患の発症様式・臨床経過に応じた治療目標も示されています(図13)。2025年9月に発表された「ERS/EULAR CTD-ILD診療ガイドライン」においても、治療に関する考慮事項として、「疾患進行を予防し、症状、生活の質、生存を改善するために重要である」と記載され、CTD-ILDにおける基本的な考え方は同様です34)。
図13
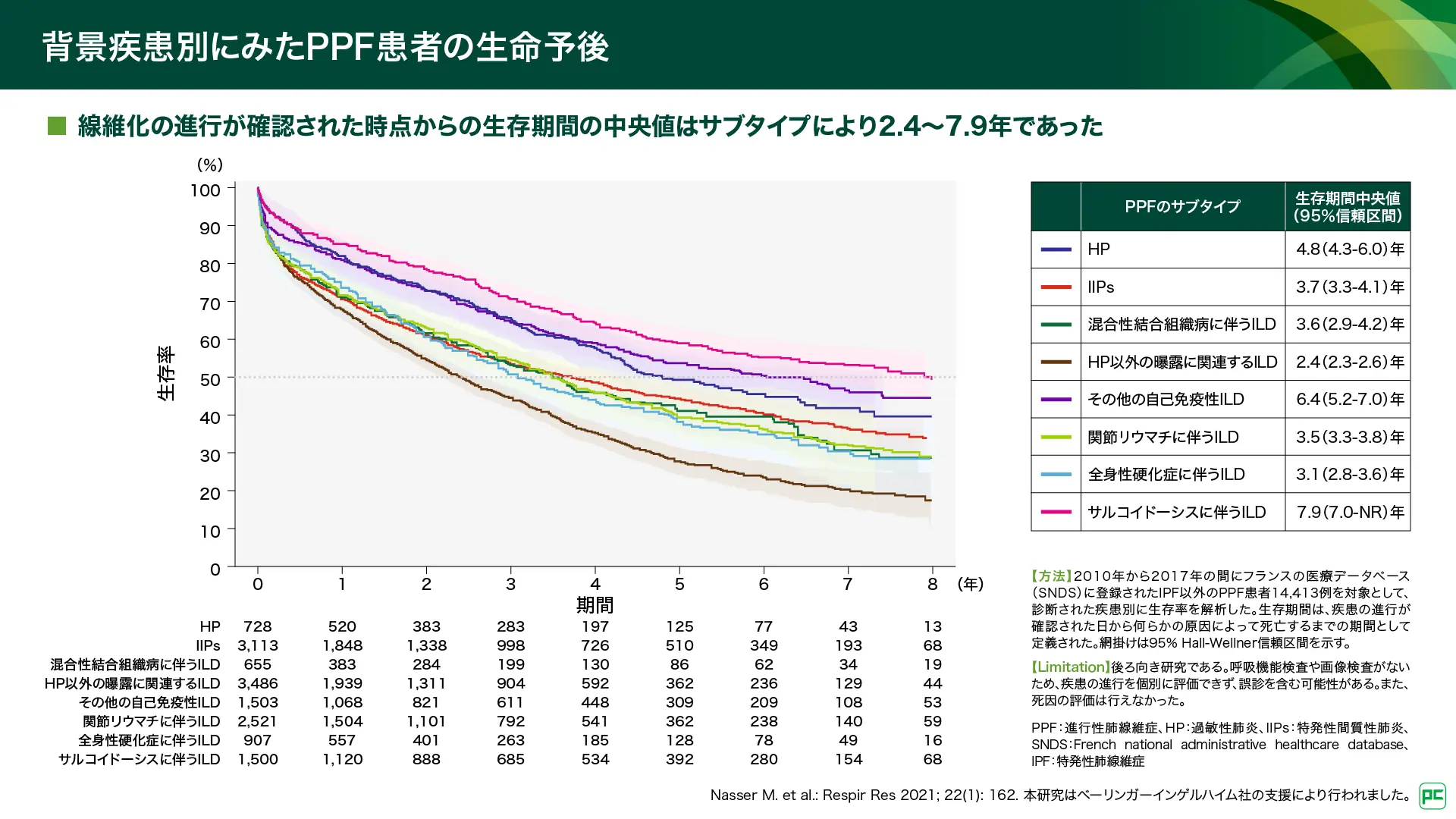
2010年から2017年の間にフランスの医療データベース(SNDS)に登録されたPPF患者14,413例を対象とした生存率の検討が報告されています35)。生存期間中央値は、RA-ILDで3.5年、SSc-ILDで3.1年、MCTD-ILDで3.6年、その他の自己免疫性ILDで6.4年などでした(図14)。
図14
また、1年生存率及び3年生存率は、RA-ILDでは72.4%及び54.6%、SSc-ILDでは73.6%及び51.2%でした(図15)35)。5年生存率はRA-ILD及びSSc-ILDとも50%以下でした(39.8%及び38.8%)。本研究の対象患者さんはフォローアップ期間中に標準的な治療を受けており、その内訳はグルココルチコイド68.5%、ミコフェノール酸モフェチル又はミコフェノール酸7.0%、アザチオプリン6.7%などでした。また、抗線維化薬は1.6%でした。
図15
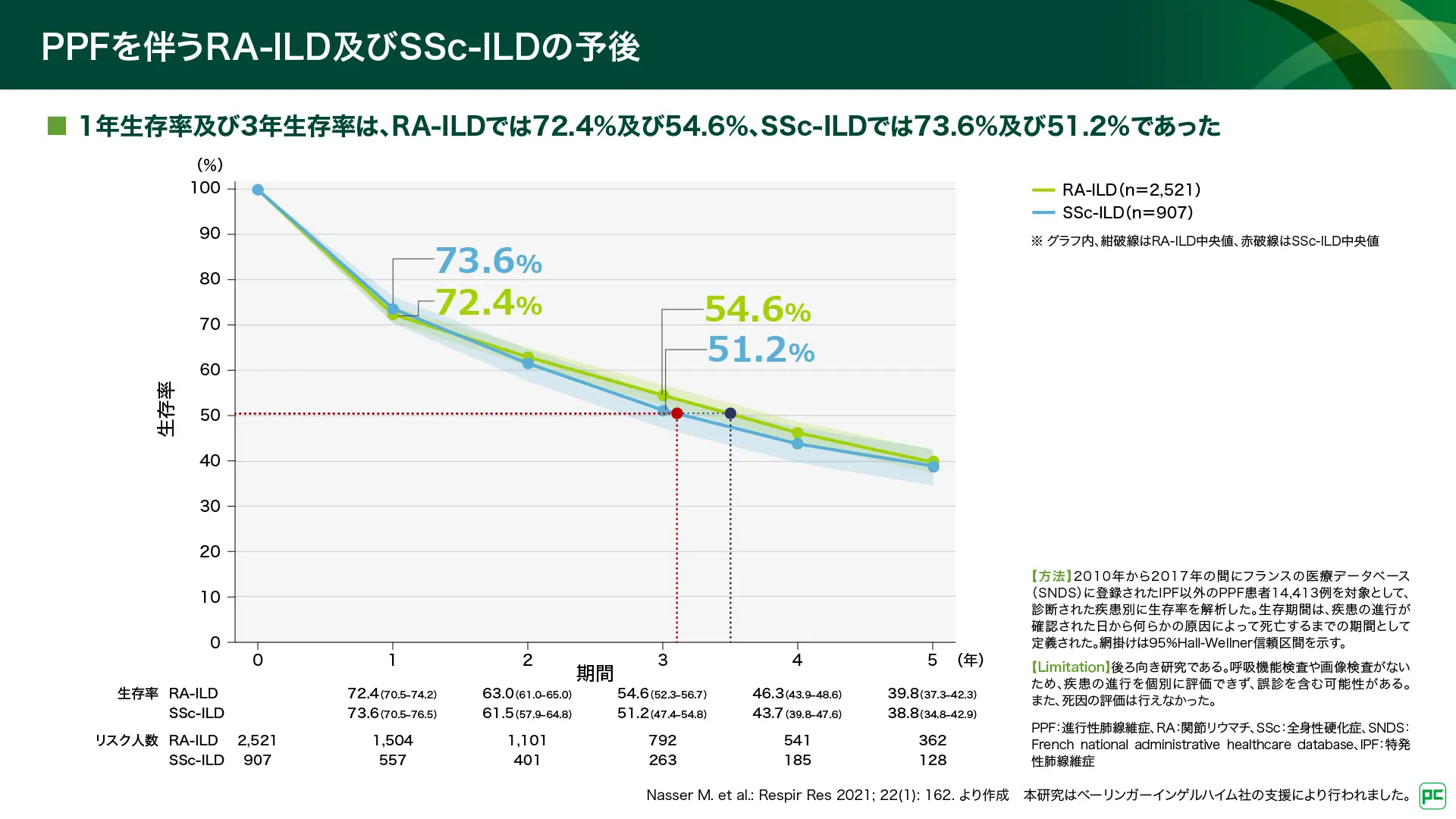
このようにPPFでは、生命予後の改善が治療目標となっていますが、2010年から2017年時点での標準的な治療を受けている患者さんにおいても、予後不良であることが示されています。
まとめ:PPFにおけるアンメットニーズ
CTD-ILDは、膠原病患者さんの生活を多岐にわたって変化させQOLの低下を引き起こします。また、死亡原因の上位を占め、生命予後に関わる重要な疾患であり、治療における最終目標は生命予後の改善とされています1)。
CTD-ILDの最大40~50%の患者さんが予後不良のPPFを呈すると報告されており、早期診断と適切な治療介入が重要です18)。診断・モニタリングにおける課題として、ILDの発症から診断、ILD診断からPPFの認識までに時間を要することが指摘されています31)。また、標準治療を受けている患者さんの5年生存率が50%以下35)であることは、未だアンメットニーズがあることを示しています。
PPFを伴うCTD-ILD患者さんの診療においては、早期かつ正確にILDを診断し、PPFを呈する患者さんを見極めて、適切なタイミングで治療介入することが重要です。最終的な治療目標である生命予後の改善1,25)に向け、新規のエビデンスの蓄積が期待されます。
図16

【参考文献】
- 日本呼吸器学会・日本リウマチ学会. 膠原病に伴う間質性肺疾患診断・治療指針2025. 2025.
- Joy GM. et al.: Eur Respir Rev 2023; 32(167): 220210.
- 厚生労働省 令和6年(2024)人口動態統計月報年計(概数)の概況
- Lee JK. et al.: Clin Pulm Med 2017; 24(5): 191-196.
- Hyldgaard C. et al.: Ann Rheum Dis 2017; 76(10): 1700-1706.
- Hoffmann-Vold AM. et al.: Am J Respir Crit Care Med 2019; 200(10): 1258-1266.
- Cerro Chiang G. et al.: Int J Mol Sci 2023; 24(3): 2405.
- Wells AU. et al.: Nat Rev Rheumatol 2014; 10(12): 728-739.
- Distler JHW. et al.: Nat Rev Rheumatol 2019; 15(12): 705-730.
- Nishioka Y. et al.: Inflamm Regen 2024; 44(1): 34.
- Kinoshita T. et al.: Int J Mol Sci 2019; 20(6): 1461.
- Wollin L. et al.: Eur Respir J 2019; 54(3): 1900161.
- Spagnolo P. et al.: Ann Rheum Dis 2021; 80(2): 143-150.
- Tsukui T. et al.: Nature 2024; 631(8021): 627-634.
- Wijsenbeek M. et al.: N Engl J Med 2020; 383(10): 958-968.
- Kondoh Y, Inoue Y.: Adv Ther 2025; 42(7): 2988-3001. 本論文の執筆は日本ベーリンガーインゲルハイム株式会社の支援により行われました。
- Raghu G. et al.: Am J Respir Crit Care Med 2022; 205: e18-e47.
- Kondoh Y. et al.: Autoimmun Rev 2025; 24(11): 103900.
- Kondoh Y. et al.: Respir Investig 2024; 62(4): 702-709. 本研究は日本ベーリンガーインゲルハイム株式会社の支援により行われました。
- Khor YH. et al.: Am J Respir Crit Care Med 2023;207:102-105.
- Kim DS. et al .: Proc Am Thorac Soc 2006; 3(4): 285-292.
- Lee JK. et al.: Clin Exp Med 2023; 23(8): 4797-4807.
- Pugashetti JV. et al.: Am J Respir Crit Care Med 2023; 207(1): 69-76.
- Kondoh Y. et al.: Chest 1993; 103(6): 1808-1812.
- Suda T. et al.: Respir Med 2009; 103(6): 846-853.
- Suzuki A. et al.: Respirology 2020; 25(5): 525-534.
- Xie M. et al.: BMC Pulm Med 2023; 23(1): 255.
- Liang J. et al.: Front Med (Lausanne) 2020; 7: 12.
- Tomiyama F. et al.: Tohoku J Exp Med 2016; 239(4): 297-305.
- Castelino FV. et al.: ACR Open Rheumatol 2021; 3(5): 295-304.
- Wijsenbeek M. et al.: Curr Med Res Opin 2019; 35(11): 2015-2024. 本研究はベーリンガーインゲルハイム社の支援により行われました。
- Kaneko Y. et al.: Front Med (Lausanne) 2025; 12: 1526530.
- Ryerson CJ. et al.: Eur Respir J 2025: 2500158.
- Antoniou KM. et al.: Ann Rheum Dis 2025: S0003-4967(25)04320-1.
- Nasser M. et al.: Respir Res 2021; 22(1): 162. 本研究はベーリンガーインゲルハイム社の支援により行われました。
その他の関連情報


特発性肺線維症および進行性肺線維症 国際診療ガイドライン2022(静止画)
日本ベーリンガーインゲルハイム
メディカルチャット 利用規約
当社の「日本ベーリンガーインゲルハイム メディカルチャット」(以下「本サービス」といいます)のご利用に際しては、本利用規約が適用されますので、必ず以下の記載事項をご確認下さい。
利用規約
- 本サービスは、当社所定のウェブページから文字によりお問い合わせいただくことにより、当社医薬品等に関する一般的な情報を、人工知能あるいは当社担当者により、文字及び図表により回答するサービスです(以下、人工知能による回答サービスを「AIチャット」、当社担当者による回答サービスを「有人チャット」といいます。)。ただし、AIチャットによる回答を原則とし、有人チャットは、AIチャットでの回答に対し、有人チャットでの回答も希望された場合に、提供させていただきます。
- 本サービスをご利用いただくことができるのは、当社医薬品等を扱いかつ国内に在住する医療関係者の方に限られます。当該医療関係者以外の方は、ご利用いただくことができません。
- 本利用規約に同意いただけない場合、本サービスを利用いただくことができません。本利用規約を最後までお読みいただき、「同意して利用する」ボタンを押した上で、本サービスをご利用下さい。
- 本サービスは、当社医薬品等に関する一般的なお問い合わせに対して回答するものとし、次の各号に掲げるお問い合わせについては、回答しないものとします。
- 当社医薬品等と関係のないお問い合わせ、または本サービスの回答範囲を逸脱したお問い合わせ
- 具体的な症状や治療方法に関するお問合せ
- 当社に適用される法令、ガイドラインまたは行政上の指導、当社自主規制その他当社が遵守すべきルールにより回答できないお問い合わせ
- 文字化け等により入力内容が判断できないお問い合わせ
- 前各号に掲げるほか、本サービスにより、適切な回答をすることができないと当社が判断した事項に関するお問い合わせ
- 本サービスは、日本語のみに対応しています。
- 本サービスは、当社医薬品の副作用、不具合及び有害事象の報告を受け付けていません。
- お問い合わせの内容によっては、本サービスでは十分に回答できない場合もございます。予めご了承下さい。
- 本サービスの利用可能時間は、以下のとおりです。
- AIチャット
24時間365日 - 有人チャット
平日9:00~17:00
- AIチャット
- 前項に関わらず、メンテナンス及び障害等のため一時的に本サービスを中断する場合がございます。
本サービスのご利用の際には、原則として、個人情報(お名前、ご住所、電話番号、メールアドレス等)を入力しないようお願いします。ただし、AIチャット及び有人チャットを問わず、当社医薬品の適用外使用に関するお問い合わせについては、コンプライアンス上の理由により、当社より、氏名及び施設名の入力を求める場合がございます。この場合には、当社プライバシーポリシーの内容を確認いただき、同意いただける場合に限り、入力して下さい(プライバシーポリシーについては「VIII 利用規約、プライバシーポリシー」に記載のURLからアクセス下さい)。その他の場合に、当社より個人情報の入力を求めることは一切ございません。
- 当社医薬品のご使用にあたっては、最新の添付文書等をご確認下さい。
- 当社は、本サービスまたは本サービスにより提供される情報の利用に際し生じた結果については、一切責任を負いません。
本サービスの利用にあたり、以下の各号の行為を禁止します。
- 本サービスにより提供される情報を複製、複写、転載、改変等する行為
- 第三者または当社の知的財産権その他の権利を侵害する行為
- 第三者または当社を誹謗中傷し、または名誉・信用を毀損する行為
- 本サービスの利用による営利目的の行為
- 本サービスの運営又は他の利用者による本サービスの利用の妨げとなる行為
- 前各号のほか、当社が不適当であると判断する行為
当社は、いつでも本サービスの提供を終了、またはその内容を変更することができるものとします。
本サービスの利用に関しては、以下の利用規約及びプライバシーポリシーが併せて適用されますので、ご確認下さい。



