
糖尿病合併の慢性腎臓病に対する治療を再考する
サイトへ公開:2025年11月11日 (火)
クイックリンク
2型糖尿病を併発した慢性腎臓病患者さんにおける腎・心血管疾患のイベントリスクと推算糸球体ろ過量(eGFR)に関する疫学データ紹介後、EMPA-KIDNEY試験、EMPA-REG OUTCOME試験の結果をお伝えします。


こちらは2型糖尿病と高血圧を合併するCKDステージG3aの患者さんです。
この患者さんのeGFRは51mL/min/1.73m2、尿蛋白は定性(-)、尿中アルブミン/クレアチニン比(UACR)は20mg/gCrです。
2型糖尿病に対してはジペプチジルペプチダーゼ4(DPP-4)阻害薬、高血圧に対してはアンジオテンシンⅡ受容体拮抗薬(ARB)で治療中です。
ARBは腎機能低下抑制のエビデンスを持つ薬剤ですが、追加治療の余地はないでしょうか。
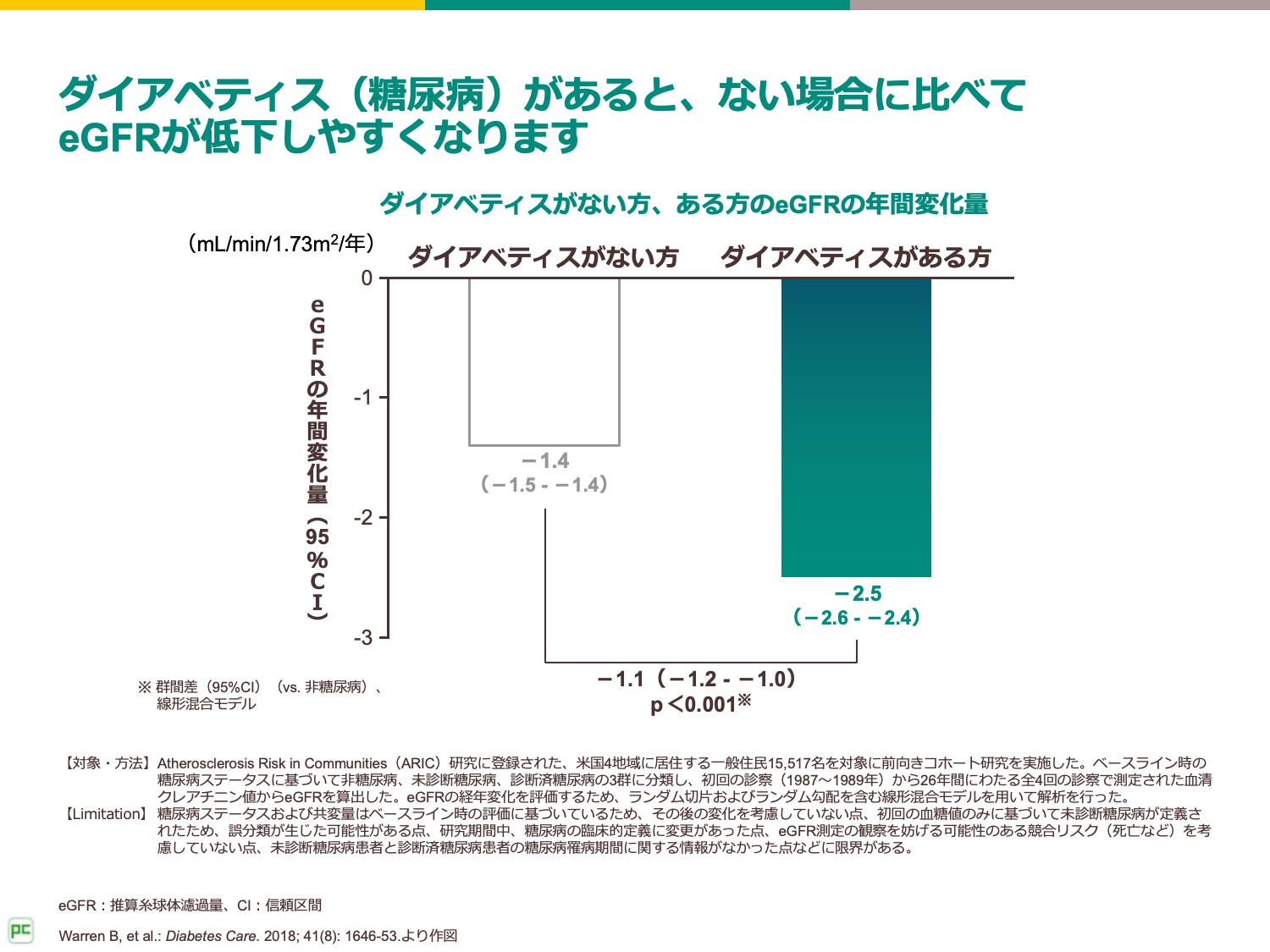
最初に、米国に居住する一般住民15,517名を対象に実施された前向きコホート研究を紹介します。
28年間にわたる全4回の診察で測定された血清クレアチニン値からeGFRを算出したところ、糖尿病のある患者さんは、ない患者さんに比べてeGFRが低下しやすい、すなわちeGFRスロープの低下速度が速いことが示されました 1)。
先生方のご実感としてはいかがでしょうか。
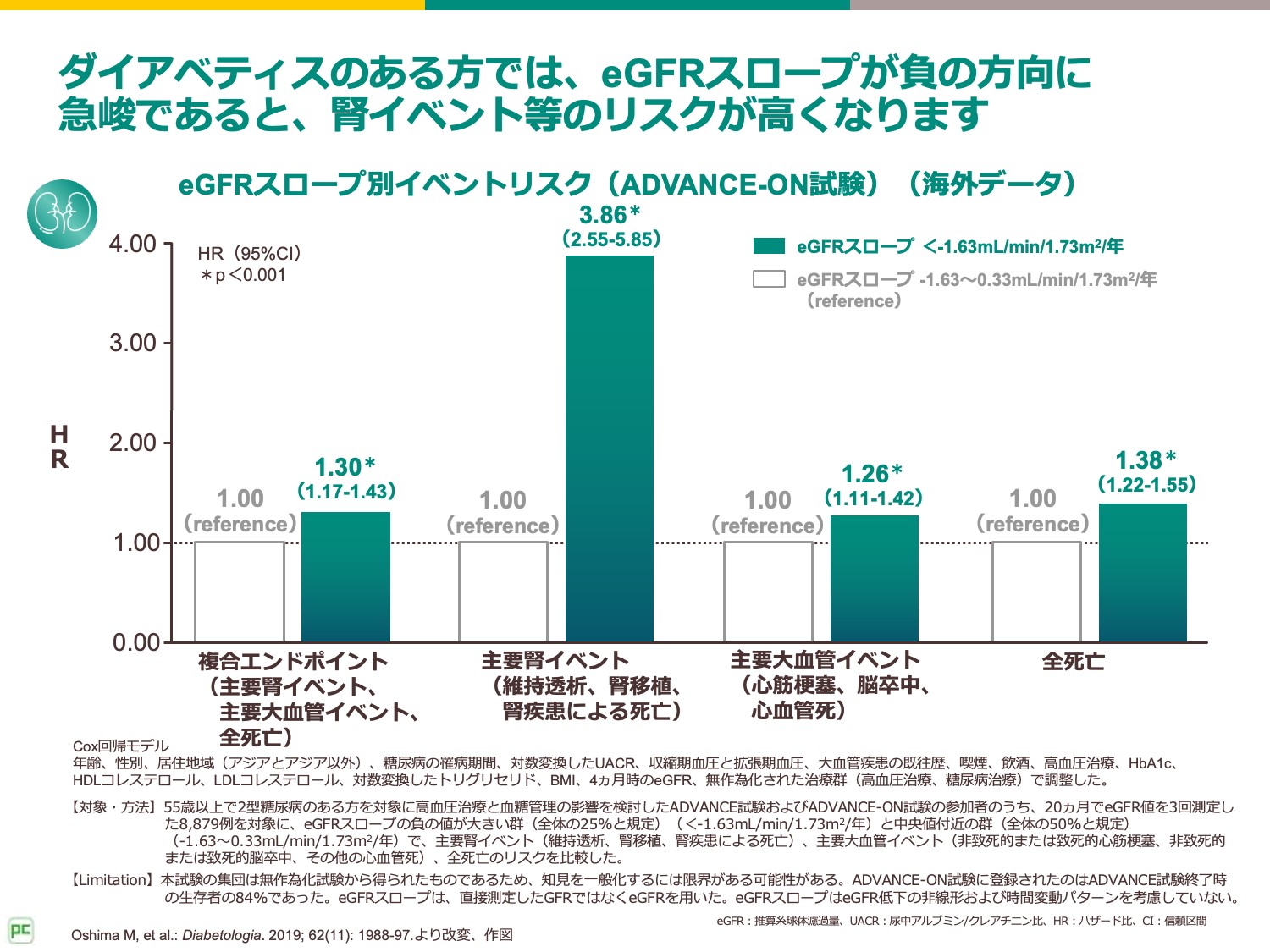
また、ADVANCE試験およびADVANCE-ON試験に参加した8879例の参加者のeGFRスロープを観察し、イベントリスクとの相関をみたデータを紹介します。
1年間当たりのeGFRスロープの値が-1.63~0.33mL/min/1.73m2の群に比べ、-1.63mL/min/1.73m2より低い群では、主要腎イベントや主要大血管イベントのリスクが増加することが示されました 2)。
EMPA-KIDNEY試験データ

本スライドより、ジャディアンスのエビデンスを紹介します。
EMPA-KIDNEY試験 3)は腎疾患進行のリスクのある慢性腎臓病患者を対象に、ジャディアンス10mgを1日1回経口投与した時の腎疾患進行または心血管死の初回発現までの期間に対する有効性および安全性を、プラセボと比較検討した試験です。

有効性・安全性の評価項目、解析計画は記載の通りとなります。
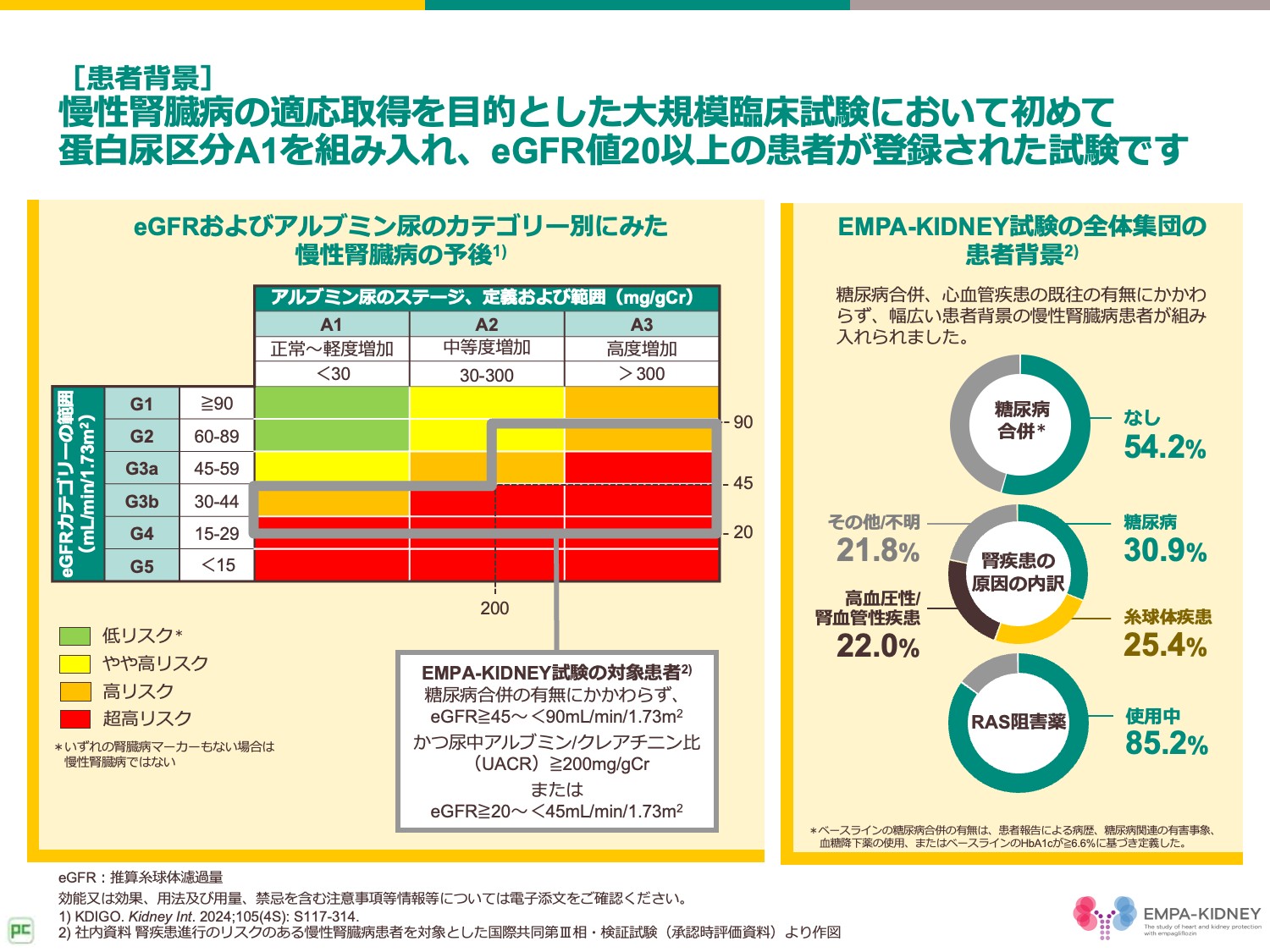
本試験の特性として注目いただきたい点は、慢性腎臓病の適応取得を目的とした大規模臨床試験において初めて蛋白尿区分A1を組み入れ、eGFR値20以上の患者が登録された点です。
こちらにお示しのように、アルブミン尿、糖尿病の有無にかかわらず、幅広いeGFR値の慢性腎臓病患者が組み入れられております。
糖尿病の合併無しの患者が54.2%、RAS阻害薬使用中の患者が85.2%でした。
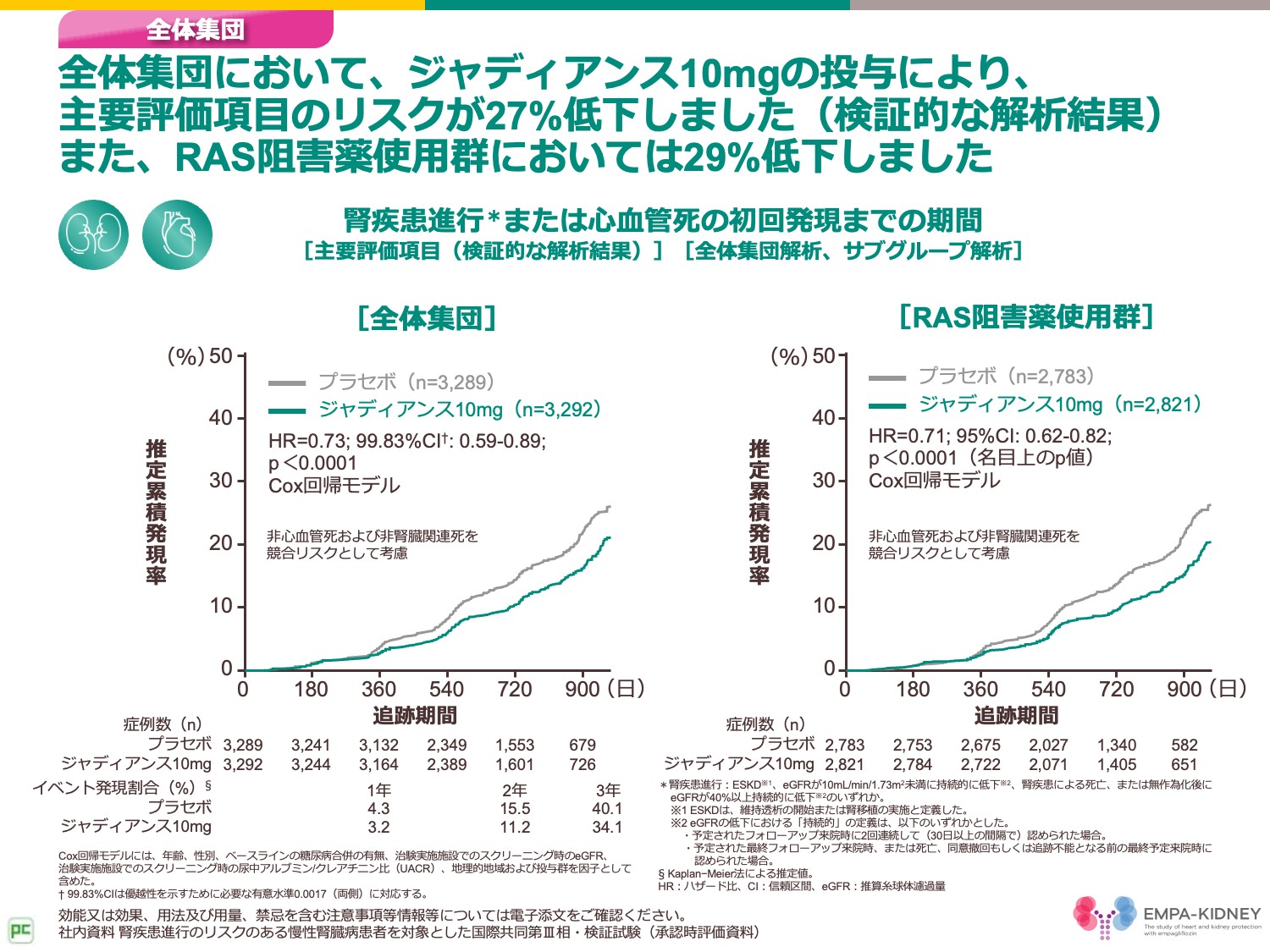
こちらが全体集団とRAS阻害薬使用群における主要評価項目に対する結果です。
全体集団においては、ジャディアンス10mgの投与によって腎疾患進行または心血管死の初回発現リスクが27%低下しました。
また、既にRAS阻害薬を投与中の患者においてもジャディアンス10mgの追加投与により、腎疾患進行または心血管死の初回発現リスクが29%低下しました。
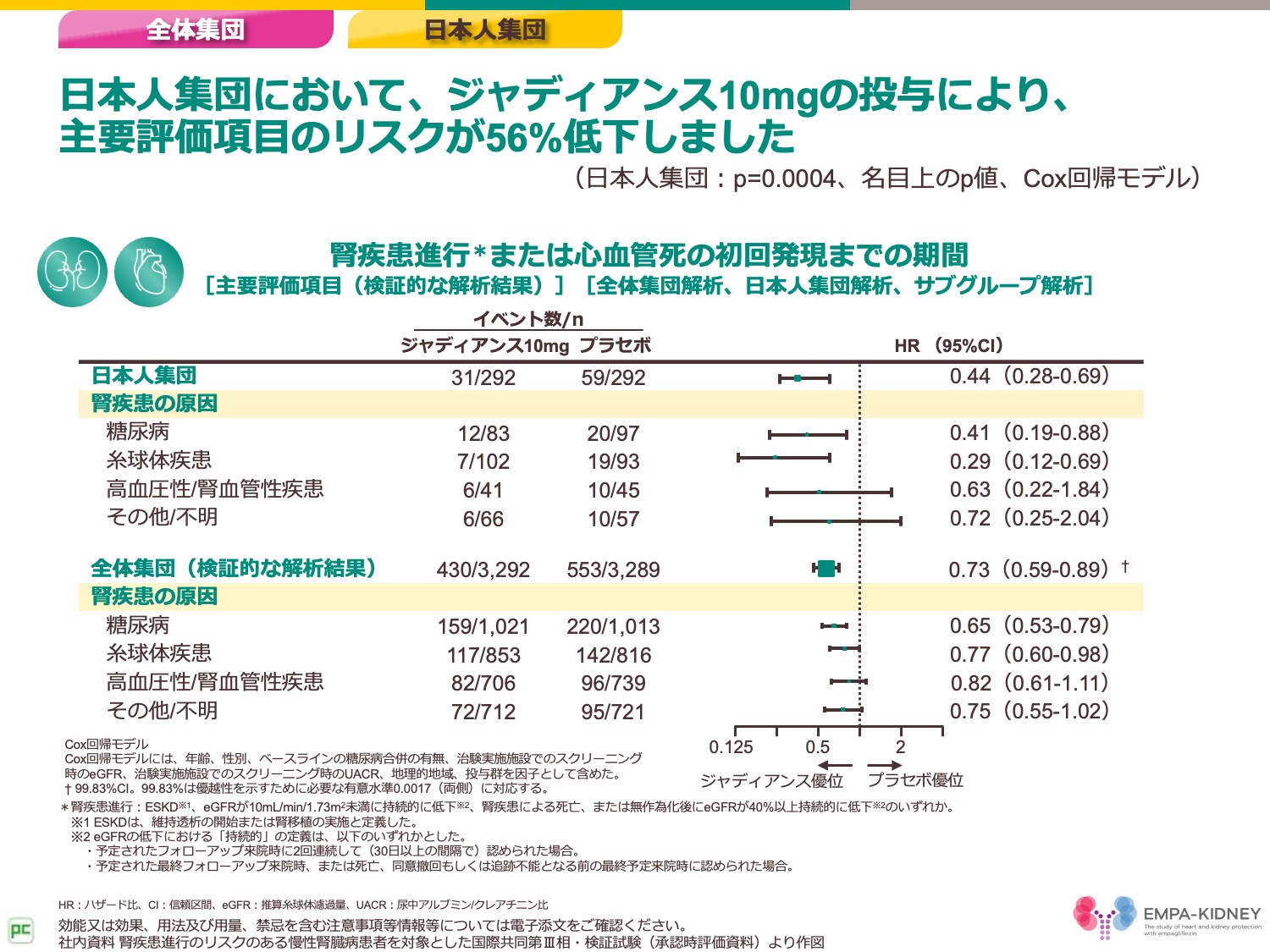
こちらは日本人集団におけるベースラインの糖尿病の有無、RAS阻害薬使用有無別に見た主要評価項目に対する結果です。
日本人においても、ジャディアンス10mgの投与により主要評価項目のリスクが56%低下しました。
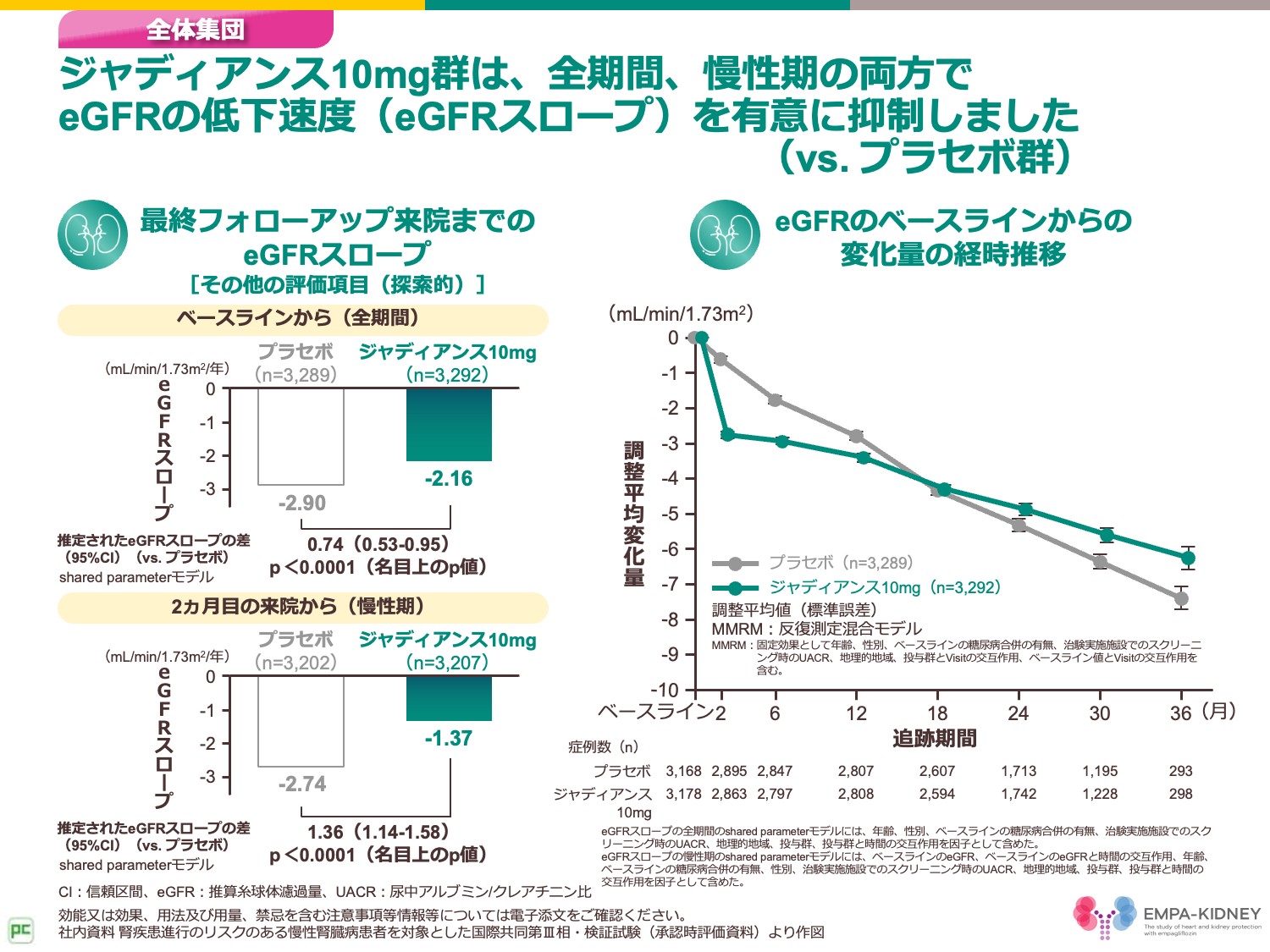
さらに、冒頭で心血管イベントとの関連性についてお示ししたeGFRスロープに関するジャディアンスのデータをご紹介いたします。
全期間におけるeGFRスロープは、プラセボ群に比べてジャディアンス10mg群で0.74mL/min/1.73m2/年と有意に負の傾きを緩やかにしました。
そして、2ヵ月目の来院から最終フォローアップ来院までの慢性期で見た際には、プラセボ群に比べてジャディアンス10mg群で1.36mL/min/1.73m2/年とeGFRスロープの負の傾きの有意な改善を示しました。
なお、eGFRのベースラインからの変化量の経時推移は、右側の図のとおり、18ヵ月でクロスしていました。
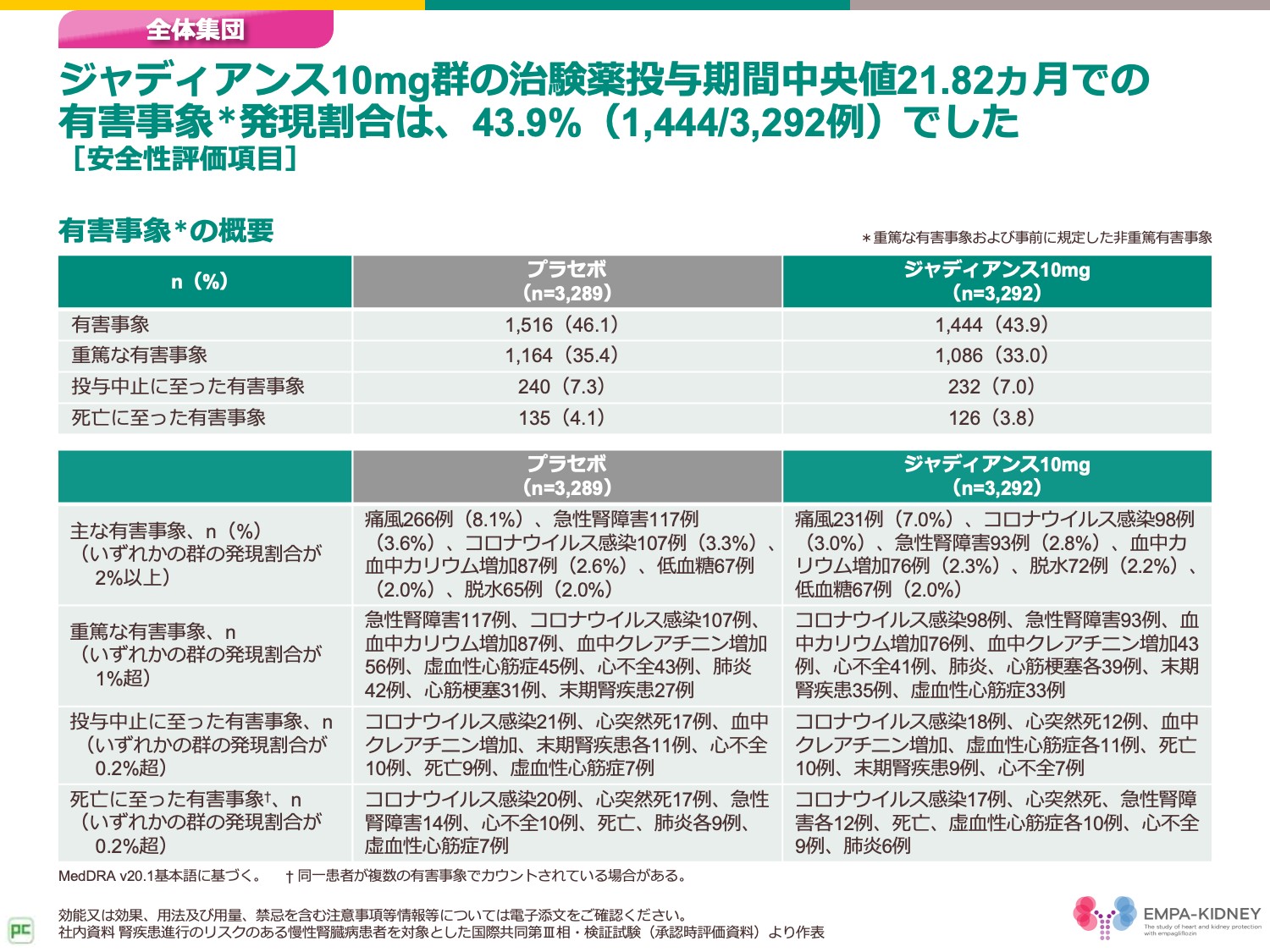
安全性について、事前に規定した非重篤有害事象および全ての重篤な有害事象に限定して有害事象を収集した結果、全体集団での発現割合はジャディアンス10mg群で43.9%でした。
主な有害事象は、ジャディアンス10mg群で痛風7.0%、コロナウイルス感染3.0%、急性腎障害2.8%等でした。
また、重篤な有害事象は、ジャディアンス10mg群でコロナウイルス感染98例、急性腎障害93例、血中カリウム増加76例等でした。
なお、投与中止、死亡に至った有害事象は表のとおりでした。
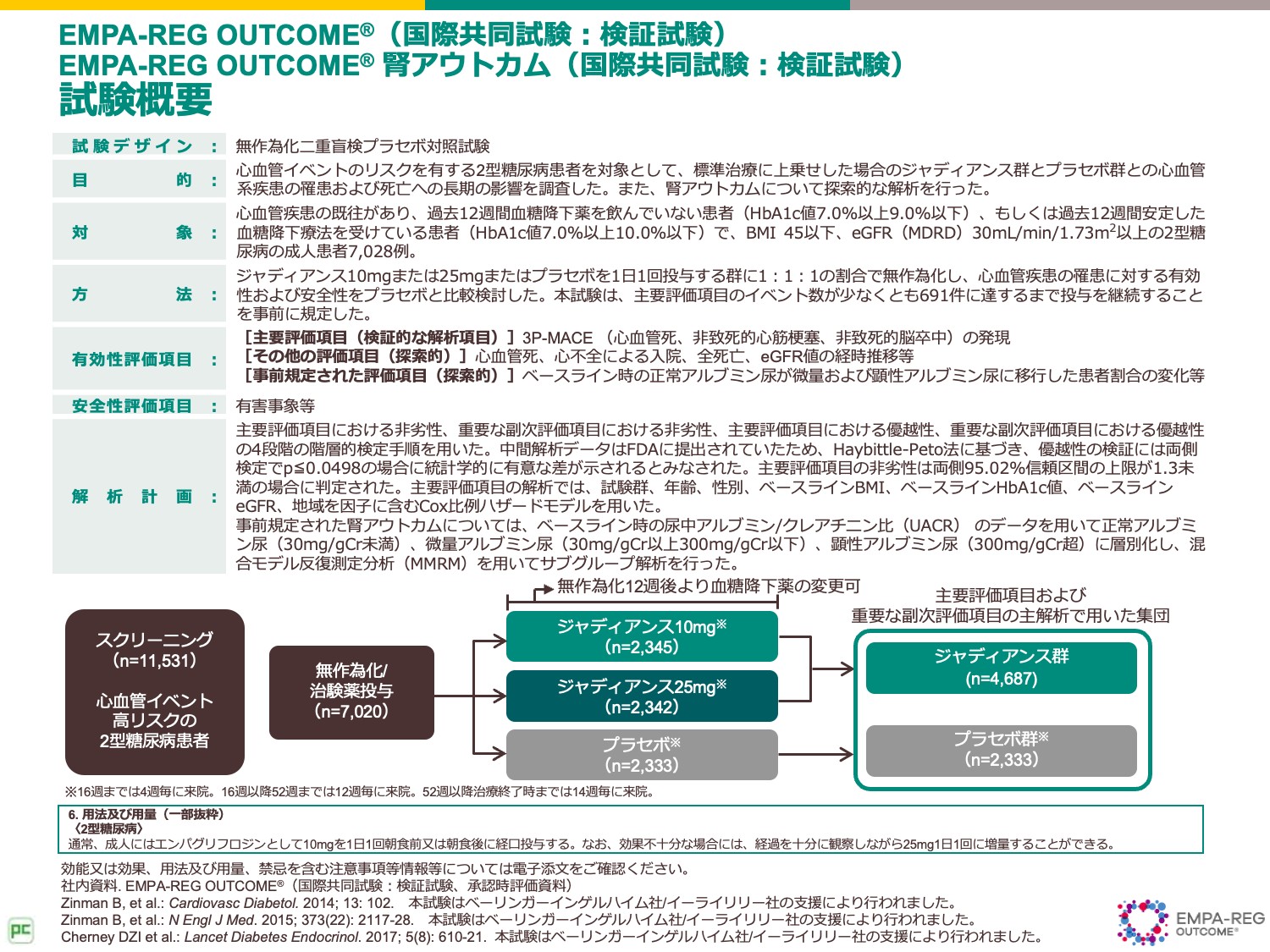
また、ジャディアンス10mgの心血管死に対する効果については、EMPA-REG OUTCOME試験にて検討されています 5) -8)。
EMPA-REG OUTCOME試験では、心血管イベントのリスクを有する2型糖尿病患者を対象として、標準治療に上乗せした場合のジャディアンス群とプラセボ群との心血管系疾患の罹患および死亡への長期の影響を調査しました。
また、腎アウトカムについて探索的な解析を行いました。
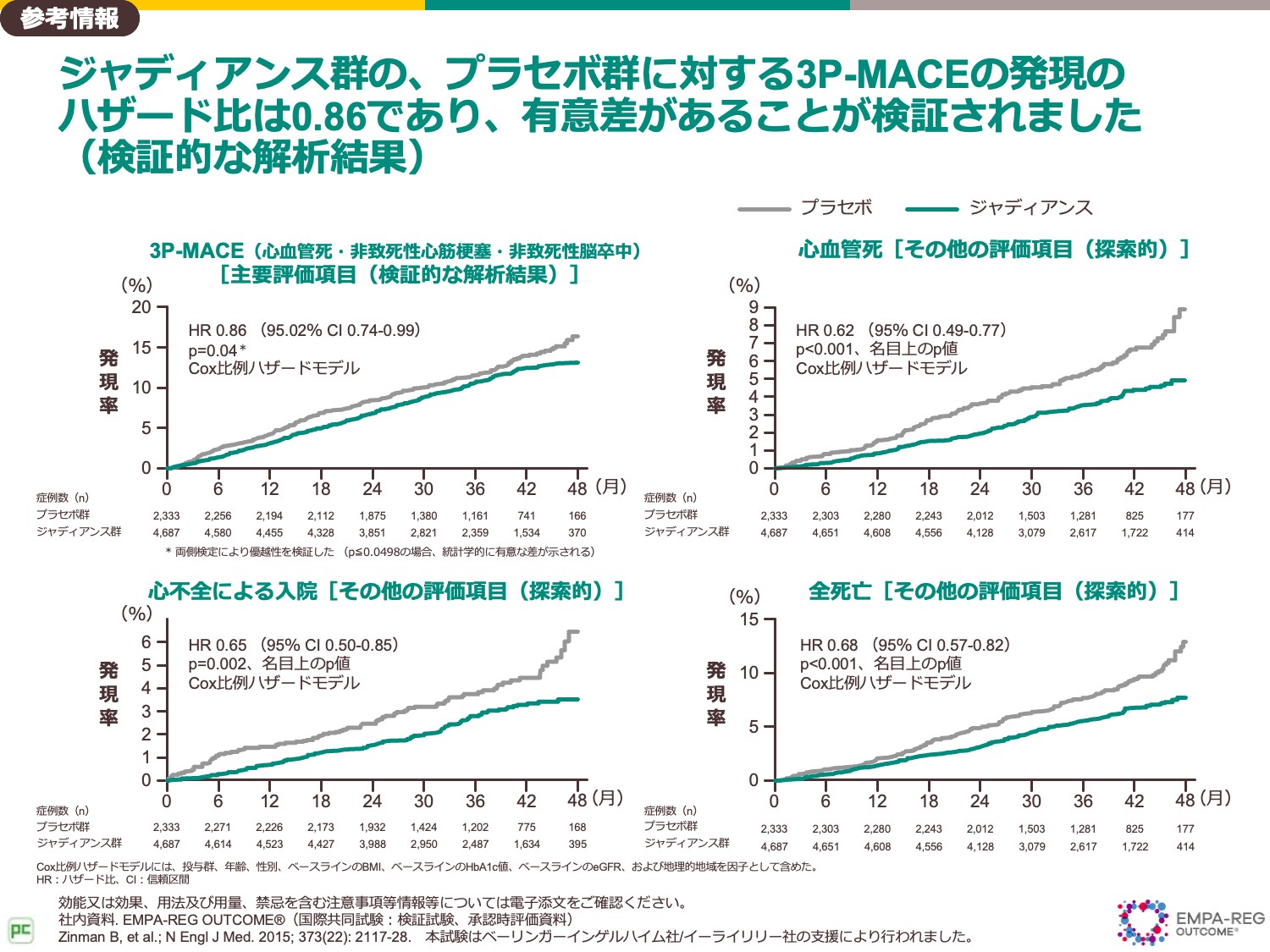
結果としては、左上の主要評価項目である3P-MACE(心血管死、非致死的心筋梗塞、非致死的脳卒中)では14%の有意なイベント抑制を示しました。
そして副次評価項目である心血管死、全死亡、心不全による入院、これらいずれの項目においても、プラセボ群に対してジャディアンス群で有意なイベントリスク抑制を示しました。
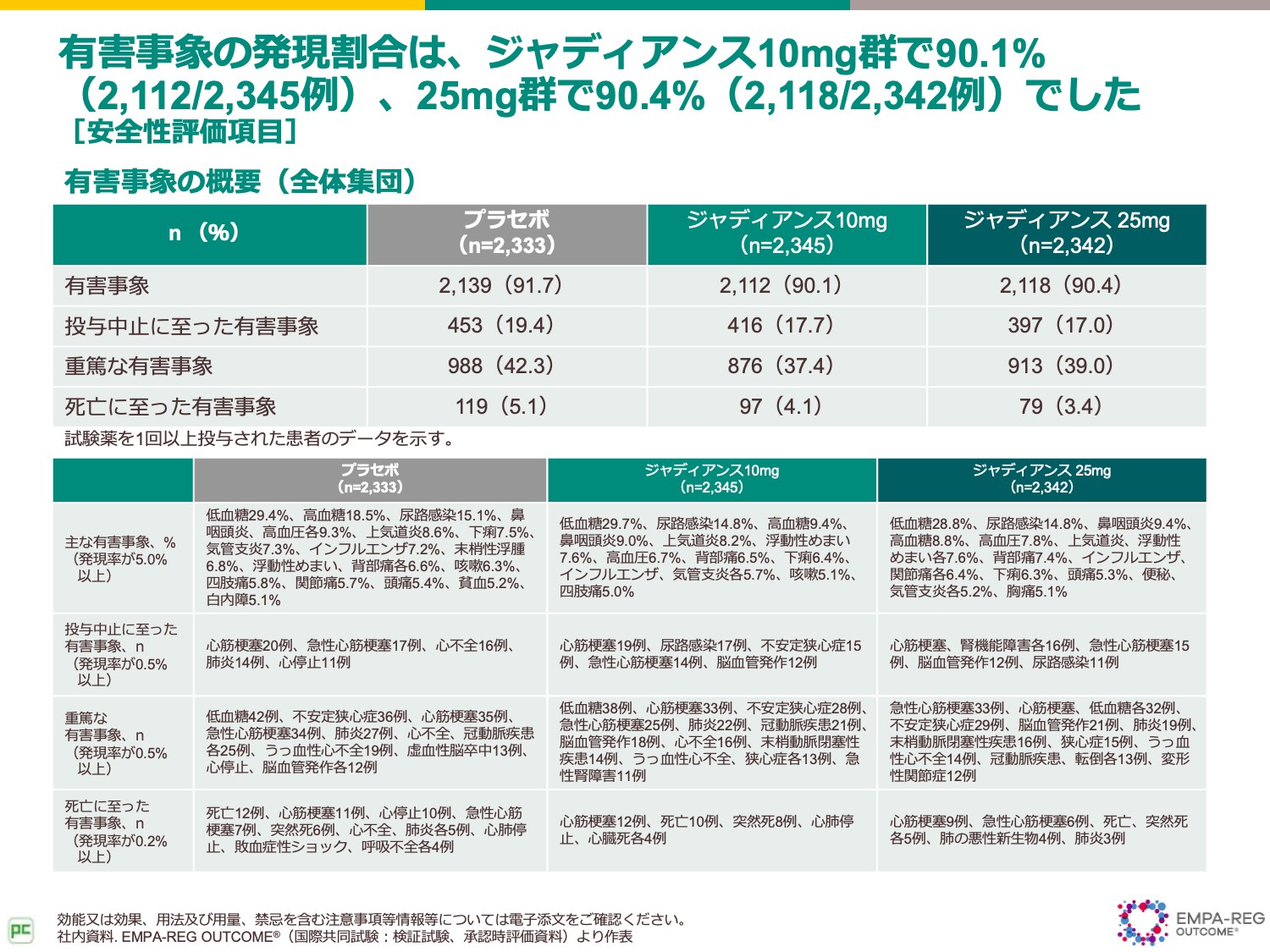
安全性について、事前に規定した非重篤有害事象および全ての重篤な有害事象に限定して有害事象を収集した結果、全体集団での発現割合はジャディアンス10mg群で90.1%、ジャディアンス25mg群で90.4%でした。
主な有害事象は、ジャディアンス10mg群で低血糖29.7%、尿路感染14.8%、高血糖9.4%等であり、ジャディアンス25mg群で低血糖28.8%、尿路感染14.8%、鼻咽頭炎9.4%でした。
また、重篤な有害事象は、ジャディアンス10mg群で低血糖38例、心筋梗塞33例、不安定狭心症28例等であり、ジャディアンス25mg群で急性心筋梗塞33例、心筋梗塞32例、低血糖32例等でした。
なお、投与中止、死亡に至った有害事象は表のとおりでした。
今回は2型糖尿病を併発した慢性腎臓病患者さんにおける腎機能と心血管イベントリスクとの関連性および、EMPA-KIDNEY試験、EMPA-REG OUTCOME試験についてご紹介しました。
2型糖尿病はeGFRの低下速度を速め、CKD進行のリスク因子となります。
また、eGFRスロープの低下速度が速くなるほど、腎イベントだけでなく心血管イベントのリスクが増加します。
2型糖尿病の治療目的の1つである合併症リスク抑制のために、腎・心血管イベントリスクを見据えた治療選択肢として、ジャディアンス10mg ※1をぜひご検討ください。
※1ただし、末期腎不全又は透析施行中の患者を除く
<参考文献>
- Warren B, et al. Diabetes Care. 2018 ; 41 : 1646-53.
- Oshima M, et al. Diabetologia. 2019 ; 62 : 1988-97. 著者にベーリンガーインゲルハイム社より講演料等を受領している者が含まれます。
- 社内資料 腎疾患進行リスクのある慢性腎臓病患者を対象とした国際共同第Ⅲ相・検証試験(承認時評価資料)
- ジャディアンス電子添文2025年9月改訂(第8版).
- 社内資料. EMPA-REG OUTCOME®(国際共同試験:検証試験、承認時評価資料).
- Zinman B, et al. Cardiovasc Diabetol. 2014 ; 13 : 102. 本試験はベーリンガーインゲルハイム社の支援により行われました。
- Zinman B, et al. N Engl J Med. 2015 ; 373 : 2117-28. 本試験はベーリンガーインゲルハイム社の支援により行われました。
- Cherney DZI, et al. Lancet Diabetes Endocrinol. 2017 ; 5 : 610-21. 本試験はベーリンガーインゲルハイム社の支援により行われました。
その他の関連情報


G3aで正常アルブミン尿の2型糖尿病を併発しているCKDのリスクを考える
日本ベーリンガーインゲルハイム
メディカルチャット 利用規約
当社の「日本ベーリンガーインゲルハイム メディカルチャット」(以下「本サービス」といいます)のご利用に際しては、本利用規約が適用されますので、必ず以下の記載事項をご確認下さい。
利用規約
- 本サービスは、当社所定のウェブページから文字によりお問い合わせいただくことにより、当社医薬品等に関する一般的な情報を、人工知能あるいは当社担当者により、文字及び図表により回答するサービスです(以下、人工知能による回答サービスを「AIチャット」、当社担当者による回答サービスを「有人チャット」といいます。)。ただし、AIチャットによる回答を原則とし、有人チャットは、AIチャットでの回答に対し、有人チャットでの回答も希望された場合に、提供させていただきます。
- 本サービスをご利用いただくことができるのは、当社医薬品等を扱いかつ国内に在住する医療関係者の方に限られます。当該医療関係者以外の方は、ご利用いただくことができません。
- 本利用規約に同意いただけない場合、本サービスを利用いただくことができません。本利用規約を最後までお読みいただき、「同意して利用する」ボタンを押した上で、本サービスをご利用下さい。
- 本サービスは、当社医薬品等に関する一般的なお問い合わせに対して回答するものとし、次の各号に掲げるお問い合わせについては、回答しないものとします。
- 当社医薬品等と関係のないお問い合わせ、または本サービスの回答範囲を逸脱したお問い合わせ
- 具体的な症状や治療方法に関するお問合せ
- 当社に適用される法令、ガイドラインまたは行政上の指導、当社自主規制その他当社が遵守すべきルールにより回答できないお問い合わせ
- 文字化け等により入力内容が判断できないお問い合わせ
- 前各号に掲げるほか、本サービスにより、適切な回答をすることができないと当社が判断した事項に関するお問い合わせ
- 本サービスは、日本語のみに対応しています。
- 本サービスは、当社医薬品の副作用、不具合及び有害事象の報告を受け付けていません。
- お問い合わせの内容によっては、本サービスでは十分に回答できない場合もございます。予めご了承下さい。
- 本サービスの利用可能時間は、以下のとおりです。
- AIチャット
24時間365日 - 有人チャット
平日9:00~17:00
- AIチャット
- 前項に関わらず、メンテナンス及び障害等のため一時的に本サービスを中断する場合がございます。
本サービスのご利用の際には、原則として、個人情報(お名前、ご住所、電話番号、メールアドレス等)を入力しないようお願いします。ただし、AIチャット及び有人チャットを問わず、当社医薬品の適用外使用に関するお問い合わせについては、コンプライアンス上の理由により、当社より、氏名及び施設名の入力を求める場合がございます。この場合には、当社プライバシーポリシーの内容を確認いただき、同意いただける場合に限り、入力して下さい(プライバシーポリシーについては「VIII 利用規約、プライバシーポリシー」に記載のURLからアクセス下さい)。その他の場合に、当社より個人情報の入力を求めることは一切ございません。
- 当社医薬品のご使用にあたっては、最新の添付文書等をご確認下さい。
- 当社は、本サービスまたは本サービスにより提供される情報の利用に際し生じた結果については、一切責任を負いません。
本サービスの利用にあたり、以下の各号の行為を禁止します。
- 本サービスにより提供される情報を複製、複写、転載、改変等する行為
- 第三者または当社の知的財産権その他の権利を侵害する行為
- 第三者または当社を誹謗中傷し、または名誉・信用を毀損する行為
- 本サービスの利用による営利目的の行為
- 本サービスの運営又は他の利用者による本サービスの利用の妨げとなる行為
- 前各号のほか、当社が不適当であると判断する行為
当社は、いつでも本サービスの提供を終了、またはその内容を変更することができるものとします。
本サービスの利用に関しては、以下の利用規約及びプライバシーポリシーが併せて適用されますので、ご確認下さい。



