
HER2 non-TKD変異陽性肺癌に対するヘルネクシオス®の有用性(静止画)
サイトへ公開:2026年04月28日 (火)
クイックリンク
ご監修:田中 謙太郎 先生(鹿児島大学大学院 医歯学総合研究科 呼吸器内科学分野 准教授)

日本人のHER2遺伝子変異陽性非小細胞肺癌(NSCLC)において、non-TKD変異は11%と報告されています1)。
本コンテンツでは、各種バリアントに対するヘルネクシオス®の阻害活性及びBeamion LUNG-1試験の第Ib相2,3)におけるnon-TKD変異症例のデータについて、鹿児島大学大学院 医歯学総合研究科 呼吸器内科学分野 准教授 田中 謙太郎 先生にご解説いただきました。
1)Kato Y. et al.: Lung Cancer 2024; 197: 107992.
2)社内資料:国際共同第I相試験(Beamion LUNG-1)[承認時評価資料]
3)Heymach JV. et al.: N Engl J Med 2025; 392(23): 2321-2333. 本試験はベーリンガーインゲルハイム社の支援により行われた。
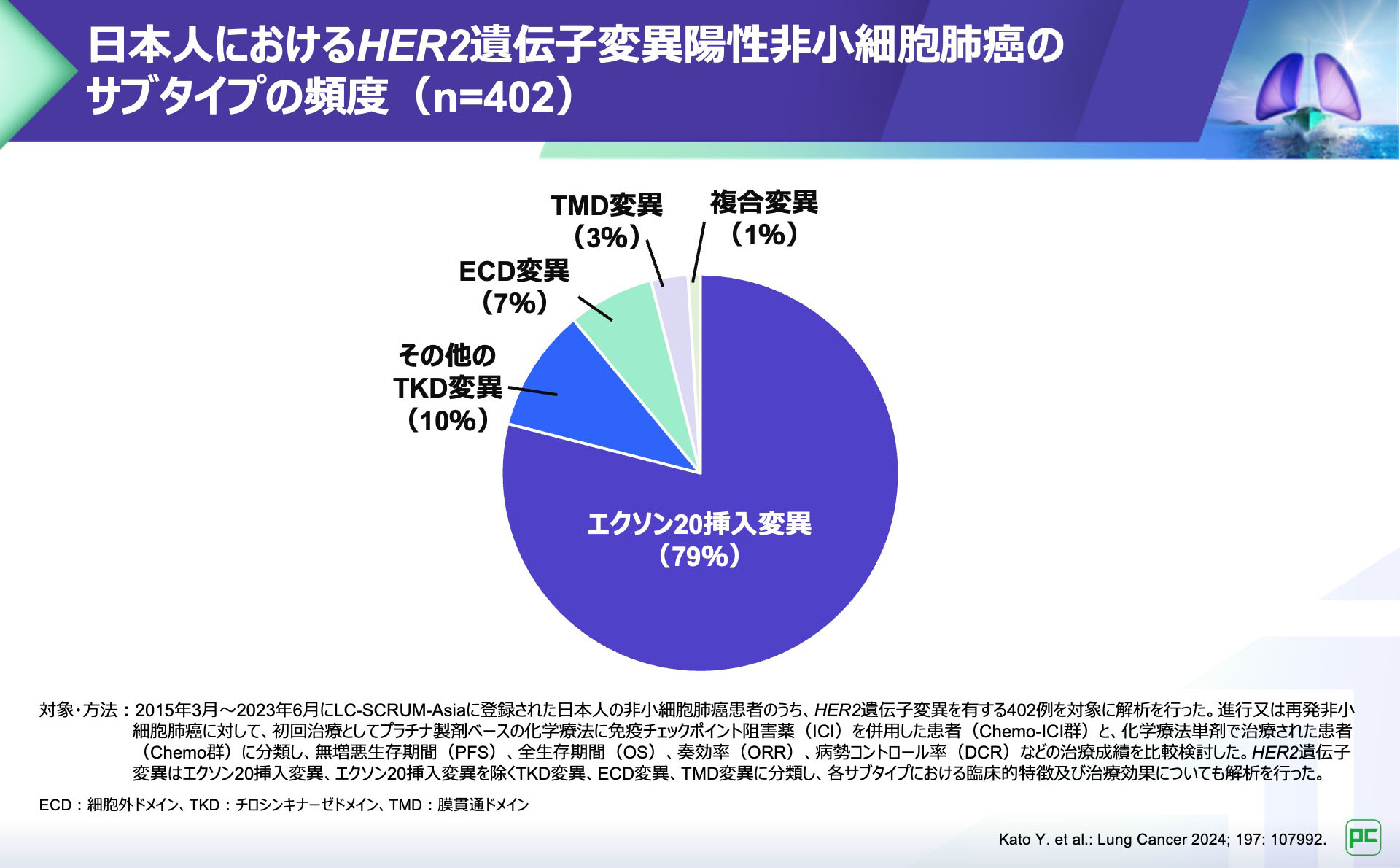
日本人におけるHER2遺伝子変異陽性非小細胞肺癌のサブタイプの頻度
HER2遺伝子変異の代表的なサブタイプには、エクソン20挿入変異、TKD変異、ECD変異、TMD変異などがあります。
日本人を対象とした報告では、non-TKD変異は11%と報告されています。
ヘルネクシオス®の効能又は効果、用法及び用量
ヘルネクシオス®は、Beamion LUNG-1試験において有効性と安全性が検討され、日本では2025年9月に承認を取得しました。

ヘルネクシオス®の作用機序
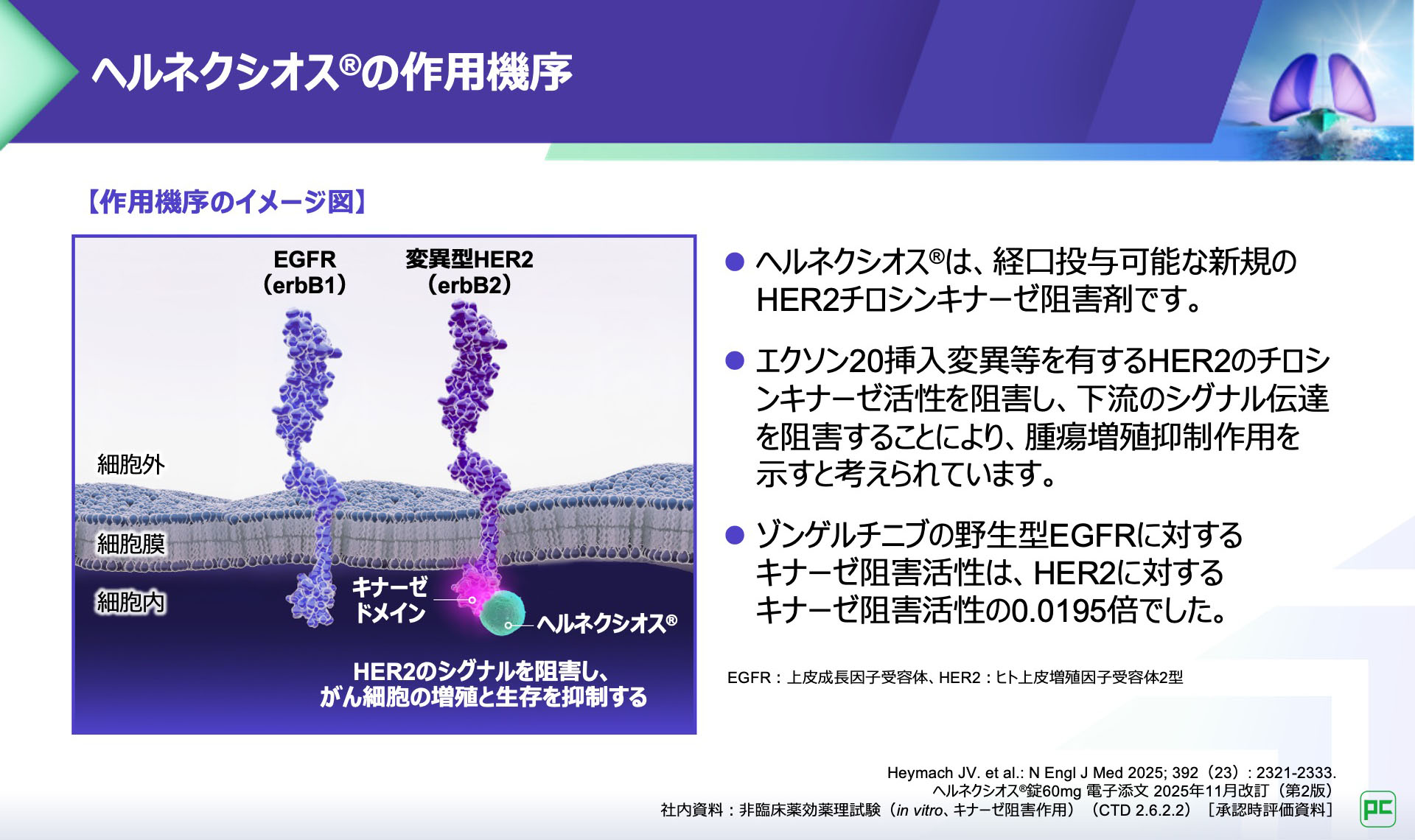
ヘルネクシオス®は、経口投与可能な新規のHER2チロシンキナーゼ阻害剤です3)。
エクソン20挿入変異等を有するHER2のチロシンキナーゼ活性を阻害し、下流のシグナル伝達を阻害することにより、腫瘍増殖抑制作用を示すと考えられています4)。
HER2選択性を高めた特性により、ヘルネクシオス®は、臨床においてもHER2遺伝子変異陽性NSCLCの腫瘍増殖及び疾患進行を抑制することが可能となります。
3)Heymach JV. et al.: N Engl J Med 2025; 392(23): 2321-2333. 本試験はベーリンガーインゲルハイム社の支援により行われた。
4)ヘルネクシオス®錠60mg 電子添文 2025年11月改訂(第2版)
ここからは、ヘルネクシオス®の有効性と安全性を評価した「国際共同第I相試験Beamion LUNG-1試験」をご紹介します。
試験概要
Beamion LUNG-1試験の第Ib相(用量拡大パート)では、進行/転移性のHER2変異陽性NSCLC患者を対象に、ヘルネクシオス®の有効性と安全性を評価しました。
同試験では、日本を含む18ヵ国で241例が登録され、そのうち日本人患者は26例でした。
同試験の第Ib相用量拡大パートのうちコホート1では、まず初めに用量最適化相として、治療歴のあるHER2変異陽性NSCLC患者を、ヘルネクシオス®120mg群又は240mg群にランダムに割り付け、治療を実施しました。
その後、用量最適化相のデータを踏まえて、120mgを推奨用量とし、コホート1を含むすべてのコホートで240mg群への組入れは中止となりました。
コホート3では、治療歴があるTKD変異以外のHER2変異陽性NSCLC患者及びHER2 TKD変異陽性扁平上皮NSCLC患者を対象に、探索的な解析を行いました。

はじめに、コホート1の結果をご紹介します。
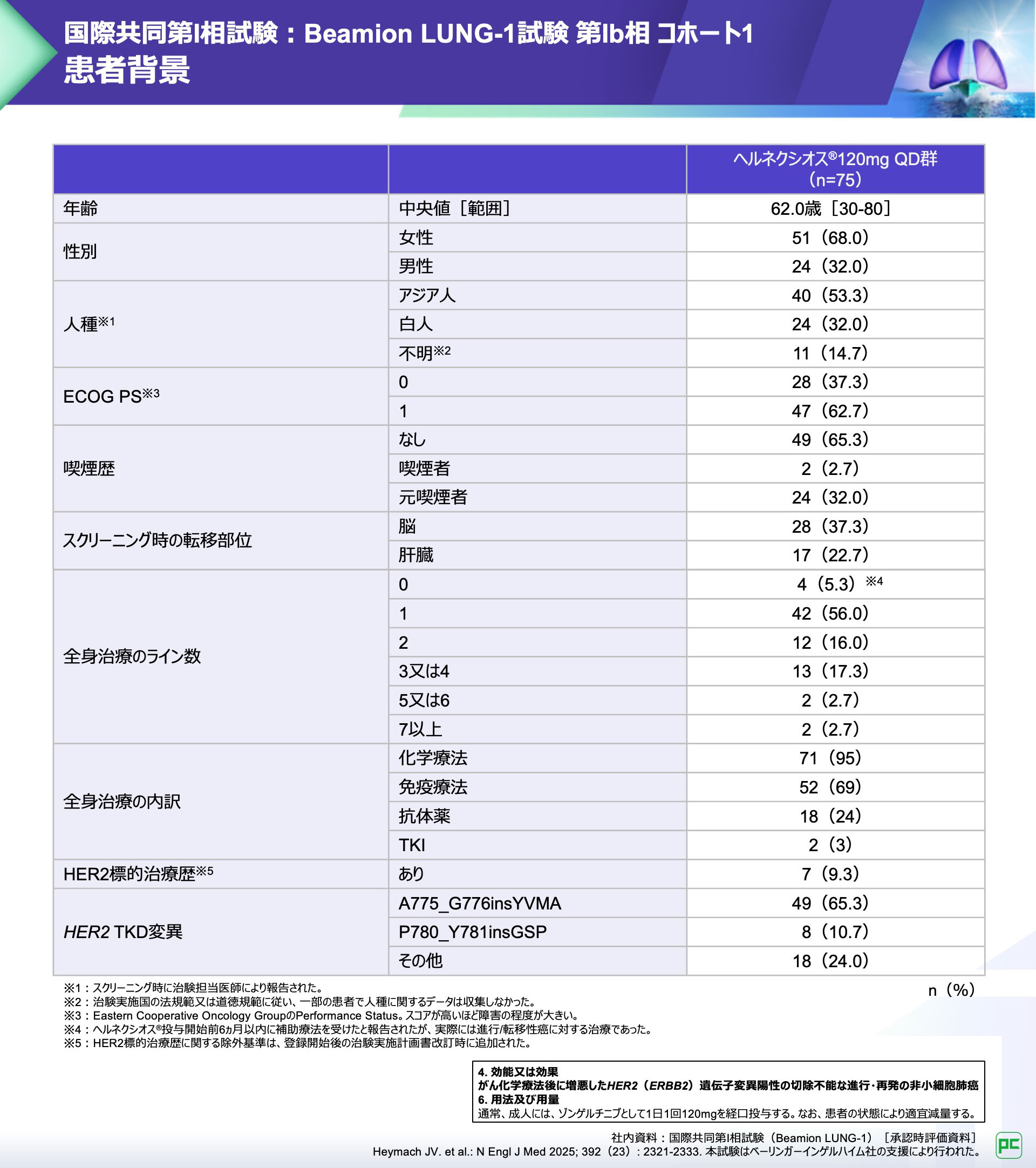
患者背景
年齢中央値は62歳で、二次治療の患者は46例(61.3%)含まれていました。
試験結果
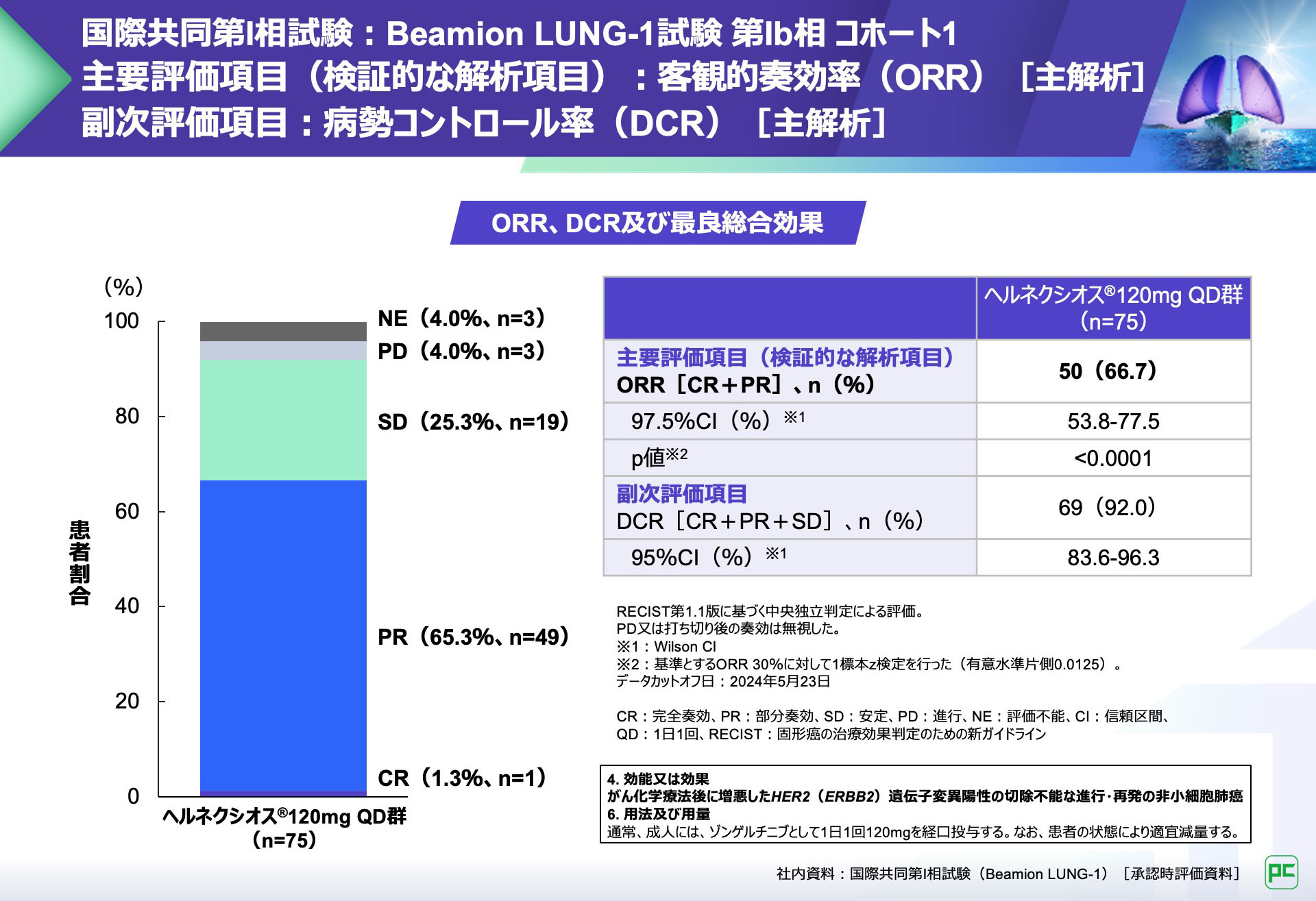
主要評価項目である客観的奏効率(ORR※1)は66.7%(50/75例、97.5%CI:53.8-77.5)と事前に規定された基準(ORR 30%)を上回りました(片側p<0.0001、検証的な解析結果、1標本z検定)。
また、副次評価項目である病勢コントロール率(DCR※2)は92.0%でした。
※1:ORR=CR+PR、※2:DCR=CR+PR+SD
ヘルネクシオス®との因果関係ありと判断された有害事象は75例中73例(97.3%)に認められました。
主な有害事象は下痢(54.7%)、AST増加(24.0%)、発疹(22.7%)、ALT増加(21.3%)などでした。
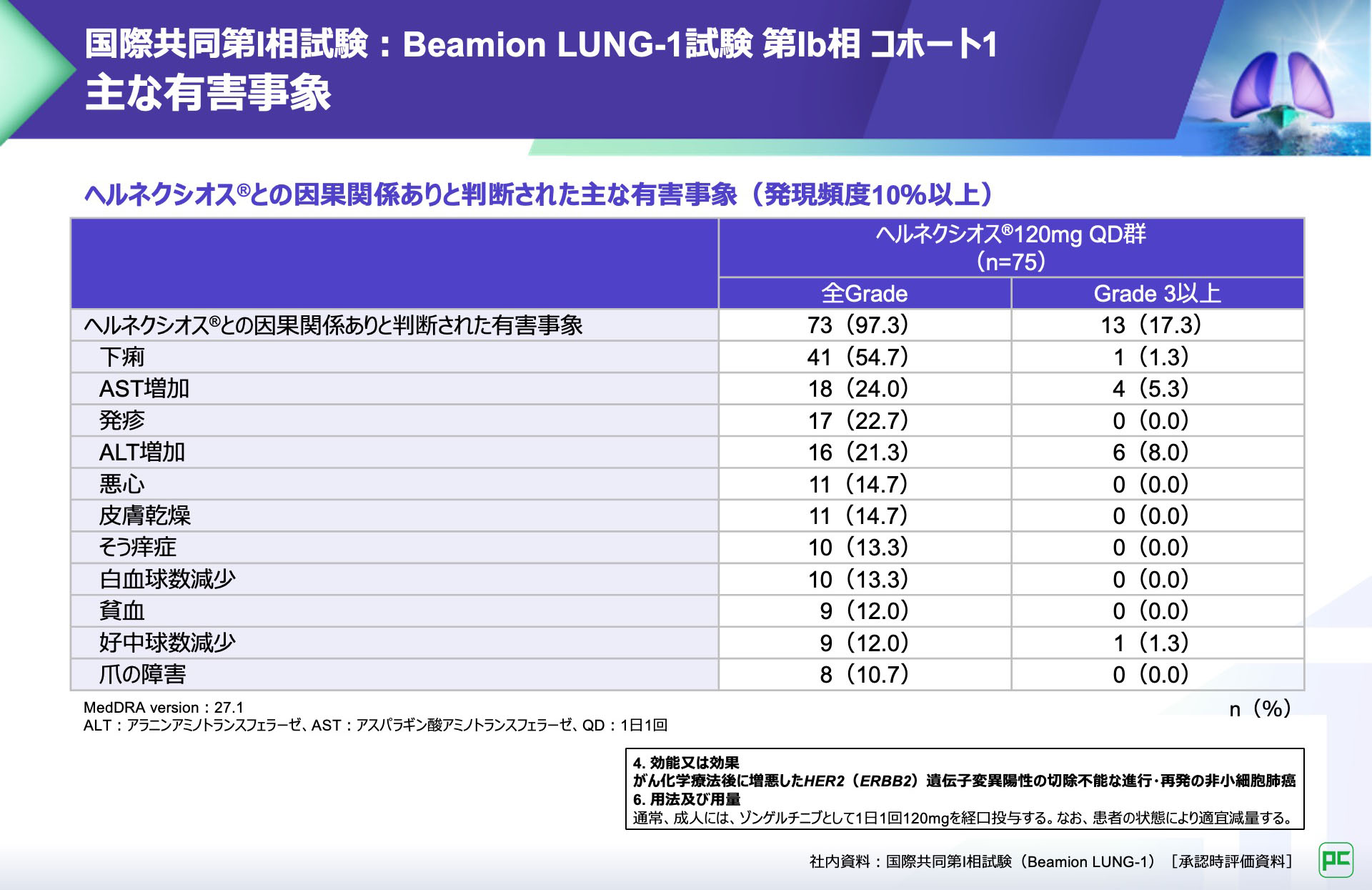
ヘルネクシオス®との因果関係ありと判断された重篤な有害事象は3例(4.0%)に認められ、ALT増加、AST増加が報告されました。
ヘルネクシオス®との因果関係ありと判断された死亡に至った有害事象は報告がありませんでした。
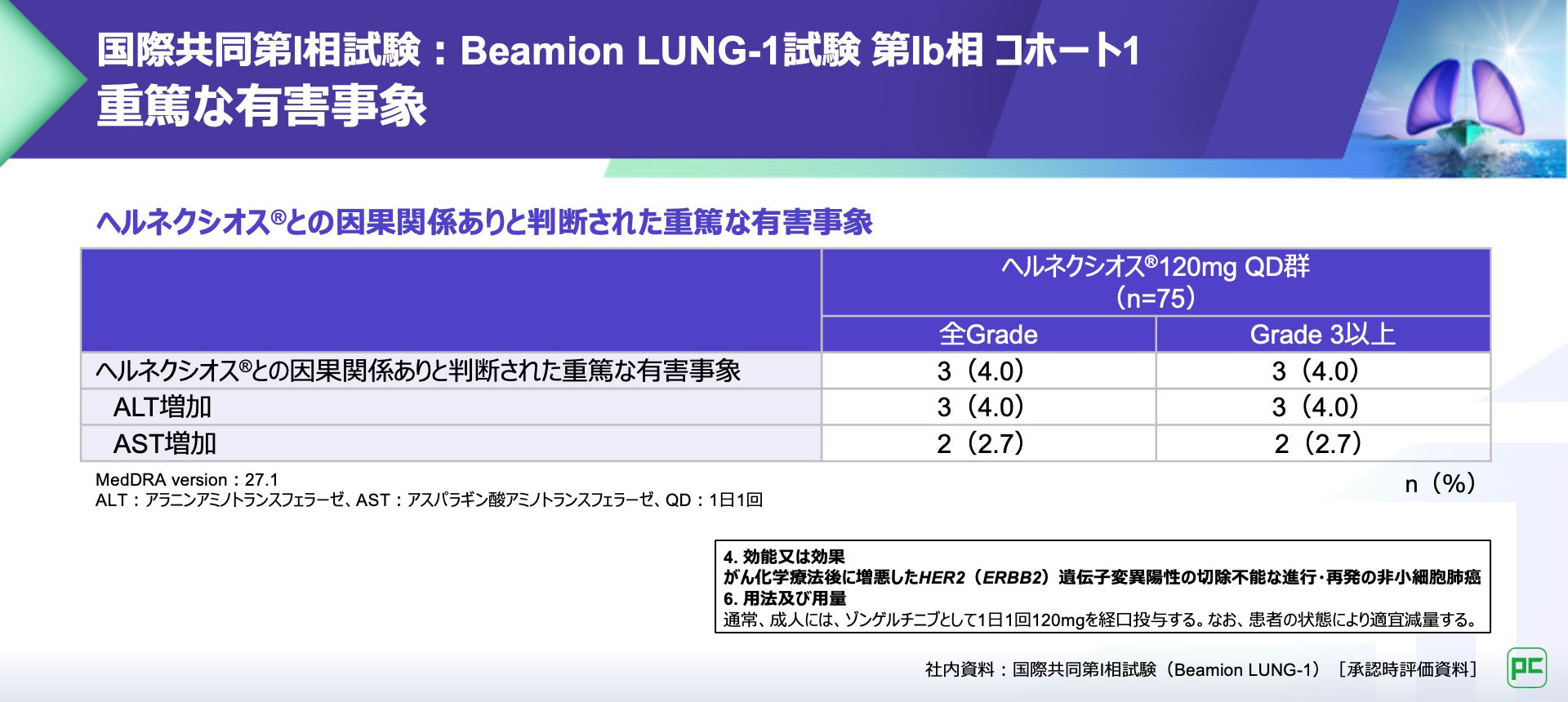
中止に至った有害事象は2例(2.7%)に認められ、ALT増加、AST増加、血中ALP増加、GGT増加及び発熱が報告されました。
休薬に至った有害事象は25例(33.3%)に認められ、2例以上にみられた有害事象はAST増加、駆出率減少、発疹、ALT増加及び嘔吐が報告されました。
減量に至った有害事象は5例(6.7%)に認められ、AST増加、ALT増加、好中球数減少、血中クレアチンホスホキナーゼ増加、GGT増加、高トランスアミナーゼ血症及び薬物性肝障害の疑いが報告されました。
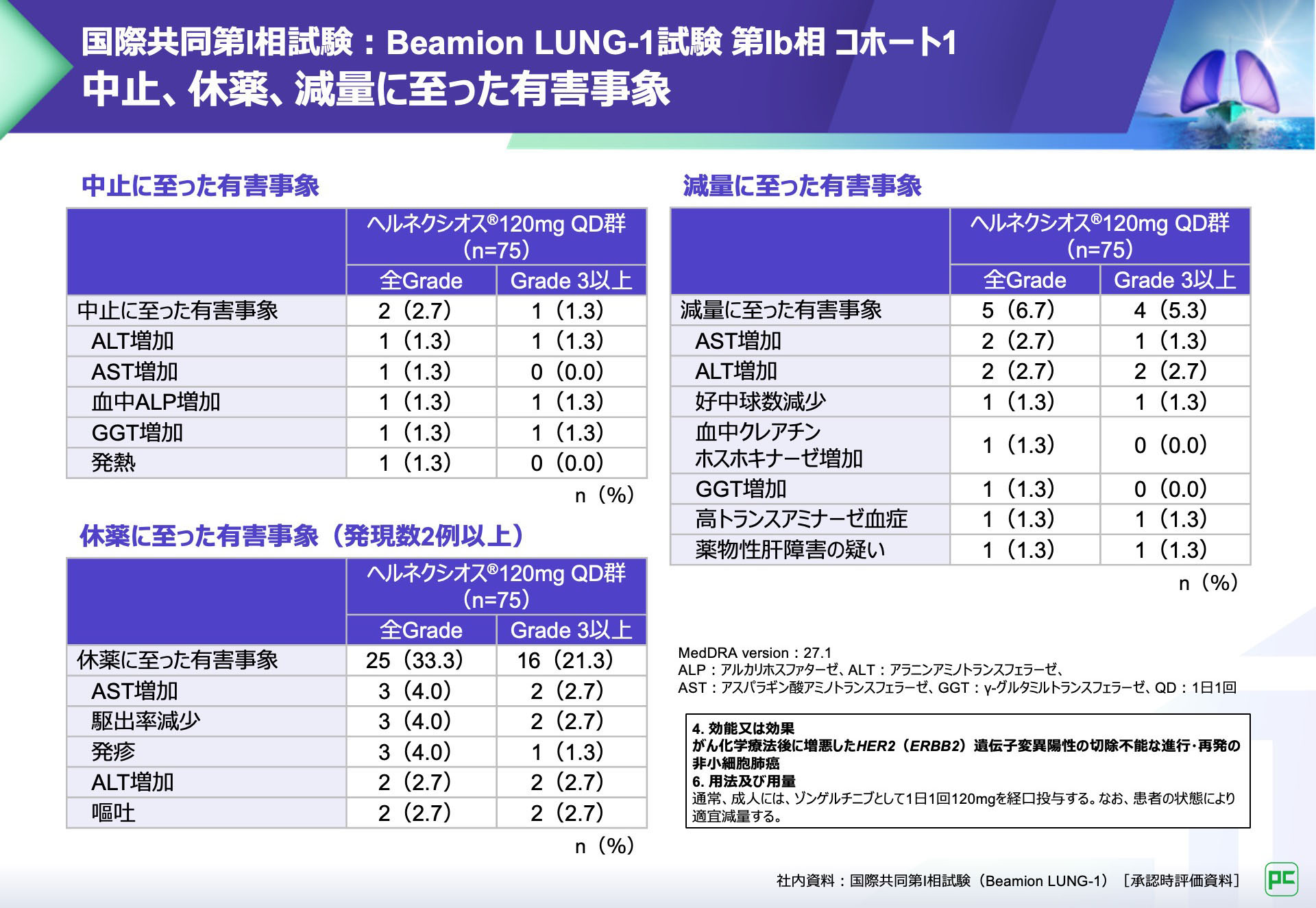
つづいて、コホート3の結果をご紹介する前に、各種バリアントに対するヘルネクシオス®の阻害活性について確認しましょう。
各種バリアントに対するヘルネクシオス®の阻害活性
ヘルネクシオス®は、TKD変異だけでなく、non-TKD変異(細胞外ドメイン、膜貫通ドメイン、その他のHER2遺伝子変異)を含む幅広いバリアントで阻害活性が確認されました。

薬理作用:野生型HER2及びHER2バリアント発現細胞におけるゾンゲルチニブの増殖抑制作用(in vitro)
S310F及びS310Yのように、TKD以外の細胞外ドメインにHER2遺伝子変異を有する細胞に対しても、ゾンゲルチニブはIC50値4nmol/L、2nmol/Lの低濃度で作用することが示されました。
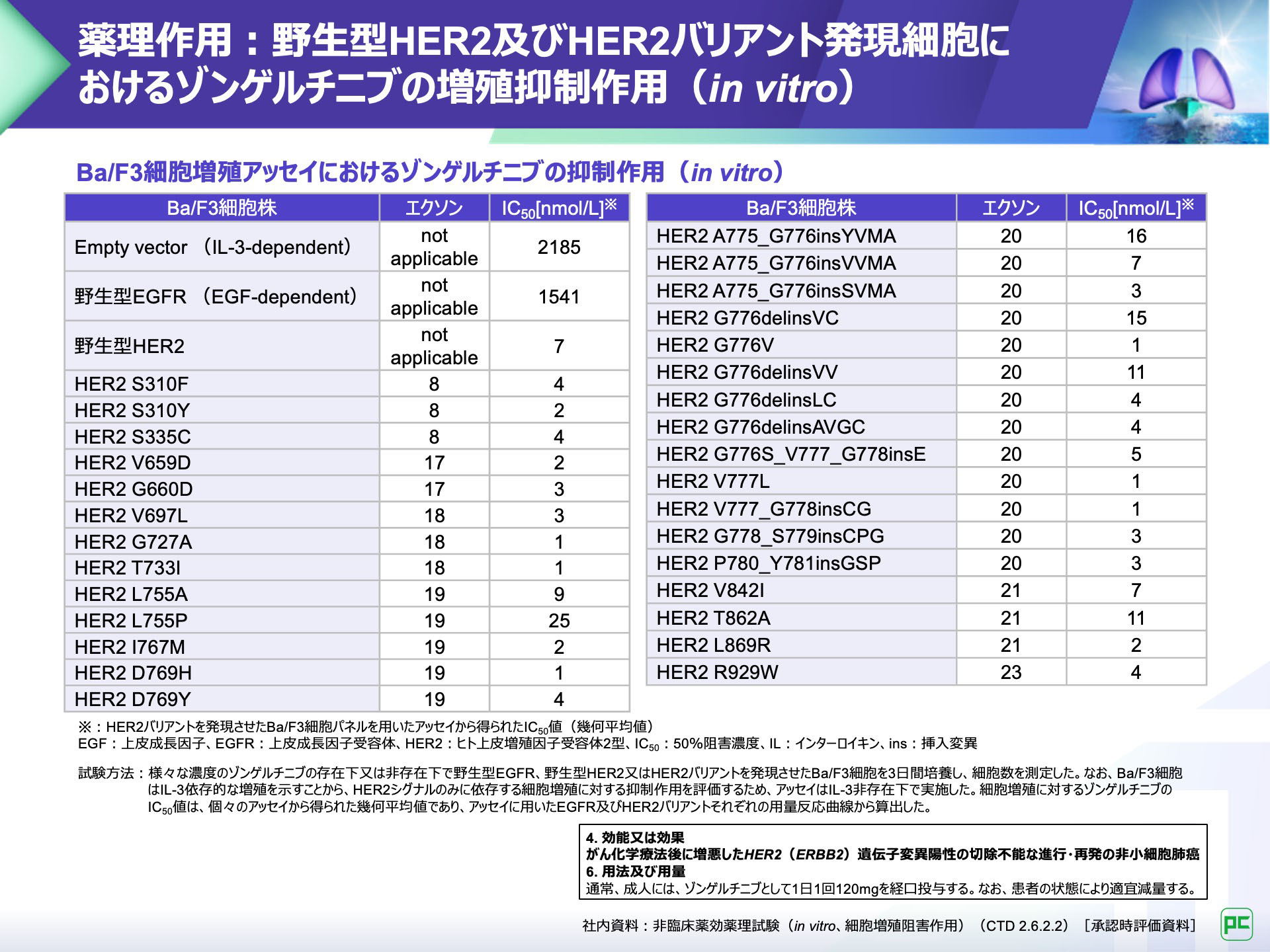
以上の内容を踏まえて、治療歴があるTKD変異以外のHER2変異陽性NSCLC患者及びHER2 TKD変異陽性扁平上皮NSCLC患者を対象としたコホート3の結果をご紹介します。
患者背景
コホート3の26例中、TKD変異以外のHER2変異を有する非扁平上皮NSCLC患者は20例で、そのうち二次治療の患者は8例(40%)でした。
TKD変異以外のHER2変異を有する非扁平上皮NSCLC患者20例のうち、S310F変異、V659E変異を有する患者はそれぞれ30%、S310Y変異を有する患者は20%でした。
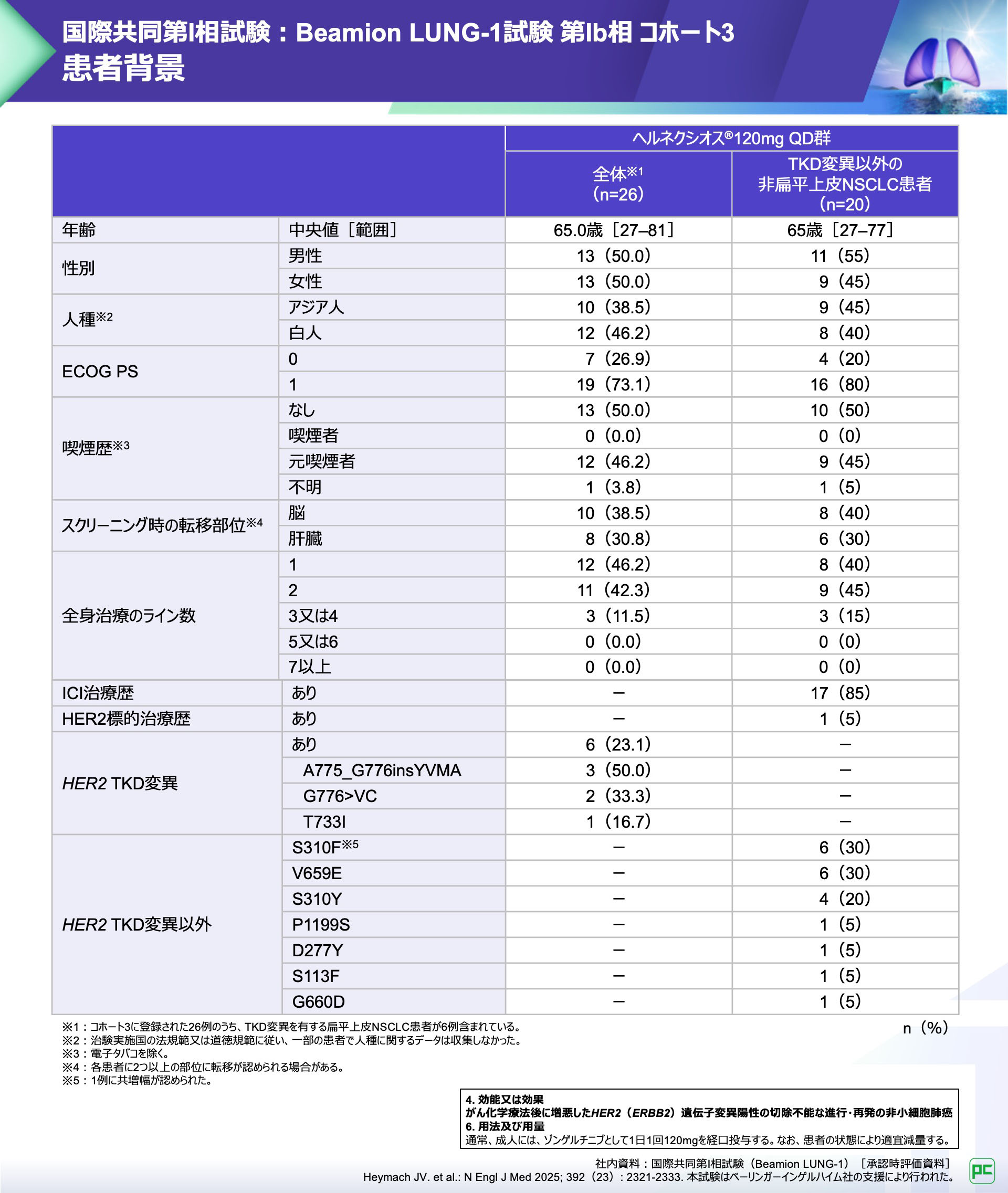
試験結果
主要評価項目である客観的奏効率(ORR※1)は30.8%(8/26例、95%CI:16.5-50.0)でした。
また、副次評価項目である病勢コントロール率(DCR※2)は69.2%でした。
※1:ORR=CR+PR、※2:DCR=CR+PR+SD

TKD変異以外のHER2変異を有する非扁平上皮NSCLC患者20例の客観的奏効率(ORR)は30.0%(6/20例、95%CI:14.5-51.9)でした。

腫瘍縮小率の推移(Spider plot)は以下のとおりでした。
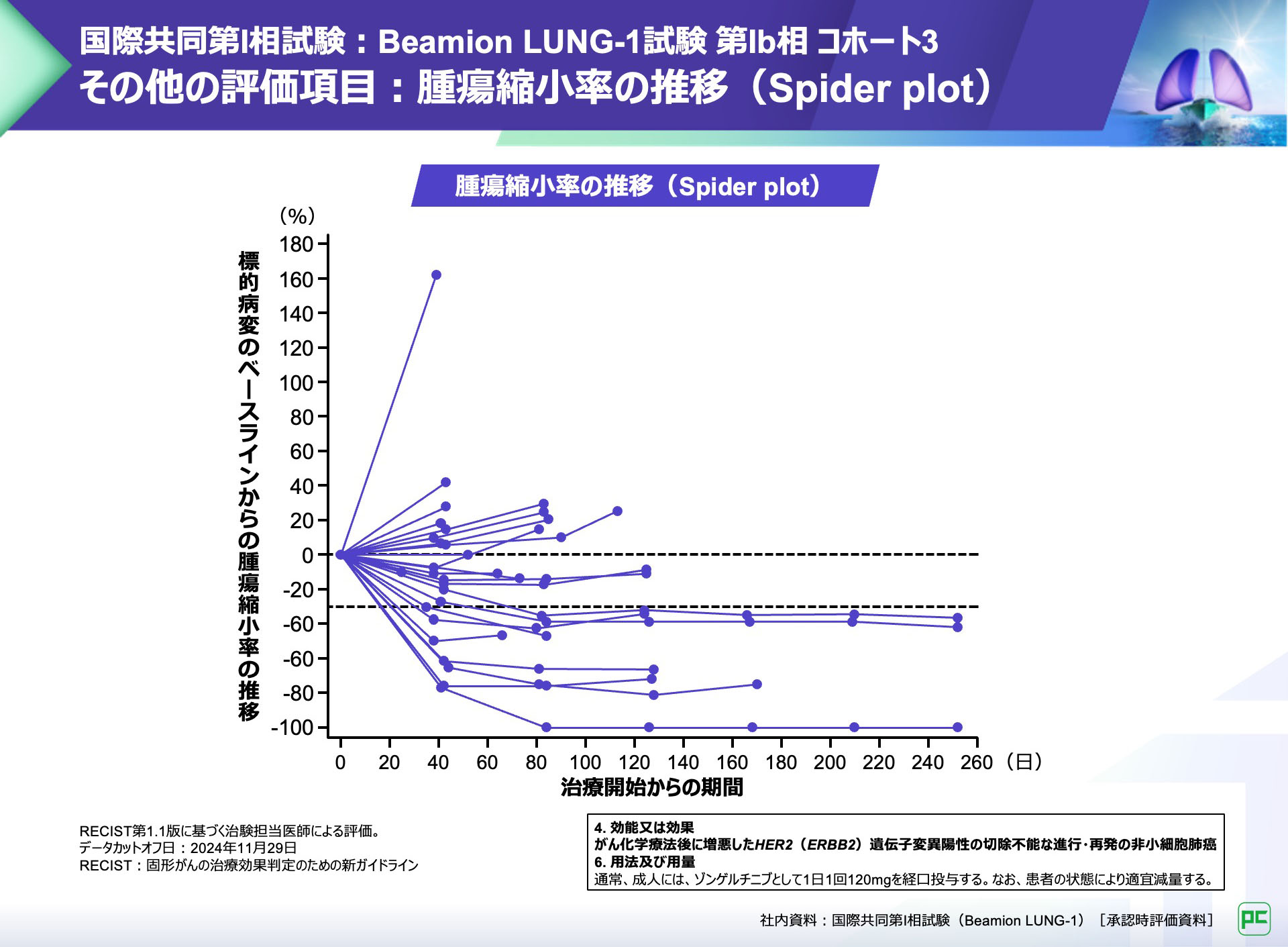
ヘルネクシオス®との因果関係ありと判断された有害事象は26例中20例(76.9%)に認められました。
主な有害事象は下痢10例(38.5%)、そう痒症5例(19.2%)、貧血、低カリウム血症、ALT増加及び血中クレアチニン増加各3例(11.5%)などでした。
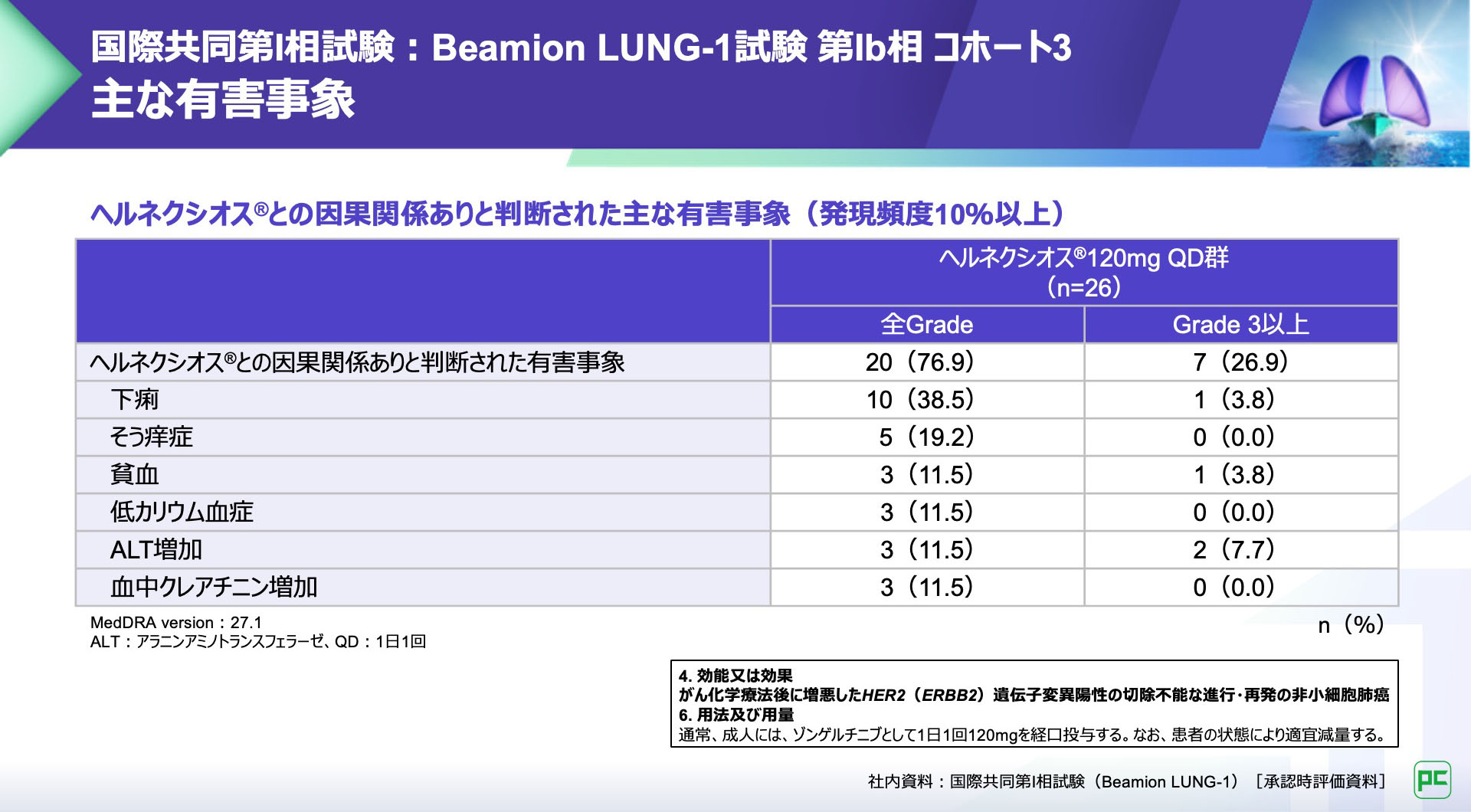
ヘルネクシオス®との因果関係ありと判断された重篤な有害事象は4例(15.4%)に認められ、薬物性肝障害及びALT増加などが報告されました。
ヘルネクシオス®との因果関係ありと判断された死亡に至った有害事象は報告がありませんでした。
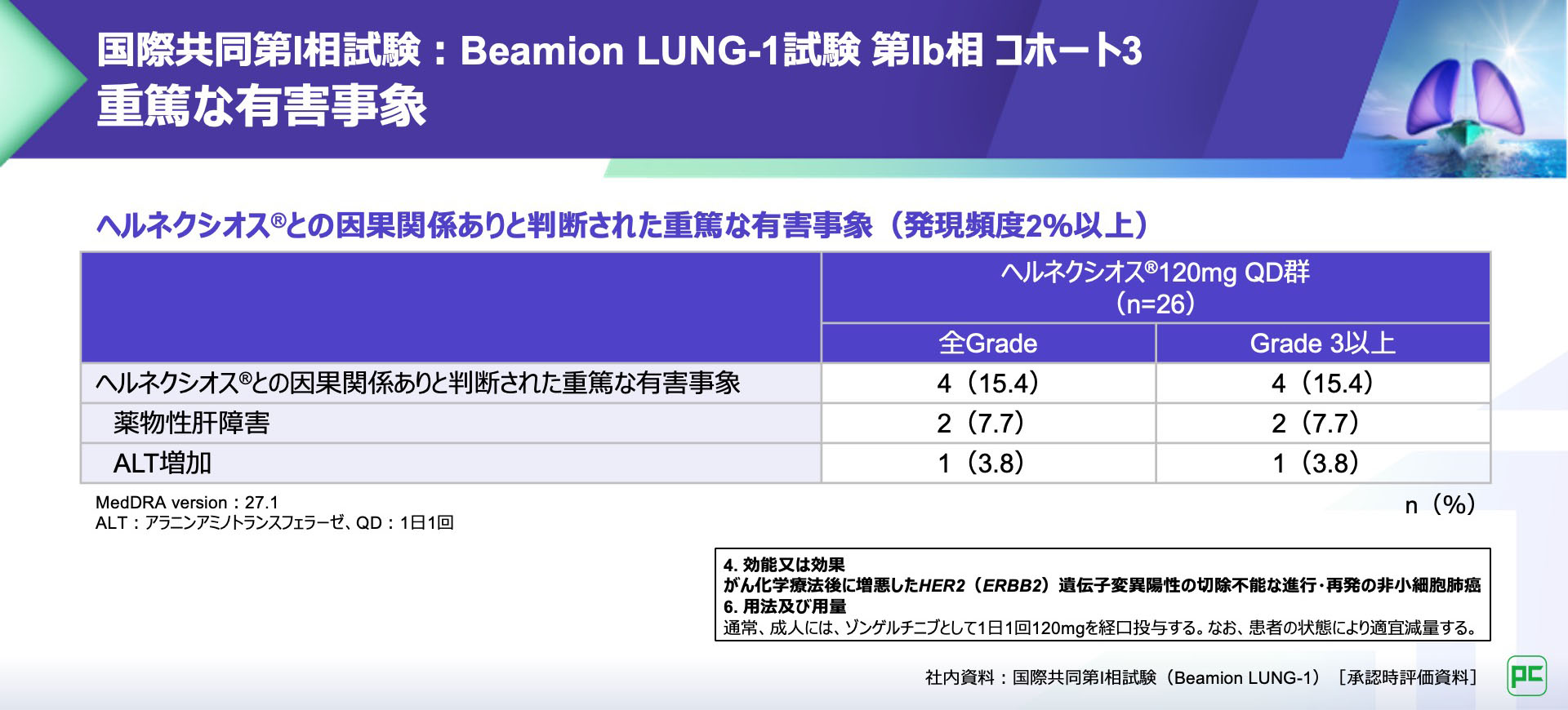
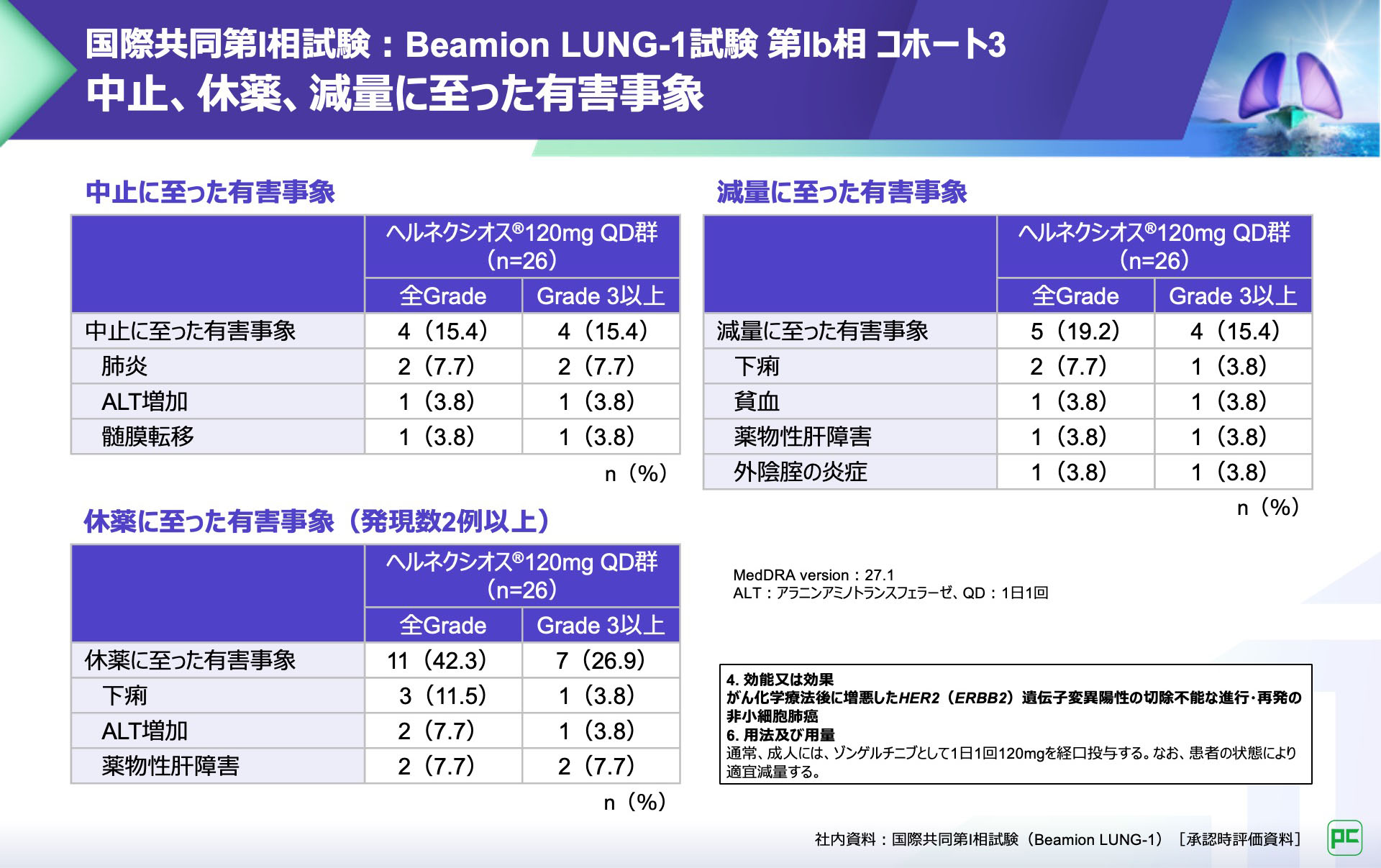
中止に至った有害事象は4例(15.4%)に認められ、肺炎、ALT増加及び髄膜転移が報告されました。
休薬に至った有害事象は11例(42.3%)に認められ、2例以上にみられた有害事象は、下痢、ALT増加及び薬物性肝障害が報告されました。
減量に至った有害事象は5例(19.2%)に認められ、下痢、貧血、薬物性肝障害及び外陰腟の炎症が報告されました。
【田中先生のお⾔葉】
HER2遺伝子変異の代表的なサブタイプには、エクソン20挿入変異、TKD変異、ECD変異、TMD変異などがあります。
日本人を対象とした報告では、TKD変異が89%を占めるのに対し、non-TKD変異は11%と少数であることが示されています1)。
ヘルネクシオス®は、Ba/F3細胞を用いた評価において、TKD変異だけでなく、non-TKD変異に対しても阻害活性を示しました5)。
今回ご紹介したBeamion LUNG-1試験のコホート3は、non-TKDのHER2変異陽性非扁平上皮NSCLC患者に焦点を当てて探索的な解析を行った貴重なデータです。本データから、ヘルネクシオス®はnon-TKD変異症例に対する治療選択肢の一つとして期待されます。
本コンテンツが、先生方の日常診療における治療方針決定の一助となれば幸いです。
1)Kato Y. et al.: Lung Cancer 2024; 197: 107992.
5)Wilding B. et al.: Cancer Discov 2025; 15(1): 119-138.
日本ベーリンガーインゲルハイム
メディカルチャット 利用規約
当社の「日本ベーリンガーインゲルハイム メディカルチャット」(以下「本サービス」といいます)のご利用に際しては、本利用規約が適用されますので、必ず以下の記載事項をご確認下さい。
利用規約
- 本サービスは、当社所定のウェブページから文字によりお問い合わせいただくことにより、当社医薬品等に関する一般的な情報を、人工知能あるいは当社担当者により、文字及び図表により回答するサービスです(以下、人工知能による回答サービスを「AIチャット」、当社担当者による回答サービスを「有人チャット」といいます。)。ただし、AIチャットによる回答を原則とし、有人チャットは、AIチャットでの回答に対し、有人チャットでの回答も希望された場合に、提供させていただきます。
- 本サービスをご利用いただくことができるのは、当社医薬品等を扱いかつ国内に在住する医療関係者の方に限られます。当該医療関係者以外の方は、ご利用いただくことができません。
- 本利用規約に同意いただけない場合、本サービスを利用いただくことができません。本利用規約を最後までお読みいただき、「同意して利用する」ボタンを押した上で、本サービスをご利用下さい。
- 本サービスは、当社医薬品等に関する一般的なお問い合わせに対して回答するものとし、次の各号に掲げるお問い合わせについては、回答しないものとします。
- 当社医薬品等と関係のないお問い合わせ、または本サービスの回答範囲を逸脱したお問い合わせ
- 具体的な症状や治療方法に関するお問合せ
- 当社に適用される法令、ガイドラインまたは行政上の指導、当社自主規制その他当社が遵守すべきルールにより回答できないお問い合わせ
- 文字化け等により入力内容が判断できないお問い合わせ
- 前各号に掲げるほか、本サービスにより、適切な回答をすることができないと当社が判断した事項に関するお問い合わせ
- 本サービスは、日本語のみに対応しています。
- 本サービスは、当社医薬品の副作用、不具合及び有害事象の報告を受け付けていません。
- お問い合わせの内容によっては、本サービスでは十分に回答できない場合もございます。予めご了承下さい。
- 本サービスの利用可能時間は、以下のとおりです。
- AIチャット
24時間365日 - 有人チャット
平日9:00~17:00
- AIチャット
- 前項に関わらず、メンテナンス及び障害等のため一時的に本サービスを中断する場合がございます。
本サービスのご利用の際には、原則として、個人情報(お名前、ご住所、電話番号、メールアドレス等)を入力しないようお願いします。ただし、AIチャット及び有人チャットを問わず、当社医薬品の適用外使用に関するお問い合わせについては、コンプライアンス上の理由により、当社より、氏名及び施設名の入力を求める場合がございます。この場合には、当社プライバシーポリシーの内容を確認いただき、同意いただける場合に限り、入力して下さい(プライバシーポリシーについては「VIII 利用規約、プライバシーポリシー」に記載のURLからアクセス下さい)。その他の場合に、当社より個人情報の入力を求めることは一切ございません。
- 当社医薬品のご使用にあたっては、最新の添付文書等をご確認下さい。
- 当社は、本サービスまたは本サービスにより提供される情報の利用に際し生じた結果については、一切責任を負いません。
本サービスの利用にあたり、以下の各号の行為を禁止します。
- 本サービスにより提供される情報を複製、複写、転載、改変等する行為
- 第三者または当社の知的財産権その他の権利を侵害する行為
- 第三者または当社を誹謗中傷し、または名誉・信用を毀損する行為
- 本サービスの利用による営利目的の行為
- 本サービスの運営又は他の利用者による本サービスの利用の妨げとなる行為
- 前各号のほか、当社が不適当であると判断する行為
当社は、いつでも本サービスの提供を終了、またはその内容を変更することができるものとします。
本サービスの利用に関しては、以下の利用規約及びプライバシーポリシーが併せて適用されますので、ご確認下さい。


