
加来先生に伺うSGLT2阻害薬の脱水予防と飲水に関するアドバイス
サイトへ公開:2021年01月30日 (土)
クイックリンク

SGLT2阻害薬は2014年に上市され、現在国内では6成分8製剤が存在します。大規模臨床試験の結果や合剤の発売により近年SGLT2阻害薬の処方が増加している中、今回川崎医科大学の加来浩平先生より、SGLT2阻害薬の脱水予防や投与初期・継続期其々に応じた患者さんへの飲水の指導について御紹介頂きます。
監修:加来 浩平 先生(川崎医科大学 名誉教授)
脱水予防のための患者指導
投与初期 喉が渇く前に水分を摂る
SGLT2阻害薬投与初期は尿量増加がみられており、患者さんへの十分な飲水指導が必要です。
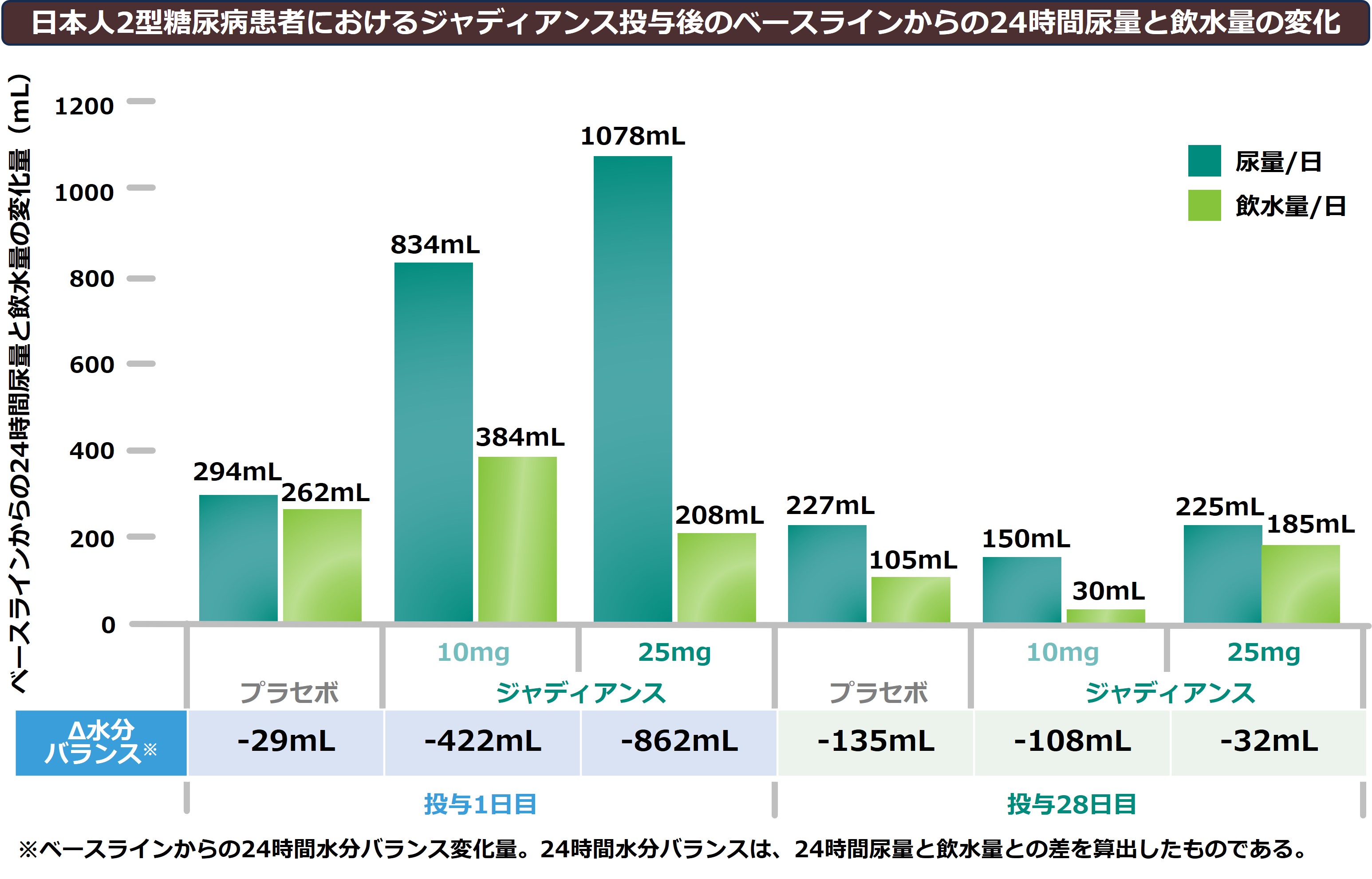
投与1日目において、ジャディアンス10mg群ではプラセボ群に比べて、約500mLの尿量増加が示されています1)
日常生活の注意
- こまめに水分を摂る 例:朝(起床後)、トイレの後、入浴前後
- 気温が高い時期には、喉が渇いていなくても早めの水分補給を心がける
投与継続期: 喉が渇いたら水分を摂る
投与初期にみられた尿量増加は、持続的にはみられません。
SGLT2阻害薬投与時の尿量は飲水量が規定因子となり2)、飲水量や回数を過度に増やすことが尿量の増加や頻尿に繋がります。
高齢者: SGLT2阻害薬投与に関わらず、普段からこまめに水分を摂る
体液量減少の有害事象は、SGLT2阻害薬投与に関わらず高齢になるにつれ発現率が高くなります。
Q&A
Q: 投与初期の目安はどれぐらいでしょうか?
A: 投与開始後1週間程度が一つの目安です。
加来先生 解説
ジャディアンスで日本人を対象に検討した試験において、投与28日目のベースラインからの尿量の変化はプラセボとジャディアンス群で同程度であり、また海外データでは5日目に尿量がベースライン時と同程度であることが示されています3)。
同様に他SGLT2阻害薬の日本人で検討した試験においても、投与1日目には尿量増加が認められましたが、投与2日目で尿量がベースライン時と変わらないことが示されています2)。
1) Yasui A, et al.: Diabetes Ther. 2018; 9: 863-71.
2) Tanaka H, et al,: Adv Ther 2017; 34: 436-51. 他のSGLT2阻害薬での検討に基づく。
3) Heise T et al.: Clin Ther 2016;38:2265-76.
国内で承認された用法・用量(抜粋)
<2型糖尿病>
通常、成人にはエンパグリフロジンとして10mgを1日1回朝食前又は朝食後に経口投与する。なお、効果不十分な場合には、経過を十分に観察しながら25mg 1日1回に増量することができる。
日本人2型糖尿病患者における24時間尿量と飲水量の評価
| 本データは、日本人2型糖尿病患者を対象にジャディアンス(エンパグリフロジン)のPK/PD、安全性、忍容性を検討した国内第Ⅱ相試験の事後解析によるものです。SGLT2阻害薬を適正使用いただくにあたり必要な情報であるとの判断のもと、掲載しております。 |

国内で承認された用法・用量(抜粋)
<2型糖尿病>
通常、成人にはエンパグリフロジンとして10mgを1日1回朝食前又は朝食後に経口投与する。なお、効果不十分な場合には、経過を十分に観察しながら25mg 1日1回に増量することができる。
Yasui A. et al.: Diabetes Ther. 2018; 9:863-71. 本試験はベーリンガーインゲルハイム社の支援により行われました。
日本人2型糖尿病患者24時間尿量と飲水量評価試験安全性
- 有害事象はエンパグリフロジン群の23/79例(29.1%)、プラセボ群の2/21例(9.5%)に認められ、主な事象はエンパグリフロジン群の便秘、鼻咽頭炎(各4例)であった。エンパグリフロジン群の1mg投与患者1例に重篤な有害事象として一過性脳虚血性発作が認められた。プラセボ群の1例で、投与中止に至った有害事象として高血糖が認められた。死亡の報告はなかった。
- 本試験において、脱水関連の有害事象はジャディアンス群およびプラセボ群において認められなかった。
- ジャディアンスの安全性については、DIスライドの安全性情報をご参照ください。
Yasui A. et al.: Diabetes Ther. 2018; 9:863-71. 本試験はベーリンガーインゲルハイム社の支援により行われました。
投与1日目にジャディアンス投与群で認められた尿量の増加は、投与28日目には認められませんでした。また、同様に水分バランス*の変化を検討したところ、投与28日目では、ジャディアンス10mg群で-108ml、25mg群で-32mL、プラセボ群で-135mlでした。これらは、日本人2型糖尿病患者にジャディアンスを投与した際に、水分バランスを維持する腎臓の生理学的なメカニズムが働いている事によるものと推測されます。
*水分バランス:24時間尿量と飲水量の差と定義
安全性併合解析(SAF43)

国内で承認された用法・用量(抜粋)
<2型糖尿病>
通常、成人にはエンパグリフロジンとして10mgを1日1回朝食前又は朝食後に経口投与する。なお、効果不十分な場合には、経過を十分に観察しながら25mg 1日1回に増量することができる。
効能又は効果、用法及び用量、禁忌を含む注意事項等情報等については電子添文をご確認ください。
Schorling OK, et al.: Adv Ther. 2020; 37(8): 3463-3484. 本試験はベーリンガーインゲルハイム社/イーライリリー社の支援により行われました。
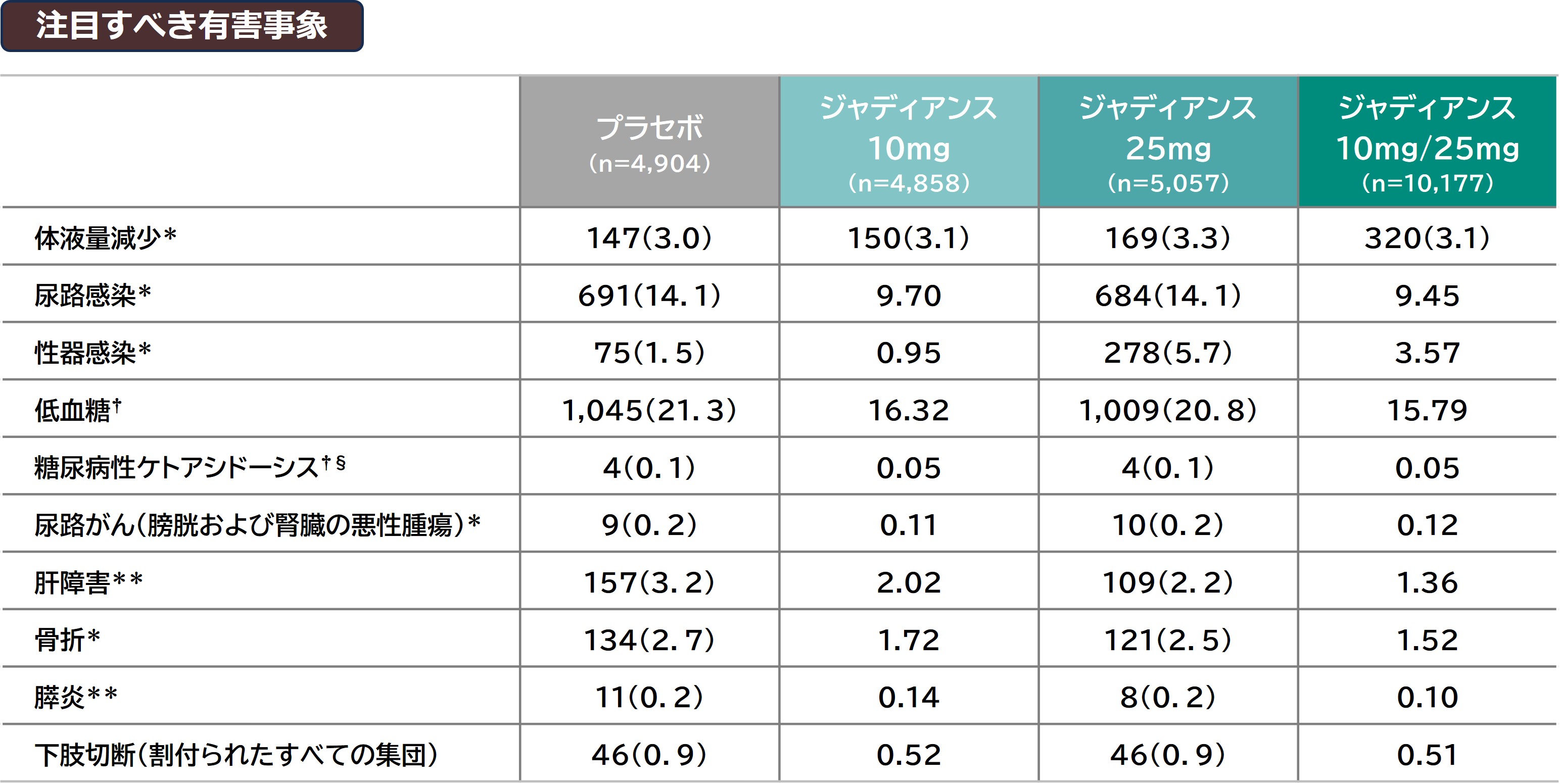
特に記載のない限りデータはn(%)。 %は、治療ごとの患者の総数を分母とする。
同一患者において複数事象を発現している場合を含む。
* BIcMQ(ベーリンガーインゲルハイム社がカスタマイズしたMedDRA検索式)によるMedDRA基本語に基づく。 MedDRA:Medical Dictionary for Regulatory Activities
† 狭義のSMQ(standardized MedDRA query)に基づく ‡ 狭義のBIcMQ(ベーリンガーインゲルハイム社がカスタマイズしたMedDRA検索式)に基づく
§ SAF42と比較してプラセボ群のイベント数が少なvいのは、MedDRAマッピング定義のバージョン間の変更による。
(例:下層語「糖尿病性ケトーシス」はv 18.0では基本語「糖尿病性ケトアシドーシス」に属するが、v 21.0では変更されている)
* * SMQ(standardized MedDRA query)に基づく
効能又は効果、用法及び用量、禁忌を含む注意事項等情報等については電子添文をご確認ください。
Schorling OK, et al.: Adv Ther. 2020; 37(8): 3463-3484. 本試験はベーリンガーインゲルハイム社/イーライリリー社の支援により行われました。
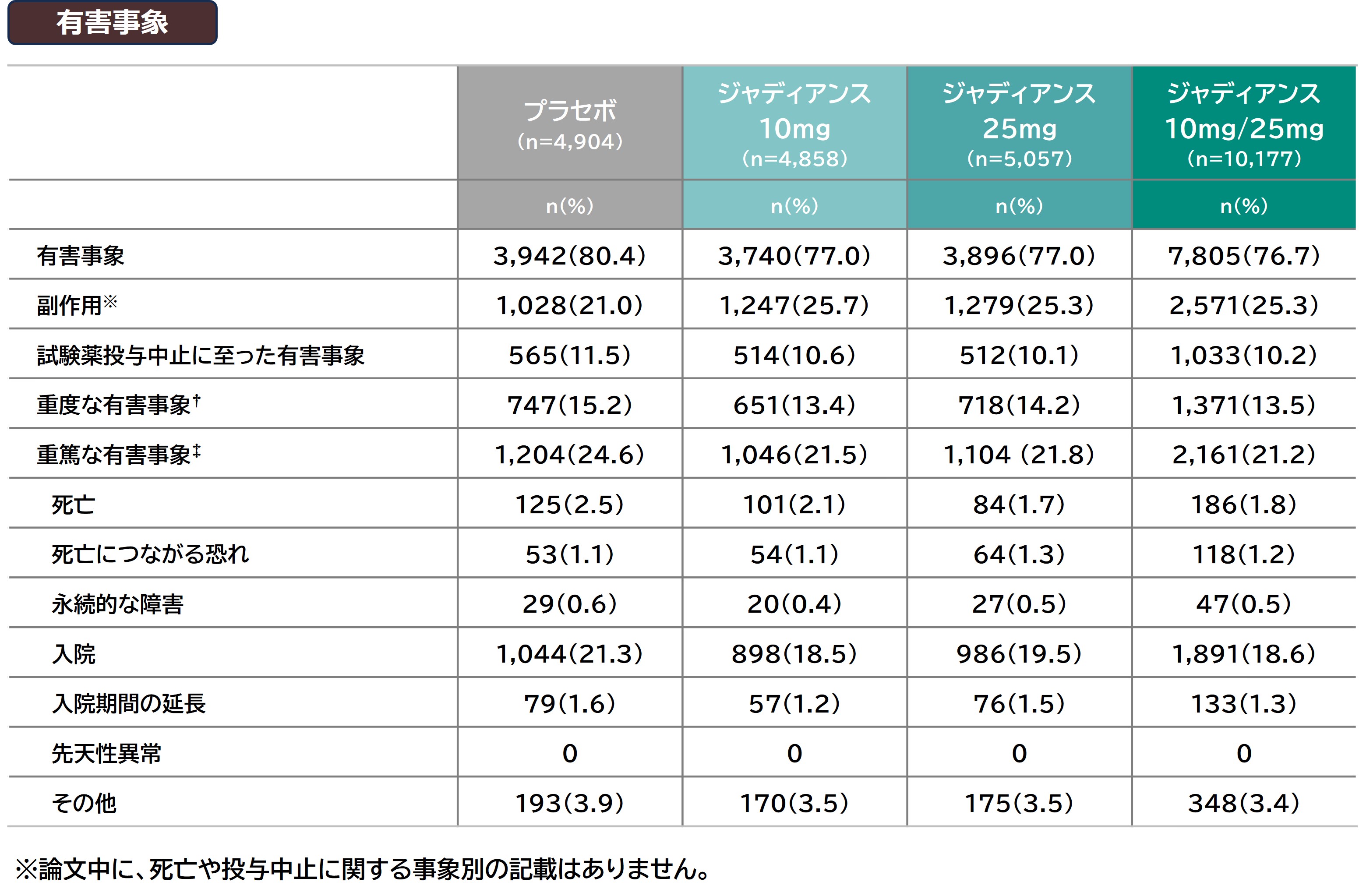
患者は複数の重症度基準にカウントされている場合がある。MedDRA:Medical Dictionary for Regulatory Activities
* 試験責任医師により薬剤との関連性ありと判断された有害事象
† 重度な有害事象とは仕事または日常生活ができない程度の徴候または症状。
‡ 重篤な有害事象とは死をもたらすもの、直ちに生命を脅かしうるもの、持続的もしくは永続的な障害をもたらすもの、患者の入院が必要となるものまたは入院期間の延長が必要となるもの、
先天性異常/出生時異常またはあらゆる他の理由で深刻であると考えられるもの。
効能又は効果、用法及び用量、禁忌を含む注意事項等情報等については電子添文をご確認ください。
Schorling OK, et al.: Adv Ther. 2020; 37(8): 3463-3484. 本試験はベーリンガーインゲルハイム社/イーライリリー社の支援により行われました。
監修者のコメント:川崎医科大学 名誉教授 加来 浩平 先生
SGLT2阻害薬投与中は、適度な水分補給の指導が大切です。SGLT2阻害薬投与による循環血漿量に与える影響を考慮すると、過度な飲水は尿量増加の原因となるため、患者さんの状態を考慮し指導する必要があります。 健康寿命の確保やQOL改善を観点に、年齢や体重に捉われずSGLT2阻害薬が幅広い患者さんに投与されることを期待します。
| 8. 重要な基本的注意(抜粋) 〈効能共通〉 8.5 本剤の利尿作用により多尿・頻尿がみられることがある。また、体液量が減少することがあるので、適度な水分補給を行うよう指導し、観察を十分行うこと。脱水、血圧低下等の異常が認められた場合は、休薬や補液等の適切な処置を行うこと。特に体液量減少を起こしやすい患者(高齢者、腎機能障害患者、利尿薬併用患者等)においては、脱水や糖尿病性ケトアシドーシス、高浸透圧高血糖症候群、脳梗塞を含む血栓・塞栓症等の発現に注意すること。 |
その他の関連情報


CKDの患者さんの食事制限とCKD治療(動画)
日本ベーリンガーインゲルハイム
メディカルチャット 利用規約
当社の「日本ベーリンガーインゲルハイム メディカルチャット」(以下「本サービス」といいます)のご利用に際しては、本利用規約が適用されますので、必ず以下の記載事項をご確認下さい。
利用規約
- 本サービスは、当社所定のウェブページから文字によりお問い合わせいただくことにより、当社医薬品等に関する一般的な情報を、人工知能あるいは当社担当者により、文字及び図表により回答するサービスです(以下、人工知能による回答サービスを「AIチャット」、当社担当者による回答サービスを「有人チャット」といいます。)。ただし、AIチャットによる回答を原則とし、有人チャットは、AIチャットでの回答に対し、有人チャットでの回答も希望された場合に、提供させていただきます。
- 本サービスをご利用いただくことができるのは、当社医薬品等を扱いかつ国内に在住する医療関係者の方に限られます。当該医療関係者以外の方は、ご利用いただくことができません。
- 本利用規約に同意いただけない場合、本サービスを利用いただくことができません。本利用規約を最後までお読みいただき、「同意して利用する」ボタンを押した上で、本サービスをご利用下さい。
- 本サービスは、当社医薬品等に関する一般的なお問い合わせに対して回答するものとし、次の各号に掲げるお問い合わせについては、回答しないものとします。
- 当社医薬品等と関係のないお問い合わせ、または本サービスの回答範囲を逸脱したお問い合わせ
- 具体的な症状や治療方法に関するお問合せ
- 当社に適用される法令、ガイドラインまたは行政上の指導、当社自主規制その他当社が遵守すべきルールにより回答できないお問い合わせ
- 文字化け等により入力内容が判断できないお問い合わせ
- 前各号に掲げるほか、本サービスにより、適切な回答をすることができないと当社が判断した事項に関するお問い合わせ
- 本サービスは、日本語のみに対応しています。
- 本サービスは、当社医薬品の副作用、不具合及び有害事象の報告を受け付けていません。
- お問い合わせの内容によっては、本サービスでは十分に回答できない場合もございます。予めご了承下さい。
- 本サービスの利用可能時間は、以下のとおりです。
- AIチャット
24時間365日 - 有人チャット
平日9:00~17:00
- AIチャット
- 前項に関わらず、メンテナンス及び障害等のため一時的に本サービスを中断する場合がございます。
本サービスのご利用の際には、原則として、個人情報(お名前、ご住所、電話番号、メールアドレス等)を入力しないようお願いします。ただし、AIチャット及び有人チャットを問わず、当社医薬品の適用外使用に関するお問い合わせについては、コンプライアンス上の理由により、当社より、氏名及び施設名の入力を求める場合がございます。この場合には、当社プライバシーポリシーの内容を確認いただき、同意いただける場合に限り、入力して下さい(プライバシーポリシーについては「VIII 利用規約、プライバシーポリシー」に記載のURLからアクセス下さい)。その他の場合に、当社より個人情報の入力を求めることは一切ございません。
- 当社医薬品のご使用にあたっては、最新の添付文書等をご確認下さい。
- 当社は、本サービスまたは本サービスにより提供される情報の利用に際し生じた結果については、一切責任を負いません。
本サービスの利用にあたり、以下の各号の行為を禁止します。
- 本サービスにより提供される情報を複製、複写、転載、改変等する行為
- 第三者または当社の知的財産権その他の権利を侵害する行為
- 第三者または当社を誹謗中傷し、または名誉・信用を毀損する行為
- 本サービスの利用による営利目的の行為
- 本サービスの運営又は他の利用者による本サービスの利用の妨げとなる行為
- 前各号のほか、当社が不適当であると判断する行為
当社は、いつでも本サービスの提供を終了、またはその内容を変更することができるものとします。
本サービスの利用に関しては、以下の利用規約及びプライバシーポリシーが併せて適用されますので、ご確認下さい。



